Endoprotetika velkých kloubů – novinky a trendy v perioperační péči
Endoprotetika kyčelního a kolenního kloubu patří k celosvětově nejčastěji prováděným a současně také nejefektivnějším operačním výkonům. Vzhledem ke zvyšujícímu se průměrnému dožití populace a v souvislosti s potřebou delší doby aktivního životního stylu lze v následujících dekádách očekávat významný nárůst počtu implantovaných kloubních náhrad.
To potvrzují i závěry mezinárodních studií, v nichž ty „ortopedicky nejoptimističtější“ předpokládají u tohoto typu operace v následujícím desetiletí nárůst až o několik set procent. Logistické, technické a zejména personální kapacity stávajících ortopedických pracovišť nebudou tomuto nárůstu při současném nastavení poskytované péče dostačovat, a bude tak potřeba vytvářet nové požadavky na úpravu koncepce pracovišť spolu se zefektivněním perioperační péče o příslušné pacienty. Výsledkem by mělo být postupné zkracování doby hospitalizace a zmenšování objemu nutně poskytované péče při zachování současné vysoké kvalitativní úrovně našeho zdravotnictví. Na mnoha špičkových zahraničních pracovištích je již dlouhou dobu běžné, že pacienti po náhradě velkého kloubu odcházejí v den operace domů, a to včetně jedinců s četnými interními komorbiditami a často ne zcela perfektním domácím zázemím. V následujícím textu se pokusíme shrnout principy systému „Enhanced Recovery After Surgery“ (ERAS), jehož zásadami se na našem pracovišti řídíme ve snaze o zefektivnění a zrychlení celého perioperačního procesu. Úhradové mechanismy českého zdravotnictví doposud potenciál a efektivitu tohoto nastavení endoprotetiky nereflektují, budou‑li však do budoucna kopírovat trendy zdravotnictví západoevropských zemí, budeme se s nimi v České republice setkávat stále častěji. Vzhledem k aktuálnosti a rozmachu tohoto tématu věříme, že informace obsažené v tomto sdělení budou přínosné pro odborníky napříč lékařskými obory, kteří v některé části léčebného procesu přicházejí do styku s kloubně‑endoprotetickými pacienty, zejména však pro praktické lékaře, protože právě u nich často „cesta pacienta“ začíná.
Obecné informace
Systém ERAS představuje multimodální a multidisciplinární soubor 17 opatření a principů zefektivňujících zotavení pacienta po operačním výkonu.1 Jedná se o sumarizaci evidence‑based postupů, které jsou tzv. ERAS® Society pravidelně aktualizovány. Své uplatnění postupně nacházejí ve všech chirurgických oborech, primárně v oblasti elektivních operačních výkonů, kdy lze jednotlivé fáze perioperačního procesu ovlivnit již s předstihem. Hlavními výhodami celého konceptu by měly být redukce předoperačního stresu pacienta, a tedy zlepšení jeho psychické a fyzické adaptability, dále pak snížení incidence komplikací a zkrácení délky hospitalizace při zachování optimálního standardu péče. Na druhou stranu je nutno podotknout, že doslovné plnění všech bodů je zatím stále ovlivňováno společenskými a kulturními zvyklostmi jednotlivých zemí a pracovišť. Proto je namístě jejich částečná individuální adaptace a optimalizace dle konkrétního prostředí, což i sama Společnost pro ERAS doporučuje.
Základní principy ERAS a jejich vztah k endoprotetice
- Předoperační ambulantní konzultace
 V četných studiích byl prokázán význam předoperační edukace pacienta, a to zejména ve smyslu jeho připravenosti, což může zásadně ovlivnit subjektivní vnímání celého procesu. Významnými aspekty jsou také snížení potřeby analgetik a incidence perioperačních komplikací charakteru poruch hojení rány či nedodržení pooperačního režimu.2,3 Již při vstupním pohovoru v rámci indikačního vyšetření pacienta informujeme o typickém průběhu jeho hospitalizace s akcentací nutnosti brzké pooperační vertikalizace a cílem časné dimise do domácího prostředí. Pacient je dále informován o nutnosti již preemptivní úpravy domácího prostředí. Dle analýzy autorů Pelt et al.2 byl potvrzen přímý vliv optimalizace předoperační informovanosti na zkrácení délky hospitalizace pacientů po implantaci totální endoprotézy (TEP) velkého kloubu (kyčel, koleno). Na našem pracovišti se neustálým zdokonalováním konceptu dostatečné informovanosti zabýváme důkladně – příkladem je např. tvorba informačních brožur a videí či pravidelné pořádání informačních přednášek pro pacienty. Jedná se o projekt s názvem Pacientská akademie. V rámci souboru přednášek, které vedou zdravotníci provázející pacienty v průběhu jejich terapie od příjmu až po propuštění, mají pacienti možnost vyslechnout prezentaci toho, jak bude jejich hospitalizace probíhat. Svůj pohled představuje mladší lékař ortoped – L1 či L2, který pacienty například přijímá na kliniku či zajišťuje denní vizity pacienta u lůžka, starší lékař ortoped – L3, který endoprotézy nejčastěji implantuje, dále anesteziolog, rehabilitační lékař, všeobecná sestra z lůžkového oddělení, perioperační sestra z operačního sálu a fyzioterapeut. V rámci těchto akademií mají pacienti možnost absolvovat školu chůze o francouzských holích a ptát se na vše, co jim v předoperačním období způsobuje nejistotu (obr. 1).
V četných studiích byl prokázán význam předoperační edukace pacienta, a to zejména ve smyslu jeho připravenosti, což může zásadně ovlivnit subjektivní vnímání celého procesu. Významnými aspekty jsou také snížení potřeby analgetik a incidence perioperačních komplikací charakteru poruch hojení rány či nedodržení pooperačního režimu.2,3 Již při vstupním pohovoru v rámci indikačního vyšetření pacienta informujeme o typickém průběhu jeho hospitalizace s akcentací nutnosti brzké pooperační vertikalizace a cílem časné dimise do domácího prostředí. Pacient je dále informován o nutnosti již preemptivní úpravy domácího prostředí. Dle analýzy autorů Pelt et al.2 byl potvrzen přímý vliv optimalizace předoperační informovanosti na zkrácení délky hospitalizace pacientů po implantaci totální endoprotézy (TEP) velkého kloubu (kyčel, koleno). Na našem pracovišti se neustálým zdokonalováním konceptu dostatečné informovanosti zabýváme důkladně – příkladem je např. tvorba informačních brožur a videí či pravidelné pořádání informačních přednášek pro pacienty. Jedná se o projekt s názvem Pacientská akademie. V rámci souboru přednášek, které vedou zdravotníci provázející pacienty v průběhu jejich terapie od příjmu až po propuštění, mají pacienti možnost vyslechnout prezentaci toho, jak bude jejich hospitalizace probíhat. Svůj pohled představuje mladší lékař ortoped – L1 či L2, který pacienty například přijímá na kliniku či zajišťuje denní vizity pacienta u lůžka, starší lékař ortoped – L3, který endoprotézy nejčastěji implantuje, dále anesteziolog, rehabilitační lékař, všeobecná sestra z lůžkového oddělení, perioperační sestra z operačního sálu a fyzioterapeut. V rámci těchto akademií mají pacienti možnost absolvovat školu chůze o francouzských holích a ptát se na vše, co jim v předoperačním období způsobuje nejistotu (obr. 1).
- Dosažitelná kompenzace interních komorbidit v předoperační fázi
Pro efektivní rehabilitaci (RHB) pacienta a v zájmu možnosti jeho časného propuštění je velmi důležitá stabilizace jeho celkového stavu. Nejedná se však pouze o medikamentózní kompenzaci interních komorbidit, nýbrž jde i o regulaci návyků, jež lze svépomocí ovlivnit. Dle studie autorů Pierre et al.4 pacienti, kteří přestali s kouřením alespoň čtyři týdny před operací, vykazovali o 25 % méně pooperačních respiračních komplikací ve srovnání s jedinci aktivně kouřícími v době výkonu. Stejně tak nadměrná konzumace alkoholu může být spojena s vyšší incidencí přidružených infekčních komplikací, případně s prodloužením doby hospitalizace.5 Velmi rizikovým faktorem je obezita II. a III. stupně (index tělesné hmotnosti [BMI] > 35, resp. > 40 kg/m2) vzhledem k možným komplikacím s anestezií a dále ve smyslu poruch hojení rány nebo prodloužené RHB.6 Na našem pracovišti z těchto důvodů nejsou přijímáni k elektivní implantaci TEP pacienti s BMI > 40 kg/m2. Těmto pacientům je doporučena konzultace v obezitologické ambulanci a při dosažení požadované redukce hmotnosti je provedeno nové indikační vyšetření. Dalším důležitým faktorem je dostatečná kompenzace v krevním obraze vzhledem k riziku perioperačních krevních ztrát, dále pak kontrola hodnoty albuminu při prokazatelně vyšší incidenci poruch hojení rány u pacientů s jeho deficiencí.7
- Prevence dehydratace a malnutrice
Dle aktuálních doporučení lze omezit lačnění před elektivním výkonem na 6 hodin, poslední příjem tekutin je pak povolen ještě 2 hodiny před operací. Delší lačnění může indukovat katabolickou reakci organismu s rozvojem inzulinové rezistence, která je asociována s prodlouženým hojením.8 Na naší klinice podáváme pacientům před operací sacharidové nápoje k zajištění optimální hydratace a tzv. nasycení sacharidy – „carb‑loading“, které podle některých studií8 může přispět k redukci pooperační ztráty svalové tkáně.
- Multimodální analgezie
V rámci pooperačního stavu po TEP je doporučeno regulovat bolesti kombinací různých skupin analgetik.9 Vzhledem k četným nežádoucím účinkům (např. respirační útlum, nauzea, močová retence), a tedy možnému omezení při časné RHB, není doporučeno podávat opiáty paušálně všem pacientům, pokud to není nezbytně nutné při velmi intenzivních bolestech.9 Základní skupinou běžně podávaných léků jsou zejména nesteroidní antiflogistika (NSAID), jež však mohou rovněž mít některé známé nežádoucí účinky (zejména gastrointestinální a renální). Dále je běžně užíván paracetamol, a to jak samostatně (infuze či tablety), tak v dnes oblíbených kombinovaných přípravcích s opiody, jako je kodein nebo tramadol (např. Ultracod®, Korylan®, Talvosilen® apod.).10 Dalším účinným opatřením je systémové perioperační podání glukokortikoidů (dexametazon). Četnými studiemi bylo prokázáno, že jejich aplikace snižuje celkovou spotřebu analgetik, přispívá k regulaci pooperační nauzey a vomitu a dále redukuje systémovou pooperační zánětlivou reakci organismu.11 Dále je v rámci protokolu ERAS často zmiňováno užívání gabapentinoidů, spíše však v souvislosti s redukcí potenciálních nežádoucích účinků současně podávaných opiodů.1 Dalším v endoprotetice zkoušeným konceptem je využití pacientem kontrolované analgezie („Patient‑controlled analgesia“, PCA). Výhodou může být redukce celkového množství podaných analgetik a dále možnost aplikace „on‑demand“ – okamžitě, tedy bez čekání na zdravotnický personál. Na druhou stranu se jedná o metodu s četnými nevýhodami, jako je např. selhání aplikačních pump, nároky na intelektuální kapacity konkrétního pacienta apod.10
- Prevence pooperační nauzey a vomitu (PONV)
K rozvoji PONV pacienta predisponuje několik faktorů: 1. ženské pohlaví; 2. nekuřáctví; 3. anamnéza kinetózy; 4. perioperační užití opiátů. Efektivní redukce rozvoje PONV může být potencována podáním kombinace glukokortikoidu (dexametazon) a antagonistů 5‑HT3 serotoninových receptorů (např. ondansetron).12
- Typ anestezie
Podobně jako u multimodální analgezie je i v případě anestezie více základních možností, které potenciálně lze kombinovat. Základními dvěma implementovanými skupinami jsou celková a neuraxiální anestezie. Vzhledem k nutnosti časné vertikalizace pacienta jakožto jednoho ze základních aspektů ERAS nejsou vhodné modality, jež navozují motorickou blokádu po delší časový úsek. Nejsou tedy doporučovány periferní nervové blokády či vysoké dávky pokračující epidurální anestezie.1 Jednou z alternativ je spinální anestezie (SA) v režimu jedné dávky – „one‑shot“ – s intratekálním podáním léků (např. lidokain, bupivakain), jejichž účinnost i s aditivy (např. vazokonstriktory nebo opiody) většinou netrvá déle než cca 12 hodin. Tento aspekt je sice výhodný z hlediska vyloučení přetrvávající motorické blokády, na druhou stranu se po vyprchání účinku mohou u pacientů dostavovat intenzivní bolesti, jež následně rovněž omezují možnosti RHB.10 Dle ERAS navíc není doporučováno rutinní intraspinální podávání vysokých dávek opioidů vzhledem k vysokému podílu nežádoucích účinků.1 Nedostatečně dlouhý analgetický účinek SA lze částečně kompenzovat využitím metod lokální infiltrační anestezie/analgezie (viz níže). Závěrem lze konstatovat, že i přes některé nesporné výhody neuraxiální anestezie (absence pooperační nauzey a vomitu, snížené riziko respiračních, kardiovaskulárních či gastrointestinálních nežádoucích účinků) si celková anestezie zachovává v endoprotetice své místo. Odpadá zde totiž riziko poranění nervových struktur při zavádění epidurálního či spinálního katétru a s tím spojené další komplikace. Navíc nedochází k alteraci motorických funkcí dolních končetin, potenciálně omezující časnost pooperační RHB.13
- Lokální infiltrační analgezie (LIA)
Jak již bylo zmíněno výše, lokální infiltrační analgezii/anestezii lze využívat jako aditivní metodu k celkové a/nebo neuraxiální anestezii.1 LIA je většinou dělena do dvou základních skupin dle aplikace. První metodou je jednorázová periartikulární či intraartikulární aplikace připravené směsi do všech tkání, jež byly vystaveny operačnímu traumatu, typicky na závěr výkonu před zašitím rány. Druhou metodou je intraartikulární zavedení katétru napojeného na dávkovací přístroj s možností kontinuálního dlouhodobého podávání anestetické směsi.14 Hlavní výhodou LIA má být zajištění poměrně vysokého analgetického účinku bez nevýhod motorické blokády. Na druhou stranu však může být dlouhodobé lokální podávání těchto látek do ošetřených tkání spojeno s některými riziky, jako je např. prodloužené hojení rány nebo systémová toxicita lokálních anestetik.15 Toto se však týká dominantně metody kontinuální LIA s využitím katétru. Na našem pracovišti využíváme rovněž metodu topické aplikace periartikulárních tkání směsí mesocainu, bupivakainu, adrenalinu a dexametazonu.
- Prevence hypotermie
Hypotermie v perioperačním období je spojena s četnými riziky, protože dochází k rozvoji stresové reakce s uvolněním vysokého množství kortizolu a katecholaminů. Jejich zvýšené hladiny mohou následně vést k častějšímu rozvoji infekčních či kardiovaskulárních komplikací a k vyšší spotřebě krevních transfuzí a analgetik. Rizika hypotermie mohou navíc být umocněna některými faktory, jako jsou např. již předoperačně snížená teplota pacienta, ženské pohlaví, nízká hodnota BMI nebo starší věk.16 V rámci prevence rozvoje perioperační hypotermie tedy lze provést některá opatření, např. zahřátí a humidifikace anestetických plynů, zahřátí intravenózně podávaných roztoků a také použití speciálních přikrývek s aktivní insuflací teplého vzduchu. Cílené zvyšování průměrné teploty vzduchu na operačním sále na více než 21 oC naopak není vhodné vzhledem k možnému zvýšení rizika infekčních komplikací.1
- Management příjmu tekutin
V rámci technik moderní endoprotetiky již většinou není počítáno s většími krevními ztrátami (> 500 ml), a tedy hypovolemie není častou pooperační komplikací.1 Z těchto důvodů je dle ERAS doporučováno individualizovat příjem tekutin v perioperačním období, vyhnout se jak hyperhydrataci, tak hypohydrataci pacienta vzhledem k přidruženým rizikům (plicní edém, precipitace srdečního selhání, renální selhání apod.). Dalšími cíli jsou pak prevence elektrolytové dysbalance a co nejdřívější navrácení perorálního příjmu tekutin v pooperačním období.16
- Zajištění močových cest
Díky rozvoji technik ortopedické operativy, především rychlosti výkonu, a technik anestezie již nebyl prokázán signifikantní rozdíl ve výskytu pooperační močové retence mezi skupinou pacientů se zavedeným močovým katétrem a skupinou bez něj.17 Na druhou stranu je samozřejmě vždy potřeba důkladně zvážit anamnestické údaje pacienta stran historie např. chronického renálního selhání, močové retence, rizikových kardiovaskulárních chorob apod. U těchto pacientů je pak jistě výhodnější zajistit močovou derivaci kvůli nutnosti přesné monitorace tekutinové bilance. Pokud pacientovi močovou cévku zavedeme, pak bychom ji měli po operaci i časně extrahovat (ideálně do 24 hodin) vzhledem k přidruženým, zejména infekčním rizikům.18 Dle ERAS bychom se při derivaci močových cest měli řídit strategií „catheterize‑when‑needed“, tedy cévkovat pouze dle potřeby, a cíleně pacienta derivovat pouze při překročení ultrazvukem verifikované náplně močového měchýře 800 ml.19 V našich podmínkách zatím není možné u každého pacienta pravidelně ultrasonograficky kontrolovat močové reziduum, avšak postupné snižování procenta cévkovaných pacientů je jedním z našich cílů.
- Antibiotická profylaxe
Podávání antibiotik (ATB) v perioperačním období TEP nemá dle ERAS zcela jasně stanovená kritéria. ATB profylaxe se tedy má primárně řídit pravidly daného zdravotnického zařízení.1 Pravidla, která by se však měla dodržovat univerzálně, zahrnují:
- podání minimálně jedné profylaktické dávky ATB (vzhledem k typickému mikrobiálnímu spektru se jedná většinou o zástupce skupiny cefalosporinů);
- ukončení administrace ATB profylaxe nejpozději do 24 hodin po operaci, pokud není objektivní důvod pro její prodloužení.
Dle posledních doporučení American Academy of Orthopaedic Surgeons (AAOS) je profylaktickým ATB první volby cefalosporin I. generace (např. cefazolin), druhou volbou je pak buď cefalosporin II. generace (např. cefuroxim), nebo glykopeptid (např. vankomycin).20 Častým problémem v managementu ATB je nesprávný čas podání a nedostatečná dávka. Např. u cefazolinu je doporučená doba podání 30–60 minut před incizí kůže, a to v dávce 1 g u pacientů s tělesnou hmotností nižší než 60 kg, 2 g při hmotnosti 60–120 kg a 3 g u jedinců vážících více než 120 kg. Pouze při dodržení těchto zásad můžeme očekávat deklarovanou účinnost podaného ATB.20 Na druhou stranu je důležité brát v potaz stoupající výskyt multirezistentních bakteriálních kmenů a profylaxi včas ukončit.21
Na našem pracovišti se typicky řídíme schématem podání jedné profylaktické dávky ATB před operací, kdy léčivem první volby jsou 2 g cefazolinu, při alergii na penicilinová ATB pak 1,2 g klindamycinu. Pokud nám situace na operačním sále dovolí uzavřít ránu bez zavedení drénu a není objektivní důvod prodloužení terapie (např. obezita v kombinaci s diabetes mellitus, kortikosteroidní léčba, velká krevní ztráta apod.), pak profylaxi touto jednou dávkou ukončujeme. Pokud je zaveden drén, pak prodlužujeme profylaxi do celkově tří dávek ATB (tedy do 24 hodin po operaci).
- Utilizace krevních transfuzí
Pooperační anemizace je stále často vídaným jevem u pacientů po implantaci TEP, přestože, jak bylo řečeno výše, incidence signifikantních ztrát má klesající tendenci. Kauzálně tento stav můžeme vyřešit podáním transfuzních přípravků, což však může být spojeno s výskytem často závažných nežádoucích účinků (např. přenos infekčních chorob, transfuzní reakce apod.). Proto je všeobecně cíleno na minimalizaci množství podaných přípravků na nezbytné minimum. K tomu je možno si pomoci, vedle miniinvazivity výkonu, např. perioperačním podáváním kyseliny tranexamové s antifibrinolytickým efektem (typicky v dávce 1 g při absenci kontraindikací).1
- Chirurgické aspekty
Zejména na poli endoprotetiky kyčelního kloubu lze snížit invazivitu výkonu využitím svaly šetřících operačních přístupů. Zejména neporušení úponů gluteálního svalstva v okolí trochanterického masivu je pro pacienta velmi důležité pro zachování síly operované končetiny při pooperačním nácviku chůze.22 Další nespornou výhodou miniinvazivity je redukce krvácení, a tedy snížení potřeby drénování rány. Zavedením drénů můžeme efektivně redukovat reziduální náplň kloubu pooperačním hematomem, jenž může potenciálně být infekčním fokusem, tzv. surgical site infection (SSI). Dle závěrů Kellyho et al.23 však nebyl tento úzus potvrzen, a nebyl tedy zaznamenán vyšší výskyt SSI u skupiny pacientů po TEP kolene bez zavedeného drénu. Dále může být drénování rizikové stran rozvoje naopak retrográdních infekcí nebo vyšších krevních ztrát a s tím spojené potřeby krevních transfuzí.23 Závěrem je však nutno podotknout, že dle ERAS nelze aktuálně doporučit jeden konkrétní operační přístup, jenž by měl signifikantní vliv na urychlení pooperační RHB.1
Dalším chirurgickým aspektem je rovněž délka operačního výkonu, neboť bylo prokázáno, že operační čas u implantace totální endoprotézy kyčelního kloubu přesahující 90 minut je spojen se signifikantně vyšším rizikem infekčních komplikací a readmise pacienta.24
- Příjem per os po operaci
Prozatím nebyla provedena studie, která by direktivně hodnotila vztah mezi časným obnovením perorální nutrice a rychlostí rekonvalescence pacienta. Nicméně brzký návrat pacienta k normálnímu stravování může mít důležitý vliv na adaptaci pacienta na běžný domácí režim.1 Zásadním rizikem je tedy hlavně již předoperační malnutrice a s ní spojená hypoalbuminemie, jež může zvyšovat podíl pooperačních komplikací (zejména alterace hojení rány, infekční komplikace apod.).25
- Prevence tromboembolické nemoci (TEN)
Dle doporučení American College of Chest Physicians z roku 2012, potažmo doporučení National Institute of Health Care and Excellence z roku 2016 by standardizovanou dobou podávání antikoagulačních léčiv (zejména nízkomolekulární heparin, fondaparinux, dabigatran etexilát či xabany) mělo být minimálně 10–14 dní po implantaci TEP kyčelního a kolenního kloubu s následným vhodným prodloužením na 28–35 dní po implantaci TEP kyčle.26,27 Jedná se však o doporučení, která byla vytvořena ze studií bez rutinní implementace principů ERAS časné rekonvalescence pacienta. Již existují studie, jež popisují i možnost podávání tromboprofylaxe pouze po dobu hospitalizace pacienta, pokud tento jedinec stráví v nemocnici kratší dobu než pět dní. Tento závěr tedy předpokládá časnou vertikalizaci pacienta, která zajistí dostatečnou mechanickou prevenci trombózy a zároveň absenci trombofilních rizikových faktorů.28 Tento postup krátké tromboprofylaxe však zatím není integrální komponentou ERAS a budou potřeba další studie k jeho optimalizaci.1
Na našem pracovišti se řídíme schématem první profylaktická dávka nízkomolekulárního heparinu (0,4 ml enoxaparinu denně) před výkonem a poté většinou jedna až dvě dávky (dle doby ponechání epidurálního katétru) po operaci. Následně pacienta převádíme na podávání 10 mg rivaroxabanu denně po dobu 14 dní po TEP kolene a 35 dní po TEP kyčle. Pokud pacient již užívá svou chronickou antikoagulaci nebo má anamnézu krvácivých či trombofilních stavů, pak tromboprofylaxi individuálně upravujeme.
- Časná mobilizace/rehabilitace + aktualizace režimových opatření
Jednou z důležitých zásad protokolu ERAS je časná mobilizace pacienta, optimálně již v den operace. Hlavní výhodou brzké RHB je její signifikantní vliv na snížení výskytu svalové atrofie pacientů a redukce přidružených komplikací (tromboembolická nemoc, plicní a infekční komplikace). Navíc lze tímto způsobem zkrátit průměrnou dobu hospitalizace o 1,8 dne.29 Dalším aspektem časné vertikalizace je i povolení plného zatěžování operované končetiny jak po TEP kolene, tak po TEP kyčle ihned po operaci, protože při tomto režimu nebylo prokázáno zvýšené riziko periprotetických komplikací. Francouzské hole, které pacienti používají, tedy mají sloužit pouze jako jistící opora zabraňující pádu, nikoliv jako element umožňující plné odlehčení operované končetiny.1,29 Stejně tak je stále častěji referována benevolence v režimových opatřeních zejména po implantaci TEP kyčle, kdy dříve zavedená pravidla o maximální flexi 90 stupňů v kyčelním kloubu, zákazu addukce nebo excesivních rotací již neplatí pro všechny pacienty.30 Důležitým faktorem je vždy identifikace individuálních rizik konkrétního pacienta (např. těžká obezita, snížená compliance, preemptivní poruchy chůze při neurologických diagnózách, případně nejistota absolutní stability implantátu při výkonu apod.). Pokud jsou taková rizika přítomna, pak je nadále vhodné antiluxační opatření implementovat, pokud ne, pak můžeme dovolit pacientovi více.1,30
- Dimise/plánování další péče
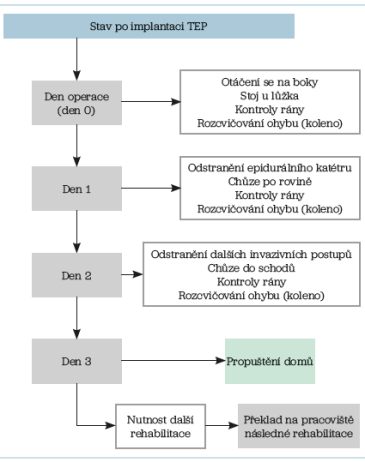 Implementací zásad ERAS se i našem pracovišti podařilo poměrně efektivně zkrátit průměrnou dobu hospitalizace. Z dříve běžných 10–14 dní jsme se nyní u nekomplikovaných a motivovaných pacientů dostali na 3–4 dny. Pokud pacient do této doby nezvládne rehabilitační program nebo není v dostatečně kompenzovaném zdravotním stavu, pak je naplánován překlad na pracoviště následné rehabilitace. Našimi požadavky je zvládnutí samostatné chůze po rovině a do schodů, manipulace při pohybu v lůžku, u TEP kolene pak ohyb v operovaném kloubu minimálně 90o. Pokud je pacient po třech dnech plně soběstačný a nejsou u něj přítomny jiné komplikace, pak je pro něj nejlepší volbou přímá dimise do domácího prostředí (obr. 2). Při správně nastavených a zejména všemi dodržených pravidlech ERAS je však možnost dimise pacienta již v den operace. Tito jedinci však musejí spolehlivě zvládnout samostatnou chůzi po rovině i schodech bez projevů nadměrné slabosti či bolestí, nesmějí vykazovat celkové nebo lokální komplikace a je vhodné mít alespoň na 24 hodin zajištěné nelimitující prostředí pobytu a osobu blízkou k zajištění základních potřeb.31
Implementací zásad ERAS se i našem pracovišti podařilo poměrně efektivně zkrátit průměrnou dobu hospitalizace. Z dříve běžných 10–14 dní jsme se nyní u nekomplikovaných a motivovaných pacientů dostali na 3–4 dny. Pokud pacient do této doby nezvládne rehabilitační program nebo není v dostatečně kompenzovaném zdravotním stavu, pak je naplánován překlad na pracoviště následné rehabilitace. Našimi požadavky je zvládnutí samostatné chůze po rovině a do schodů, manipulace při pohybu v lůžku, u TEP kolene pak ohyb v operovaném kloubu minimálně 90o. Pokud je pacient po třech dnech plně soběstačný a nejsou u něj přítomny jiné komplikace, pak je pro něj nejlepší volbou přímá dimise do domácího prostředí (obr. 2). Při správně nastavených a zejména všemi dodržených pravidlech ERAS je však možnost dimise pacienta již v den operace. Tito jedinci však musejí spolehlivě zvládnout samostatnou chůzi po rovině i schodech bez projevů nadměrné slabosti či bolestí, nesmějí vykazovat celkové nebo lokální komplikace a je vhodné mít alespoň na 24 hodin zajištěné nelimitující prostředí pobytu a osobu blízkou k zajištění základních potřeb.31
Závěr
Kontinuální snaha o optimalizaci péče v kloubní endoprotetice je jistě velmi důležitou a aktuální problematikou v ortopedii. Na jednotlivá pracoviště budou kladeny vysoké nároky vzhledem k narůstajícímu množství pacientů, což s sebou přináší nutnost zásadních modifikací koncepce celého perioperačního procesu kloubních náhrad. Naše dosavadní zkušenosti s postupy ERAS ukazují, že problém nespočívá ani tak v technice operativy nebo zajištění špičkové perioperační péče, ale že hlavní překážkou je prozatímní nepřipravenost tuzemské společnosti na tak rychlý průběh hospitalizace. Věříme, že důkladnou a opakovanou edukací pacientů, a to i v kvalitní spolupráci s praktickými lékaři, budeme schopni i tento aspekt efektivně řešit.
MUDr. Jan Černý / MUDr. Tomáš Novotný, Ph.D., MBA
Ortopedická klinika Fakulty zdravotnických studiíUniverzity J. E. Purkyně v Ústí nad Labema Krajské zdravotní, a.s. – Masarykovy nemocnicev Ústí nad Labem, o.z.
Korespondenční adresa: tomas.novotny@kzcr.eu
Literatura
- Wainwright TW, Gill M, McDonald DA, et al. Consensus statement for perioperative care in total hip replacement and total knee replacement surgery: Enhanced Recovery After Surgery (ERAS®) Society recommendations. Acta Orthop 2020;91:3–19. doi:10.1080/17453674.2019.1683790
- Pelt CE, Gililland JM, Erickson JA, et al. Improving Value in Total Joint Arthroplasty: A Comprehensive Patient Education and Management Program Decreases Discharge to Post‑Acute Care Facilities and Post‑Operative Complications. J Arthroplasty 2018;33:14–18. doi:10.1016/j.arth.2017.08.003
- Koivisto JM, Saarinen I, Kaipia A, et al. Patient education in relation to informational needs and postoperative complications in surgical patients. Int J Qual Health Care 2020;32:35–40. doi:10.1093/intqhc/mzz032
- Pierre S, Rivera C, Le Maître B, et al. Guidelines on smoking management during the perioperative period. Anaesth Crit Care Pain Med 2017;36:195–200. doi:10.1016/j.accpm.2017.02.002
- Eliasen M, Grønkjær M, Skov‑Ettrup LS, et al. Preoperative alcohol consumption and postoperative complications: a systematic review and meta‑analysis. Ann Surg 2013;258:930–942. doi:10.1097/SLA.0b013e3182988d59
- Tabatabai S, Do Q, Min J, et al. Obesity and perioperative outcomes in older surgical patients undergoing elective spine and major arthroplasty surgery. J Clin Anesth 2021;75:110475. doi:10.1016/j.jclinane.2021.110475
- Gu A, Malahias MA, Strigelli V, et al. Preoperative Malnutrition Negatively Correlates With Postoperative Wound Complications and Infection After Total Joint Arthroplasty: A Systematic Review and Meta‑Analysis. J Arthroplasty 2019;34:1013–1024. doi:10.1016/j.arth.2019.01.005
- Smith I, Kranke P, Murat I, et al. Perioperative fasting in adults and children: guidelines from the European Society of Anaesthesiology. Eur J Anaesthesiol 2011;28:556–569. doi:10.1097/EJA.0b013e3283495ba1
- Pitchon DN, Dayan AC, Schwenk ES, et al. Updates on Multimodal Analgesia for Orthopedic Surgery. Anesthesiol Clin 2018;36:361–373. doi:10.1016/j.anclin.2018.05.001
- Halawi MJ, Grant SA, Bolognesi MP. Multimodal Analgesia for Total Joint Arthroplasty. Orthopedics 2015;38:e616–e625. doi:10.3928/01477447‑20150701‑61
- Ruberto RA, Farah O, Lopez C, Hickernell T. Perioperative Intravenous Glucocorticoids in Total Joint Arthroplasty: A Systematic Review. J Am Acad Orthop Surg 2023;31:e94–e106. doi:10.5435/JAAOS‑D‑22‑00232
- Koh IJ, Chang CB, Lee JH, et al. Preemptive low‑dose dexamethasone reduces postoperative emesis and pain after TKA: a randomized controlled study. Clin Orthop Relat Res 2013;471:3010–3020. doi:10.1007/s11999‑013‑3032‑5
- Aasvang EK, Luna IE, Kehlet H. Challenges in postdischarge function and recovery: the case of fast‑track hip and knee arthroplasty. Br J Anaesth 2015;115:861–866. doi: 10.1093/bja/aev257
- Perret M, Fletcher P, Firth L, Yates P. Comparison of patient outcomes in periarticular and intraarticular local anaesthetic infiltration techniques in total knee arthroplasty. J Orthop Surg Res 2015;10:119. Published 2015 Jul 31. doi:10.1186/s13018‑015‑0249‑x
- Seangleulur A, Vanasbodeekul P, Prapaitrakool S, et al. The efficacy of local infiltration analgesia in the early postoperative period after total knee arthroplasty: A systematic review and meta‑analysis. Eur J Anaesthesiol 2016;33:816–831. doi:10.1097/EJA.0000000000000516
- Soffin EM, YaDeau JT. Enhanced recovery after surgery for primary hip and knee arthroplasty: a review of the evidence. Br J Anaesth 2016;117(suppl 3):iii62–iii72. doi:10.1093/bja/aew362
- Huang Z, Ma J, Shen B, Pei F. General anesthesia: to catheterize or not? A prospective randomized controlled study of patients undergoing total knee arthroplasty. J Arthroplasty 2015;30:502–506. doi:10.1016/j.arth.2014.09.028
- Bjerregaard LS, Homilius M, Bagi P, et al. Indwelling urinary catheterisation may increase risk of complications in hip and knee arthroplasty. Dan Med J 2019;66:A5538.
- Bjerregaard LS, Hornum U, Troldborg C, et al. Postoperative urinary catheterization thresholds of 500 versus 800 ml after fast‑track total hip and knee arthroplasty: a randomized, open‑label, controlled trial. Anesthesiology 2016a;124:1256–1264. doi: 10.1097/ ALN.0000000000001112
- American Academy of Orthopaedic Surgeons Diagnosis and Prevention of Periprosthetic Joint Infections Evidence‑Based Clinical Practice Guideline. https://www.aaos.org/globalassets/quality‑and‑practice‑resources/pji/pji‑clinical‑practice‑guideline‑final‑9‑18‑19‑.pdf [accessed 05.12.21].
- Rondon AJ, Kheir MM, Tan T L, et al. Cefazolin Prophylaxis for Total Joint Arthroplasty: Obese Patients Are Frequently Underdosed and at Increased Risk of Periprosthetic Joint Infection. Arthroplasty 2018. doi:10.1016/j.arth.2018.06.037
- Vučković M, Ružić L, Tudor A, Šutić I. Difference in patient quality of life after hip arthroplasty with a minimally invasive approach or classic approach. Acta Clin Croat 2021;60:89–95. doi:10.20471/acc.2021.60.01.13
- Kelly EG, Cashman JP, Imran FH, et al. Systematic review and meta‑analysis of closed suction drainage versus non‑drainage in primary hip arthroplasty. Surg Technol Int 2014;24:295–301.
- Nowak LL, Schemitsch EH. Duration of surgery affects the risk of complications following total hip arthroplasty. Bone Joint J 2019;101‑B(6_Supple_B):51–56. doi:10.1302/0301‑620x.101b6.bjj‑2018‑1400.r1
- Nanri Y, Shibuya M, Fukushima K, et al. Preoperative malnutrition is a risk factor for delayed recovery of mobilization after total hip arthroplasty. PM R 2021;13:1331–1339. doi:10.1002/pmrj.12570
- Falck‑Ytter Y, Francis CW, Johanson NA, et al. Prevention of VTE in orthopedic surgery patients. Antithrombotic therapy and prevention of thrombosis, 9th ed. American College of Chest Physicians Evidence‑Based Clinical Practice Guidelines. Chest 2012;141(2 Suppl.):e278S‑e325S. doi: 10.1378/chest.11‑2404.
- National Guideline Centre (UK). Venous thromboembolism in over 16s: Reducing the risk of hospital‑acquired deep vein thrombosis or pulmonary embolism. London: National Institute for Health and Care Excellence (NICE); March 2018.
- Petersen PB, Kehlet H, Jorgensen CC, Lundbeck Foundation Centre for Fasttrack H, Knee Replacement Collaborative G. Safety of in‑hospital only thromboprophylaxis after fast‑track total hip and knee arthroplasty: a prospective follow‑up study in 17,582 procedures. Thromb Haemost 2018a;118:2152–2161. doi: 10.1055/s‑0038‑1675641
- Guerra ML, Singh PJ, Taylor NF. Early mobilization of patients who have had a hip or knee joint replacement reduces length of stay in hospital: a systematic review. Clin Rehabil 2015;29:844–854. doi:10.1177/0269215514558641
- Rowan FE, Benjamin B, Pietrak JR, Haddad FS. Prevention of Dislocation After Total Hip Arthroplasty. J Arthroplasty 2018;33:1316–1324. doi:10.1016/j.arth.2018.01.047
- Gromov K, Kjærsgaard‑Andersen P, Revald P, et al. Feasibility of outpatient total hip and knee arthroplasty in unselected patients. Acta Orthopaedica 2017;88:516–521. doi:10.1080/17453674.2017.1314158