Jak se neztratit v diferenciální diagnostice anémie

Základní diferenciální diagnostika anémií vychází z běžné anamnézy, klinického vyšetření a několika laboratorních parametrů. Následující text na toto téma je určen zejména praktickým lékařům a lékařům interních oborů. Větší pozornost je soustředěna na sideropenickou anémii.
Anémie je stav charakterizovaný poklesem koncentrace hemoglobinu (Hb), ev. hematokritu pod fyziologickou mez. U dospělých mužů je patologická koncentrace Hb pod 135 g/l, u žen pod 120 g/l. To vede k omezení transportní kapacity krve pro kyslík a v případě těžké anémie až ke tkáňové hypoxii.
V rozvojových zemích jsou nejčastější příčinou anémie nedostatek železa v potravě a parazitární infekce, ve vysokopříjmových zemích (včetně České republiky) se častěji jedná o anémii chronických chorob provázející celou řadu jiných diagnóz (střevní zánětlivá onemocnění, renální insuficienci, chronické kardiální selhání, nádorová onemocnění). Fyziologický pokles hemoglobinu (Hb) daný hemodilucí vídáme u gravidních žen, hemoglobin by ale neměl klesat pod 105 g/l.
Vstupní základ diagnostiky se obvykle odehrává v ambulanci praktického lékaře. Pacienta k němu přivedou buď potíže spojené s anemickým syndromem (dušnost, slabost, únava, tachykardie), nebo se jedná o náhodný nález např. v rámci preventivní prohlídky či předoperačního vyšetření. Je zapotřebí od nemocného získat podrobné údaje z osobní anamnézy (ostatní chronická onemocnění, prodělané operace, farmakoterapie). Zjišťujeme, jak rychle vznikly symptomy anemického syndromu, zda jsou přítomny celkové příznaky (horečka, hubnutí, pocení), patologická barva stolice/příměs krve ve stolici.
Při vyšetřování anémií primárně posuzujeme střední objem erytrocytů (MCV). Podle něj anémie dělíme na mikrocytární (MCV < 80 fl, obvykle provázané sníženou koncentrací MCH), normocytární (MCV 80–100 fl) a makrocytární (MCV > 100 fl). Dále zohledňujeme koncentraci retikulocytů. Retikulocyty jsou nezralé červené krvinky obsahující zbytky RNA. Jejich zvýšená koncentrace svědčí pro zachovanou proliferační činnost kostní dřeně. Setkáváme se s ní u hemolytických anémií. Naopak u primárního postižení kostní dřeně je koncentrace retikulocytů snížená.
Mikrocytární anémie (se sníženým MCV erytrocytů)
Nejčastější příčinou mikrocytární anémie (i anémií obecně) je sideropenická anémie. Erytrocyty jsou zároveň hypochromní (pokles střední koncentrace hemoglobinu v erytrocytech [MCHC]). Při vyšetření metabolismu železa (Fe) posuzujeme koncentraci železa v séru, saturaci transferinu, koncentraci feritinu. Citlivým parametrem sideropenie jsou solubilní transferinové receptory, při nedostatku Fe jsou spolehlivě zvýšeny. Koncentrace feritinu je ovlivněna celou řadou faktorů, protože patří mezi bílkoviny akutní fáze. Je proto zvýšená při zánětlivém, infekčním nebo nádorovém onemocnění.
Příčiny sideropenie
Nedostatek železa v organismu (sideropenie) může být způsoben jeho sníženou resorpcí, zvýšenými ztrátami anebo fyziologicky zvýšeným výdejem (těhotenství, kojení) (viz tabulku). U žen je proto při vyšetřování příčin anémie samozřejmostí doplnění gynekologického vyšetření.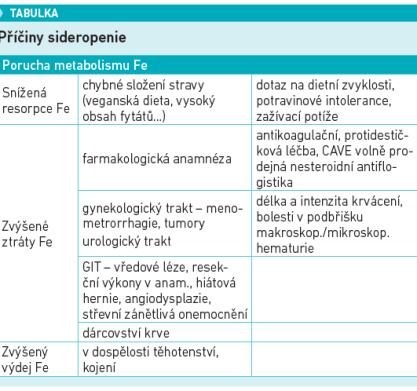
Neinvazivním způsobem vyloučení krevních ztrát do GIT je vyšetření okultního krvácení. Imunochemické stanovení lidského hemoglobinu slouží k detekci krvácení do distálních partií GIT. Není zatíženo interferencí s potravou a léky. Jeho senzitivita pro detekci kolorektálních tumorů je 75 procent, specificita 95 procent. Větší výpovědní hodnotu má endoskopické vyšetření GIT. U mužů a postmenopauzálních žen nebo mladších žen s gastrointestinálními potížemi je jednoznačně preferujeme. Standardně indikujeme ezofagogastroduodenoskopii (EGDS) a kolonoskopii. EGDS je důležitá i pro diagnostiku celiakie. Při negativitě výsledků je vhodné doplnit kapslovou enteroskopii, ev. CT enteroklýzu. V případě, že se zdroj krvácení neprokáže a anémie/sideropenie recidivuje, je třeba vyšetření po čase zopakovat, aktivně pátrat po tom, zda např. kolonoskopie byla provedena v plném rozsahu.
Při záchytu mikrocytární anémie bez sideropenie pomýšlíme na některou z forem hemoglobinopatií – nejčastěji se setkáváme s talasémií, jejíž diagnostiku dokončí specializované hematologické pracoviště.
Léčba sideropenické anémie
Denně se z potravy v lidském organismu vstřebá 1–2 mg železa, což zhruba pokryje přirozené ztráty způsobené deskvamací kožních buněk a epitelových buněk sliznic ve střevě. U žen je třeba počítat se ztrátami Fe během menstruace (fyziologicky 40–60 ml krve/cyklus = 16–25 mg Fe). Pokud ztráty Fe převýší jeho příjem, v organismu se rozvíjí sideropenie.
V léčbě primárně volíme substituci železa perorální formou. Železo je v ní přítomno ve formě dvojmocných nebo trojmocných solí. Pro dostatečně razantní substituční léčbu podáváme 180–200 mg železa denně (raději rozdělené do dvou denních dávek). Z tohoto množství se vstřebá pouze 50–60 mg/den. V ideálním případě pak pacient zareaguje vzestupem hemoglobinu o 2 g denně. Perorální léčba železem bývá často komplikována gastrointestinálními potížemi (častěji u přípravků s železnatou solí, tj. dvojmocné železo). V ambulantní praxi máme dobrou zkušenost s přípravkem s trojmocným železem s polymaltózou ve formě kapek, sirupu nebo žvýkacích tablet, který je pacienty dobře tolerován. Resorpci železa usnadní přítomnost aminokyselin a kyseliny askorbové a citronové v potravě. Naopak fosfáty, fytáty a oxaláty resorpci inhibují. Při substituční léčbě Fe zohledňujeme možné lékové interakce, především u přípravků s dvojmocným železem – pokles resorpce Fe při užívání inhibitorů protonové pumpy nebo snížené vstřebávání hormonů štítné žlázy.
Resorpční test absorpce Fe se vzhledem k zažívacím potížím pacientů po velké jednorázové dávce Fe provádí jen velmi vzácně. Pokud pacient netoleruje perorální léčbu nebo železo nevstřebává, je indikována intravenózní aplikace. Současné moderní nitrožilní železo je bezpečné a aplikace není spojena s vysokým rizikem alergických reakcí. Nejčastěji užívanými přípravky jsou glukonát sodno‑železitý (v jedné dávce je 62,5 mg, je třeba opakovaných podání) a železitá sůl karboxymaltózy (FCM, v jedné dávce 500 mg Fe). Výhodou přípravku FCM (Ferinject) je rychlý nástup účinku a možnost podat až 1 000 mg při jedné aplikaci a současně dlouhodobější efekt. Přípravek má plnou úhradu ze zdravotního pojištění u jasně definované skupiny pacientů s chronickým srdečním selháním.
Normocytární anémie
Při normálním MCV erytrocytů se může jednat o primárně hematologické onemocnění. Pro hematologické onemocnění (zejména akutní formu) svědčí leukocytóza nebo leukopenie, patologický diferenciální rozpočet leukocytů – přítomnost blastů nebo atypických buněk v periferní krvi, trombocytopenie. V této situaci je nutné co nejdříve doplnit diagnostiku, proto musí být pacient odeslán na hematologické pracoviště. Varovnou známkou je u anémií také vysoká koncentrace celkové bílkoviny a známky renální insuficience, ev. hyperkalcémie. V tomto případě se pravděpodobně jedná o mnohočetný myelom, který patří mezi nejčastější hematologická maligní onemocnění. K základnímu biochemickému vyšetření patří zhodnocení celkové bílkoviny, elektroforetické vyšetření séra (ideálně s imunofixací a volnými lehkými řetezci).
Často se setkáváme s anémií chronických chorob (ACHN). Tento stav provázejí např. chronické autoimunitní zánětlivé diagnózy, chronická infekční nebo onkologická onemocnění. V organismu dochází ke zvýšené produkci některých cytokinů (IL‑6, TNFα, IFNγ), následně je v játrech zvyšována tvorba regulační látky hepcidinu. Hepcidin pak ovlivňuje metabolismus Fe – vázne jeho resorpce ve střevě a zároveň je zadržováno v monocyto‑makrofágovém systému v játrech a v kostní dřeni. Železo, přestože je v organismu přítomno, není dostupné pro erytropoezu. Zároveň nadprodukce cytokinů způsobuje sníženou citlivost kostní dřeně k regulačnímu působení erytropoetinu. Anémie je obvykle normocytární normochromní, v metabolismu železa vidíme normální nebo zvýšenou koncentraci feritinu. Pokud se nepodaří ovlivnit základní onemocnění, je léčba často svízelná.
Další velkou skupinu představují hemolytické anémie. Pro ty je charakteristický zvýšený počet retikulocytů v periferní krvi, MCV je v normě nebo lehce zvýšený. Jedná se o skupinu anémií, u kterých je životnost erytrocytů zkrácena. Dochází k rozpadu erytrocytů (extravaskulárně v monocyto‑makrofágovém systému jater a sleziny a/nebo intravaskulárně). Koncentrace retikulocytů odpovídá stimulované erytropoeze ve funkční kostní dřeni. Pacienti přicházejí se známkami anemického syndromu, při fyzikálním vyšetření současně zjišťujeme ikterické zbarvení kůže a sklér. V séru je přítomna zvýšená koncentrace bilirubinu a laktátdehydrogenázy (LD). Nejčastější příčina hemolýzy je autoimunitní. Hemolýzu z mechanických příčin vídáme vzácně, např. u dysfunkčních chlopenních náhrad (vlivem abnormálního toku krve). V případě, že je v krevním obraze zároveň trombocytopenie a navíc jsou v mikroskopickém nátěru popsány fragmenty erytrocytů (tzv. schistocyty), je třeba myslet na možnost vzácné mikroangiopatické hemolytické anémie – trombotické trombocytopenické purpury. Jedná se o život ohrožující stav vyžadující urgentní řešení a další dovyšetření. Proto je nutné pacienta po předchozí konzultaci odeslat na hematologické, ev. interní pracoviště.
Vrozené (primární) hemolytické anémie jsou obvykle diagnostikovány v dětském věku. Podrobnější informace jsou nad rámec tohoto článku.
Makrocytární anémie
Při deficitu vitaminu B12 a kyseliny listové je erytropoeza v kostní dřeni neefektivní v důsledku poruchy syntézy DNA. Koncentrace retikulocytů je proto snížená. V krevním obraze je obvykle přítomna leukopenie a trombocytopenie, vídáme lehké známky hemolýzy (zvýšený konjugovaný bilirubin a LD). Při nedostatku vitaminu B12 je vhodné provést EGDS. Obvyklým nálezem je obraz atrofické gastritidy s achlorhydrií. V séru je možné detekovat protilátky proti parietálním buňkám. Po stanovení diagnózy zahajujeme substituci vitaminu B12 intramuskulárně, sledujeme odezvu v krevním obraze (očekáváme vzestup koncentrace retikulocytů během 7–10 dní). V případech, kdy je resorpce alespoň částečně zachována, lze k dlouhodobé substituci použít perorální vysoce dávkovaný vitamin B12 (1 000 µg denně). Je dobré myslet na to, že překotná krvetvorba může vést k přechodnému nedostatku Fe. Proto bychom měli za jeden až dva měsíce od léčby vitaminem B12 zkontrolovat parametry metabolismu Fe.
Nedostatek kyseliny listové rovněž vede k makrocytární anémii. Vídáme ho u pacientů se špatným složením potravy (např. anorexie, alkoholismus) nebo při poruše resorpce (celiakie, zánětlivá střevní onemocnění).
Transfuzní léčba
Podání transfuzí patří do léčby těžkých anémií s manifestními projevy anemického syndromu. U pacientů s kardiorespiračními chorobami mohou být indikovány již při koncentraci Hb kolem 90 g/l. Jinak zdravý jedinec obvykle toleruje koncentrace Hb kolem 70 g/l. Závažná anémie vyžaduje rychlé dovyšetření příčiny. V případě akutní krevní ztráty (u netraumatických příčin, např. při krvácení z jícnových varixů) zůstává hodnota hemoglobinu zpočátku stabilní, protože pacient ztrácí plnou krev se všemi složkami.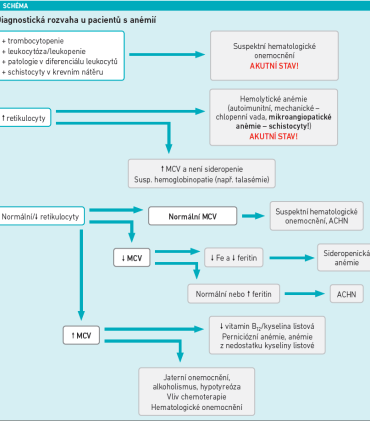
Kazuistika
Muž ve věku 55 let byl praktickým lékařem objednán k hematologickému vyšetření pro těžkou mikrocytární hypochromní anémii (z donesených výsledků v listopadu 2022: hemoglobin vstupně 72 g/l, MCV 63,5 fl, leukocyty a trombocyty v normě, v biochemických testech jednoznačně těžká sideropenie). Měl provedena endoskopická vyšetření GIT. EGDS s normálním nálezem (z r. 2020), bezprostředně před návštěvou v naší ambulanci absolvoval kolonoskopii (zde pouze sporadicky krvácející vnitřní hemoroidy).
Při odebírání osobní anamnézy pacient uvedl tato chronická onemocnění: diabetes mellitus 2. typu na kombinované léčbě perorálními antidiabetiky a inzulin, asthma bronchiale, arteriální hypertenze, jaterní steatóza, obezita a polyvalentní léková alergie. V minulosti užíval perorální přípravek s Fe, ten ovšem netoleroval pro úpornou zácpu.
První vyšetření u nás proběhlo koncem prosince 2022, Hb byl 62 g/l, MCV 62 fl, leukocyty a trombocyty v normě. Subjektivně si pacient stěžoval na velkou únavu a námahovou dušnost, hubnutí (6 kg za 6 měsíců, zde zvažován efekt perorální antidiabetické léčby empagliflozinem a metforminem). Fyzikální nález byl kromě bledé barvy kůže a sliznic bez patologie.
Vstupně byly podány dvě transfuzní jednotky erytrocytární resuspenze. Dále již při první návštěvě bylo intravenózně podáno železo (FCM v dávce 500 mg). Považovali jsme za nutné provést kontrolní EGDS, kde byly popsány drobné angiodysplazie duodena.
Na další kontrolu přišel pacient se zpožděním až v únoru 2023, protože se léčil pro akutní tonzilitidu. Při této návštěvě byl Hb 76 g/l, parametry metabolismu Fe byly rovněž velmi snížené – feritin 6,9 µg/l (norma 20–510 µg/l). U pacienta bylo nutné dovyšetřit zažívací trakt, zejm. oblast tenkého střeva. Vzhledem k udávané alergii na jódovou kontrastní látku byla provedena MR enteroklýza (březen 2023) po premedikaci kortikoidy a dále kapslová enteroskopie (duben 2023). Výsledkem vyšetření byl tumor stenozující orální jejunum s metastatickým postižením peritonea. V květnu 2023 pacient podstoupil gastroeneteroanastomózu, z odebraného materiálu byla stanovena diagnóza dobře diferencovaného adenokarcinomu jejuna. Od června 2023 je pacient léčen kombinací klasické chemoterapie a biologické léčby. Onemocnění je stabilizované, pacient má dosud slušnou kvalitu života.
Z tohoto případu vyplývá, že pokud nález z EGDS a kolonoskopického vyšetření nevysvětluje recidivující sideropenickou anémii, je třeba doplnit další vyšetření k vyloučení krevních ztrát z GIT. V případě, že tato vyšetření nejsou indikována, může být pacient ohrožen nediagnostikovaným maligním onemocněním.