Nová možnost léčby srdečního selhání pro pacienty po dekompenzaci
Na nedávném XXX. výročním sjezdu České kardiologické společnosti zaznělo 9. května také sympozium podpořené společností Bayer, které se jako jedno z prvních zabývalo novou možností léčby srdečního selhání pro pacienty po dekompenzaci.
Dnes již není snadné rozdělit pacienty na ty, kteří mají a kteří nemají chronické srdeční selhání (CHSS). Pacient s CHSS je charakterizován symptomy, známkami tohoto onemocnění (dušnost, otoky, únava či nevýkonnost) a strukturálním poškozením srdce. „Čím více je abnormalit konzistentních s diastolickou dysfunkcí plnicích tlaků LK, včetně zvýšení koncentrace natriuretických peptidů (NP), tím pravděpodobnější je diagnóza srdečního selhání. Optimálně léčený pacient s CHSS může být ale asymptomatický, včetně nízké koncentrace NP,“ uvedl prof. MUDr. Mgr. Jiří Pařenica, Ph.D., z Interní kardiologické kliniky FN Brno.
Ani získání dat o prevalenci a incidenci srdečního selhání není jednoduché. Podle dat publikovaných v r. 2018 v Lancetu prevalence pacientů s CHSS stále narůstá, ve Velké Británii dosahovala v roce 2014 cca 1,4 procenta populace. Údaje publikované v roce 2020 (NHANES) získané na základě dotazníkové metody ukazují, že v roce 2016 byla prevalence CHSS v USA 2,2 procenta populace. V ČR dosahovala v roce 2018 prevalence 2,69 procenta (celkem 285 745 pacientů), zatímco v roce 2012 to bylo 1,68 procenta (Táborský et al., ESC Heart Failure 2021). Jak ale prof. Pařenica vysvětlil, při uplatnění širší identifikace pacientů s CHSS se prevalence dostává až nad tři procenta, což považuje za reálné číslo. „Ukazuje se, že od roku 2012 postupně přibývá pacientů s CHSS. Je zřejmé, že jejich počet výrazně narůstá s věkem a se stárnutím populace. Průměrný věk pacientů s CHSS je kolem 74 let, přičemž u mužů je to v průměru o sedm let méně,“ doplnil.
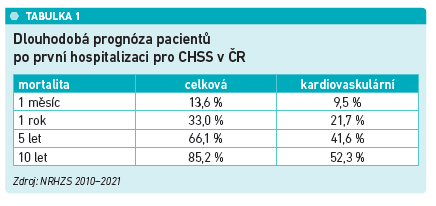
Incidence pacientů s hlavní dg. srdečního selhání je v posledních deseti letech stabilní, kolem 35 000, hospitalizací je ale daleko více (až 60 000), což je dáno častou rehospitalizací. Přitom právě hospitalizace je značně riziková (viz tabulku). „Hospitalizace pro CHSS výrazně zhoršuje prognózu a pro pacienty je výrazně traumatizující. Zatímco po infarktu myokardu se do kardiocentra nemocný stále dostává po více než třech hodinách, u CHSS je to cca 2,5 hodiny, což dokazuje, že jde o onemocnění silně symptomatické,“ vysvětlil prof. Pařenica.
Rozdělíme‑li pacienty podle EF, je prognóza víceméně stejná. Třetina pacientů po dvou letech přežívá a zůstane bez hospitalizace, třetina pacientů, část bez hospitalizace, v tomto období zemře. Znamená to, že dg. srdečního selhání, bez ohledu na EF, je závažná. Pacienti s HFrEF tvoří 42,3 procenta, pacienti s HFmEF 14,3 procenta a nemocní s HFpEF 43,4 procenta. Nemocných s pokročilým CHSS, kde i přes léčbu dochází k opakovaným hospitalizacím, je deset až čtrnáct procent, tedy cca 0,2 procenta populace. Řada nemocných má ale spolu s CHSS i několik komorbidit, např. hypertenzi (92 %), fibrilaci síní (49 %), DM (41 %), CHOPN, chlopenní vady, malignity, CMP, demenci/Alzheimerovu nemoc nebo IM. Podle prof. Pařenici postupně ubývá pacientů s jednou, dvěma nebo třemi komorbiditami a narůstá počet pacientů s pěti, šesti a více komorbiditami. Právě další souběžná onemocnění přitom mají výrazný vliv na prognózu pacientů. Jak ukazují data z registru AHEAD (n = 5 846), při hodnocení parametrů věk nad 70 let, kreatinin nad 130 µmol/l, anémie, DM a fibrilace síní zvyšuje každý jeden bod roční mortalitu o 10 procent.
Při pohledu na medikaci předepsanou do šesti měsíců od zahájení hospitalizace pro CHSS stojí na předních místech kličkové diuretikum furosemid (73 %), betablokátory (63 %), ACEI/AT2 (60 %), inhibitory kalciového kanálu, digoxin, jiná diuretika a ARNI. Nicméně jsou pacienti, kteří tyto léky netolerují.
Jak prof. Pařenica upozornil, pokud jde o prognózu, velice důležitá je tzv. vulnerabilní fáze po propuštění nemocného z hospitalizace, kdy jsou pacienti nejvíce ohroženi úmrtím nebo recidivou. Nejčastější příčinou rehospitalizace je nedostatečná dekongesce (20 %), ischémie, fibrilace síní, infekce a další komorbidity, ale častá je i non‑compliance, alkohol a nemožnost kontroly po propuštění. Ke snížení rizika je potřebné zavedení/uptitrace léčby ACEI/ARB, BB, MRA, ARNI. Navíc dnes již existují důkazy o prospěšnosti včasného nasazení inhibitoru SGLT‑2 nebo vericiguatu již za hospitalizace.
„Prevalence srdečního selhání se pohybuje mezi dvěma a třemi procenty, což v ČR představuje na 330 000 pacientů, kdy dochází k 40 000–45 000 hospitalizací s hlavní diagnózou srdečního selhání. Pětiletá celková mortalita zůstává okolo 66 procent. Během dvou let přežívá bez hospitalizace třetina pacientů, bez ohledu na EF. Riziko v období vulnerabilní fáze po propuštění lze ovlivnit farmakologickými i nefarmakologickými postupy. Důležitá je kontrola komorbidit a časná kontrola po propuštění,“ shrnul prof. Pařenica.
Co nového přináší vericiguat v léčbě HFrEF?
Jak vysvětlil prof. MUDr. Vojtěch Melenovský, CSc., z Kliniky kardiologie, IKEM Praha, při léčbě CHSS můžeme podávat léky, které antagonizují systém RAS, ale ještě výhodnější se jeví využít endogenní hormonální systémy v těle a posílit je tak, aby se negativní vliv RAS utlumil. Jednou z možností je signální systém NO/cGMP, který má antihypertrofické a antifibrotické účinky.
U pacientů s CHSS je snížená dostupnost NO a současně je přítomen oxidační stres, který inaktivuje sGC (solubilní guanylát cykláza). Oxidace sGC vede k endoteliální dysfunkci, plicní hypertenzi, rezistenci na NO. Na základě těchto poznatků začal vývoj nových farmak, která jsou schopna tento deficit korigovat, a to tím, že přímo stimulují sGC. Z testů zatím vyšly vítězně dva léky: riociguat, který se již úspěšně využívá v léčbě plicní arteriální hypertenze, a vericiguat. Ten byl úspěšně testován a v současné době se zavádí u léčby srdečního selhání. Molekula byla optimalizována, aby neměla žádné interakce se známými farmaky a aby bylo možné ji podávat i pacientům, kteří mají pokročilou renální dysfunkci, která se často pojí s CHSS, a zároveň aby antifibrotický a antiproliferační efekt převážil hypotenzní účinky.
Nejprve byl lék testován ve studii fáze II SOCRATES REDUCED u pacientů s HFrEF po epizodě dekompenzace. Zde lék ukázal vynikající toleranci, minimum hypotenzních účinků a možnou efektivitu ve smyslu redukce koncentrace natriuretických peptidů u nemocných s progredujícím srdečním selháním. Na základě těchto výsledků vznikla rozsáhlá studie VICTORIA, do níž bylo zařazeno 5 050 pacientů z 616 center a 42 zemí (včetně ČR), z nichž 2 526 bylo léčeno vericiguatem a 2 524 placebem.
Cílem této randomizované, dvojitě zaslepené a placebem kontrolované studie fáze III bylo posoudit klinickou efektivitu vericiguatu proti placebu při přidání k optimální farmakoterapii CHSS. Primárním ukazatelem studie byl výskyt kardiovaskulárního úmrtí nebo první hospitalizace pro srdeční selhání. Do studie byli zařazováni pacienti s těžší a progredující formou chronického srdečního selhání (NYHA II–IV, na stabilní optimální farmakoterapii, s ejekční frakcí levé komory (EF LK) < 45 %, s nedávnou hospitalizací pro CHSS nebo potřebou intravenózního podání diuretik). Pacienti museli mít výrazně zvýšenou koncentraci natriuretických peptidů: NT‑proBNP ≥ 1 000 pg/ml (≥ 1 600 pg/ml při fibrilaci síní) nebo BNP ≥ 300 pg/ml (≥ 500 pg/ml při fibrilaci síní) a museli mít systolický krevní tlak ≥ 100 mm Hg. Pacienti byli sledováni po dobu necelých 11 měsíců.
Toto klinické hodnocení ukázalo, že strategie zvýšení aktivity sGC u pokročilejších pacientů s HFrEF s recentní dekompenzací je efektivní a snižuje riziko klinických událostí, a to především riziko rehospitalizace pro CHSS. Ve studii byla pozorována absolutní redukce 4,2 události/100 pacientoroků, což je víc než např. ve studii DAPA‑HF nebo PARADIGM‑HF. Tento lék významně o 10 procent snížil primární ukazatele studie, tedy hospitalizaci pro CHSS nebo KV úmrtí.
„Zároveň se vericiguat ukázal jednoznačně jako bezpečný lék, dobře tolerovaný a snadno titrovatelný do maximální dávky bez nutnosti monitorace renálních funkcí, elektrolytů či krevního tlaku. Vericiguat může představovat novou možnost léčby pacientů se srdečním selháním, zvláště když použití ostatní farmakoterapie je omezeno hypotenzí nebo rozvojem kardiorenálního syndromu,“ uvedl prof. Melenovský.
Jak vysvětlil, specifikem studie VICTORIA byla vysoká morbidita zahrnuté populace a na základě retrospektivní analýzy lze předpokládat, že pokud by lék byl testován u méně nemocných pacientů, výsledky by mohly být ještě lepší. Nicméně i tato data stačila na schválení vericiguatu k léčbě CHSS a tento lék se již objevuje i v nových guidelines ESC z roku 2021. Zde je zařazen mezi přípravky doplňující základní čtyřkombinaci. „Jsou to léky, které lze zvážit k doplnění léčby CHSS. Zejména u pacientů s nedávnou epizodou dekompenzace to může být doplňkový lék, který sníží riziko rehospitalizace pro CHSS a KV mortalitu,“ zdůraznil prof. Melenovský.
Podle SPC je doporučeno vericiguat volit u pacientů, kteří mají symptomatické chronické HFrEF po nedávné epizodě dekompenzace vyžadující i.v. léčbu, současně s jinými přípravky k léčbě CHSS. Terapii zahajujeme po dosažení kompenzace a stabilizace volémie v dávce 2,5 mg 1× denně. Následuje zdvojnásobení dávky asi po dvou týdnech až do dosažení cílové dávky 10 mg/den. Při symptomatické hypotenzi nebo STK pod 90 mm Hg je doporučena přechodná downtitrace nebo vysazení, ale nejsou nutné laboratorní kontroly. Opatrnost je namístě při současném podávání organických nitrátů. Léčbu se nedoporučuje zahajovat při STK < 100 mm Hg, při eGFR < 15 ml/min/1,73 m2 nebo hemodialýze, při závažné dysfunkci jater a při souběžném užívání inhibitoru PDE5.
Subanalýza dat studie dle vstupního NT‑proBNP ukázala, že u pacientů s extrémní elevací NT‑proBNP (nad 8 000 pg/ml) vericiguat již nefungoval. Jednalo se spíše o kandidáty nefarmakologické léčby. Oproti tomu u pacientů s NT‑proBNP do této hodnoty přípravek významně redukoval jak hospitalizaci pro CHSS, tak i KV mortalitu. Zároveň se ukázalo, že pacienti s nižšími hodnotami NT‑proBNP těžili z této léčby ještě více, než byl průměr, což naznačuje, že lék může být účinný i u méně symptomatických a méně pokročilých pacientů, čímž se zabývají probíhající studie.
„Stimulátory sGC jsou novou skupinou KV léků augmentující signální cestu NO/cGMP. Vericiguat 10 mg denně přidaný k optimální farmakoterapii u pacientů s progredujícím HFrEF snižuje klinické události. Hlavní efekt je na první a opakované hospitalizace pro CHSS. Lék je velmi dobře tolerován, má příznivý bezpečnostní profil a jednoduchou titraci bez nutnosti kontroly biochemických parametrů. Navíc jej lze použít i u pacientů s pokročilou renální dysfunkcí (eGFR ≥ 0,15 ml/min/1,73 m2). Vericiguat může být přínosný jako ‚easy add‑on‘ lék u pokročilých/progredujících stadií CHSS (ale s NT‑proBNP < 800 pg/ml). Zatím nevyjasněné zůstávají otázky ohledně efektu na KV mortalitu u méně pokročilých forem onemocnění a ohledně kombinací s léky zvyšujícími cGMP (ARNI, inhibitory PDE5) nebo inhibitory SGLT‑2,“ shrnul prof. Melenovský.
První zkušenosti v klinické praxi s vericiguatem v ČR
„U srdečního selhání, které je progresivním onemocněním, se snažíme zabránit každé dekompenzaci a rehospitalizaci, která je bezpochyby negativním prognostickým faktorem, kdy je riziko mortality vysoké bez závislosti na tom, kde je pacient léčen. Registr PINNACLE jasně ukázal, že riziko rehospitalizací pro dekompenzaci CHSS stoupá v čase. Nemocní, kteří mají opakované hospitalizace pro dekompenzace CHSS, mají velmi špatnou prognózu, dvacet procent z nich i přes moderní léčbu CHSS umírá na vlastní CHSS, nikoli na komorbidity,“ upozornil prof. MUDr. Miloš Táborský, CSc., z I. interní kliniky – kardiologické LF UP a FN Olomouc. Jak se v průběhu sympozia ukázalo, naprostá většina přítomných lékařů by uvítala další farmakoterapeutickou možnost nad rámec optimalizované standardní léčby u svých opakovaně hospitalizovaných pacientů z důvodů dekompenzace HFrEF.
Guidelines ESC 2021 jasně definují pozici vericigulatu (II B), který je doporučen právě pro pacienty s dekompenzovaným CHSS, a díky doplnění tohoto léku se tak terapie zaměřuje na celou patofyziologii srdečního selhání. Zahájení terapie touto molekulou a veškerá optimalizace léčby, včetně nefarmakologické, by podle guidelines měly nastat hned v době hospitalizace pro dekompenzaci CHSS.
Jak prof. Táborský připomněl, dnes již máme data o tom, že ARNI podané za hospitalizace pro dekompenzaci CHSS jsou nepochybně přínosem, stejně jako vericigulat nebo inhibitory SGLT‑2. Ve fázi rehospitalizace nelze zapomínat ani na optimalizaci nefarmakologické léčby, kdy je potřeba myslet na možnost:
- ablace AVJ u pacientů s FS a nízkým procentem resynchronizační terapie (CRT),
- upgrade ½ D systémů na CRT‑D/stimulaci LBBB,
- reevaluace indikace HTx u pacientů v transplantačním oknu,
- ablace komorových i síňových tachykardií, které vedou k progresi CHSS,
- modulace srdeční kontraktility (CCM) – od 1. 5. 2022 má pět českých center možnost specificky řešit určité pacienty pomocí CCM,
- nově i na hemodynamický monitor – v ČR (IKEM) jsou již první zkušenosti se systémem CARDIOMEMS.
Prof. Táborský se podělil i o první klinické zkušenosti s vericigulatem u skupiny pacientů léčených na jeho pracovišti. „Zatím je potřeba žádat o úhradu v režimu § 16, kde předkládáme jednak žádanku o schválení zvýšené úhrady, dále sumarizaci klinického stavu, včetně aktuální terapie, propouštěcí zprávu s jasně dokumentovanými opakovanými rehospitalizacemi pro dekompenzace CHSS a cenovou kalkulaci léku. Mezi prvními pacienty jsou muži i ženy od 60 do 80 let věku se značným počtem dekompenzací v posledních 24 měsících.“
Kazuistika
Muž, nar. 1962, neischemická kardiomyopatie, těžká dysfunkce levé komory (EF LK 0,20) a aneurysma LK. Je léčen ve spádovém centru, kde byla realizována farmakologická terapie + CRT se suboptimálním výsledkem. Od ledna 2021 byl šestkrát hospitalizován pro dekompenzaci CHSS, v IKEM byla dvakrát provedena katetrizační ablace frekventních komorových tachykardií. Pacient byl těžce symptomatický, kvůli hypotenzi bylo nutno ukončit terapii sakubitril/valsartanem a přejít pouze na nízké dávky ramiprilu, BB a MRA. Netoleroval ani jednu ze dvou molekul inhibitoru SGLT‑2, objevila se hypoglykémie jako raritní NÚ u CHSS. V listopadu 2021 byly všechny možnosti léčby vyčerpány. Byla podána žádost na VZP o úhradu vericiguatu, která byla dvakrát odmítnuta kvůli vyjádření revizního lékaře, podle něhož nebyly splněny podmínky pro § 16. Pacient souhlasil s tím, že si léčbu bude hradit sám, v současné době je na terapii Verquvo (vericigulat) 5,0 mg denně v ambulantním režimu při kontrolách každých šest až osm týdnů. „Pacient od té doby neměl jedinou hospitalizaci, neměl jedinou arytmii a lék toleruje velmi dobře. Tito pacienti jsou složití a je potřeba se jim opravdu věnovat. Zároveň věříme, že se nám u tohoto nového léku podaří vyjednat rozumné úhradové podmínky,“ uvedl prof. Táborský.
Jak uzavřel, v současné době jsme svědky toho, že máme k dispozici novou molekulu – vericiguat, která působí na dosud nevyužitou dráhu patofyziologie srdečního selhání s cílem zlepšit myokardiální a vaskulární funkce. Jde o bezpečný lék s jednoduchou titrací, který lze kombinovat s dalšími léky pro CHSS. Zároveň, jak ukázala studie VICTORIA, lék je účinný u specifické vysoce rizikové skupiny pacientů s nedávnou dekompenzací CHSS. Signifikantní redukce rizika hospitalizace pro CHSS nebo KV úmrtí je o 4,2 příhody na 100 pacientoroků (NNT 24). Nežádoucí účinky jsou porovnatelné s placebem stejně jako výskyt symptomatické hypotenze a synkopy. Nejen přednášející, ale i téměř sto procent přítomných lékařů v sále je přesvědčeno, že po stanovení úhrady jsou inovativní terapie skutečnou šancí zlepšit prognózu a kvalitu života pacientů s velmi pokročilým srdečním selháním.