Onkologii posouvá jak nástup precizní medicíny, tak optimalizace chemoterapie
Nádory zažívacího traktu stále představují obrovskou zátěž pro nemocné, jejich blízké i celý systém. A tato zátěž se bude zvyšovat už jen spolu s tím, jak populace stárne. Jak ji alespoň výrazně zmírnit? Na tuto otázku se zaměřilo minikolokvium podpořené společností Servier, které tvořilo součást odborného programu letošního kongresu PragueONCO.
Na úvod sympozia MUDr. Tomáš Svoboda, Ph.D., z Onkologické a radioterapeutické kliniky LF UK a FN Plzeň připomněl, že kolorektální karcinom, karcinom pankreatu nebo cholangiocelulární karcinom sice představují odlišná onemocnění, pokud jde o výskyt nebo prognózu, přesto mají něco společného – a to praktické uplatnění precizní medicíny. Prof. MUDr. Luboš Petruželka, CSc., z Onkologické kliniky 1. LF UK, ÚVN a VFN v Praze doplnil, že u některých nádorů, zejména biliárního traktu a časem i u karcinomu pankreatu, lze již hovořit dokonce o počátcích období „ultraprecizní“ medicíny, onkologie se však stále neobejde bez chemoterapie (CHT).
Proč chemoterapie zůstává základním pilířem léčby
Jak uvedl doc. MUDr. Michal Vočka, Ph.D., z Onkologické kliniky 1. LF UK a VFN v Praze, v éře precizní onkologie stále častěji podklady pro testování léků a jejich schvalování ze strany regulačních agentur tvoří data založená na přítomnosti prediktivních markerů, už méně na lokalizaci nádorového onemocnění [1]. To podtrhuje potřebu kvalitního bioptického materiálu a včasného vyšetření, ideálně hned při diagnostice a před zahájením léčby. Molekulární profilování umožňuje dělit pacienty na podskupiny, které pak mohou podstupovat specifickou léčbu. Realita se však podle doc. Vočky od této ideální představy přece jenom poněkud liší. Často sice dochází k výraznému ovlivnění přežití, někteří pacienti však navzdory prediktorům ze specifické léčby neprofitují. Faktem podle doc. Vočky zůstává, že „jednoduchá“ a „stará“ CHT výrazně prodloužila přežití u většiny diagnóz, funguje u většiny pacientů s danou diagnózou a u velké části malignit GIT stále představuje páteř terapie.
Kolorektální karcinom
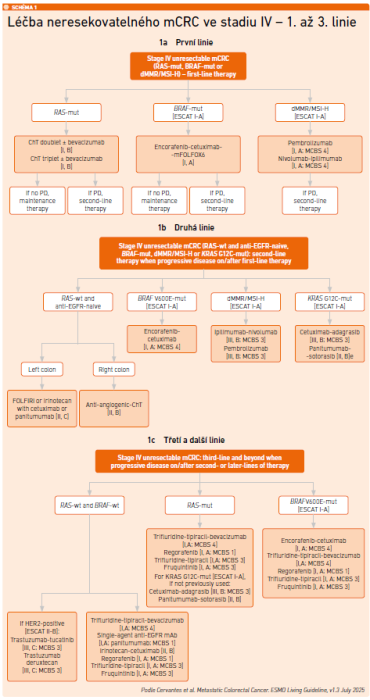 Poté se doc. Vočka již blíže zaměřil na problematiku kolorektálního karcinomu. V absolutním počtu tyto nádory sice v čase klesají, nezmenšuje se však podíl pacientů, kteří přicházejí s generalizovaným onemocněním (20–25 %). Před zahájením terapie je nutné molekulární vyšetření (RAS, BRAF, MSS, POLE/POLD1, HER2, NTRK) a na základě těchto molekulárních cílů se pacienti s CRC dělí na stále menší soubory s odlišnou strategií terapie (viz schéma 1). Přestože ovšem rozšiřování léčebných možností a větší využití lokálních metod postupně zlepšují přežití, většinu pacientů se nedaří vyléčit [2].
Poté se doc. Vočka již blíže zaměřil na problematiku kolorektálního karcinomu. V absolutním počtu tyto nádory sice v čase klesají, nezmenšuje se však podíl pacientů, kteří přicházejí s generalizovaným onemocněním (20–25 %). Před zahájením terapie je nutné molekulární vyšetření (RAS, BRAF, MSS, POLE/POLD1, HER2, NTRK) a na základě těchto molekulárních cílů se pacienti s CRC dělí na stále menší soubory s odlišnou strategií terapie (viz schéma 1). Přestože ovšem rozšiřování léčebných možností a větší využití lokálních metod postupně zlepšují přežití, většinu pacientů se nedaří vyléčit [2].
Základem léčby u většiny pacientů zůstává chemoterapie, ve všech třech liniích si udržuje pevné místo (FOLFOX, FOLFIRI, FOLFOXIRI, FUFA). Ve 3. linii je preferovanou volbou trifluridin/tipiracil (FTD/TPI) ± bevacizumab (beva) (viz schéma 1c). Na základě studie fáze III SUNLIGHT by měla být upřednostňována kombinace FTD/TPI s beva (pokud není beva kontraindikován) [3]. FTD/TPI prokázal dobrou účinnost i bezpečnost. Jeho nežádoucí účinky (NÚ) spočívají především v poklesu počtu krvinek, což, jak uvedl přednášející, „pacient na sobě příliš nepozoruje, a tím pádem není stresován nežádoucími účinky, které by ho v životě limitovaly“. Zdůraznil, že z publikovaných analýz vyplynulo, že „pokud dojde k poklesu počtu krvinek, který brání v dalším podání FTD/TPI, a do sedmi dnů k normalizaci počtu bílých krvinek, není doporučováno redukovat dávku, protože se tím snižuje účinnost, a zároveň ti, u kterých došlo k poklesu, mají větší benefit z terapie“.
 Trvá snaha přesunout opravdu účinnou terapii (inhibitory BRAF či RAS, imunoterapie, anti‑HER2) do časnějších linií. Příznivě se do lepšího přežití pacientů propisuje úzká spolupráce s chirurgy, radioterapeuty a intervenčními radiology.
Trvá snaha přesunout opravdu účinnou terapii (inhibitory BRAF či RAS, imunoterapie, anti‑HER2) do časnějších linií. Příznivě se do lepšího přežití pacientů propisuje úzká spolupráce s chirurgy, radioterapeuty a intervenčními radiology.
Karcinom pankreatu (PC)
Drtivou většinu (> 90 %) případů PC tvoří adenokarcinomy (PAC). Karcinomů pankreatu stále přibývá, křivky mortality následují křivky incidence a neklesá podíl generalizovaných onemocnění (asi 45–50 %) ani lokálně pokročilých (asi 10–15 %). Vyskytuje se většinou (75 %) ve věku nad 65 let (40 % ve věku nad 75 let) [2].
Molekulární cíl, na nějž se lze zaměřit, je přítomen jen asi u maximálně 20 procent případů, v běžné praxi spíše 10 procent. Často pro tento účel není k dispozici dostatečné množství materiálu a dosažitelnost pro novou biopsii je obtížná. Léčba je pro řadu pacientů neúnosná. Její základ představuje nadále CHT. V 1. linii ukazují stejné výsledky z hlediska OS i PFS režimy FOLFIRINOX a gemcitabin (gem) + nab‑paklitaxel. Standard ve 2. a dalších liniích po terapii založené na gem tvoří pegylovaný lipozomální irinotekan (nal‑IRI) + FUFA (na základě studie fáze III NAPOLI‑1) [4]. Trvá snaha snížit incidenci III. a IV. stupně sledováním a časnou diagnostikou rizikových osob.
Karcinom žlučníku a žlučových cest
I zde se v drtivé většině případů (> 95 %) vyskytují adenokarcinomy (CCA). Incidence i mortalita zůstávají stejné, podíl generalizovaných onemocnění neklesá (cca 35–40 %), stejně tak lokálně pokročilých (cca 15–20 %). Většina (80 %) se taktéž vyskytuje u osob starších 65 let (45 % ve věku nad 75 let) [2].
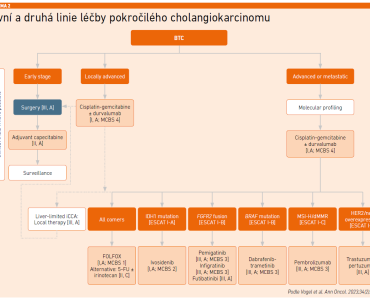
U více než 50 procent je přítomen molekulární cíl, nejvíce v případě intrahepatálních cholangiokarcinomů. Jedná se o alterace FGFR2, mutace IDH1 a alterace HER2. Je tedy nutné vyšetření, ideálně hned na začátku. Základ 1. linie léčby tvoří CHT v kombinaci s imunoterapií (stále na paragraf 16). Ve 2. linii se podává terapie podle molekulárního cíle. Například u 15–20 procent pacientů je přítomna mutace IDH1 a u nich prokázal účinnost ivosidenib (studie fáze III ClarIDHy) [5,6]. Dlouhodobí respondéři tvoří malou, ale důležitou skupinu pacientů, „které bychom měli být schopni vybrat, ale zatím nejsme“. Pokud není možné léčbu specificky zaměřit, volí se FOLFOX (viz schéma 2).
Režim SUNLIGHT ve 3. linii léčby mCRC – kazuistika
O své zkušenosti s podáváním kombinace FTD/TPI + beva podle studie SUNLIGHT v klinické praxi se s auditoriem podělil MUDr. Marián Liberko, Ph.D., z Onkologické kliniky 3. LF UK a FNKV Praha. Jak uvedl, režim SUNLIGHT ve FNKV dosud podstoupilo přes 20 pacientů, z nich u 17 (12 žen, 5 mužů) již bylo provedeno alespoň jedno CT vyšetření. V této 17členné skupině je medián věku 71 let (43–78). Podle přednášejícího data z reálné praxe odpovídají výsledkům studie SUNLIGHT, tolerance léčby je přijatelná, toxicita převážně laboratorní a pacienti si udržují dobrý výkonnostní status (PS) s možností další linie léčby. Připojil také kazuistiku pacientky s mCRC s mutací BRAF a MSI‑H nádorem.
Popis případu
Žena narozená v r. 1948 (v době diagnózy cca 75letá), vdaná, aktuálně starobní důchodkyně, nekuřačka a abstinentka, s pozitivní rodinnou anamnézou (matka zemřela v 57 letech na karcinosarkom dělohy, bratr v 65 letech na karcinom sigmatu) se léčí s arteriální hypertenzí, fibrilací síní, dyslipidémií a byla sledována po excizi maligního melanomu na levé horní končetině. Užívala medikaci odpovídající věku.
Pro pozitivní test okultního krvácení byla praktickým lékařem odeslána na koloskopii, při níž však došlo k iatrogenní perforaci tlustého střeva s nutností semiakutní operace. Odhalen byl karcinom apendixu s expanzí do pravého tračníku a gynekologické oblasti. Dne 4. 12. 2022 podstoupila rozsáhlou operaci zahrnující hemikolektomii i adnexektomii. Operace však byla spojena s komplikacemi, takže rekonvalescence trvala poměrně dlouho. Histologie prokázala mucinózní adenokarcinom apendixu G2–3 a metastázy v ovariích, omentu a peritoneu – pT4bpN1b(2/7)pM1c.
Na první kontrolu na spádové onkologii se dostavila až v březnu 2023. Vzhledem k tříměsíčnímu odstupu od operace a PS 2 WHO byla sledována, CT neprokázala relaps onemocnění.
V květnu 2023 podstoupila okluzi ileostomie s komplikacemi a protrahovaným hojením.
V říjnu 2023 byla zjištěna elevace markerů, na CT při děložním rohu vlevo cystoidní formace nejasné etiologie. Vaginální ultrazvuk detekoval dva útvary poblíž dělohy.
V listopadu 2023 PET/CT potvrdila relaps onemocnění. Největší postižení se nacházelo v pánvi, několik ložisek ale i v dutině břišní. Pacientka byla odeslána na pracoviště přednášejícího.
Na onkologii ve FNKV
Pacientka měla dobrý PS (1 WHO), PET/CT ukázala FDG méně avidní peritoneální ložiska, bez lymfadenopatie a orgánových metastáz, z prediktivních markerů byly zjištěny mutace BRAF, wtRAS a mikrosatelitová instabilita (MSI‑H).
Jelikož ještě nebylo možné indikovat nivolumab s ipilimumabem, jako 1. linii léčby mCRC začala 4. 12. 2023 užívat pembrolizumab v monoterapii (viz schéma 1a).
V březnu 2024 podstoupila další CT, z ní sice vyplynula progrese, pacientka ale byla klinicky bez symptomů a markery byly rovněž neprůkazné. Dále tedy užívala pembrolizumab. Progrese se zcela potvrdila v červnu 2024. PFS na imunoterapii trvalo pouze šest měsíců.
Jako 2. linii léčby wtRAS, mtBRAF, MSI‑H mCRC začala 3. 7. 2024 užívat kombinaci enkorafenib + cetuximab (viz schéma 1b), CT v září 2024 ale prokázala rozsáhlou progresi v břiše i pánvi. PFS trvalo tři měsíce.
3. linie léčby byla zahájena 23. 10. 2024, a to kombinací FTD/TPI + beva (viz schéma 1c). Pacientka dostávala FTD/TPI v dávce 70 mg 1–0–1 a bevacizumab 500 mg každých 14 dní.
Od září 2024 do října 2025 žena podstoupila několik CT vyšetření, ta opakovaně potvrdila stabilizaci onemocnění – vícečetná metastatická ložiska v peritoneu, metastázy kapsuly sleziny i kapsuly jater, nejrozsáhlejší postižení v malé pánvi, některá ložiska se zvětšila, jiná zmenšila, nová se neobjevila. Pacientka si udržela PS 1 WHO.
V lednu 2026 (v době konání kongresu PragueONCO) pokračovala v užívání FTD/TPI + beva (14. cyklus).
Za celé období užívání této kombinace se vyskytly zejména hematologické NÚ – anémie, neutropenie (obvykle G1–2 před zahájením dalšího cyklu), zpočátku také GI povahy (průjmy, nauzea, zvracení, byly ale dobře řešitelné), alopecie. PFS zatím činilo více než 15 měsíců.
Nal‑IRI jako standard ve 2. linii léčby mPDAC – kazuistika
Vlastní zkušenost sdílel také MUDr. Stanislav John, Ph.D., z Kliniky onkologie a radioterapie LF UK a FN Hradec Králové. Tentokrát se jednalo o kazuistiku pacientky s generalizovaným duktálním adenokarcinomem pankreatu (mPDAC) léčené pegylovaným lipozomálním irinotekanem.
Popis případu
Žena narozená v r. 1957, s PS 0 dle WHO, nekuřačka, alkohol konzumující jen velmi výjimečně, si v dubnu 2022 stěžovala na hubnutí a bolesti zad a nadbřišku. Otec zemřel v 74 letech na tumor prostaty. Poměrně rychle jí byl diagnostikován nádor slinivky břišní – v červnu 2022 prokázaly UZ + CT trupu resekabilní tumor těla pankreatu (cT3 cN1 M0), podstoupila bezprostřední operaci, kterou zvládla. Vícečetné cysty se nacházely v játrech a ledvinách. V úvodu měla také poměrně vysokou hodnotu onkomarkeru CA19‑9. Histologicky se jednalo o nádor pT3 pN2 M0, v pankreatu se nacházela dvě ložiska s infiltrací žíly, z 33 uzlin bylo 11 pozitivních.
Pooperační průběh byl vcelku dobrý, až na drobnou plicní embolizaci i přes zajištění nízkomolekulárním heparinem (zůstala bez následků).
Jako adjuvantní léčba byl zvolen modifikovaný FOLFIRINOX (mFOLFIRINOX) na základě dat ze studie PRODIGE 24 [7]. V období od srpna do listopadu 2022 dostala šest cyklů, pak muselo být podávání ukončeno pro NÚ a do září 2023 byla sledována.
V září 2023 došlo k lokální progresi retroperitoneálně s infiltrací jaterního hilu.
Jako 1. linii paliativní léčby užívala od září 2023 do března 2024 nab‑paklitaxel + gem (6 cyklů), avšak onemocnění lokálně progredovalo (infiltrát hilu jater, lůžka tumoru). V dubnu 2024 podstoupila analgetickou radioterapii tumoru paraaortálně.
V červnu 2024 CT ukázalo nové metastatické ložisko v játrech. Hodnoty markerů stouply.
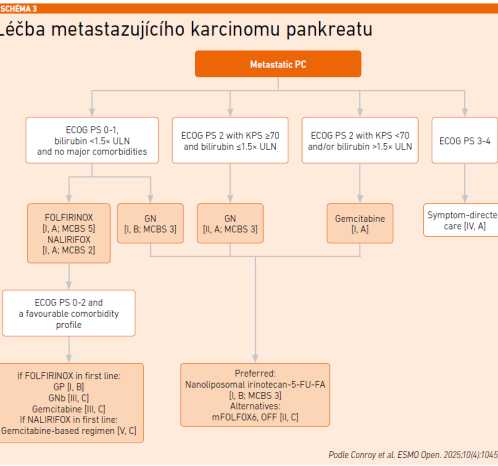 Zvolena tedy byla paliativní léčba 2. linie na základě doporučených postupů vycházejících ze studie NAPOLI‑1 – nal‑IRI + 5‑FU + FA (viz schéma 3). Pacientka ji zahájila v srpnu 2024 a v listopadu 2024 CT ukázala parciální regresi. Přednášející poznamenal, že v praxi se potvrzuje, že tento režim léčby je spojen také s menší toxicitou oproti FOLFIRINOX.
Zvolena tedy byla paliativní léčba 2. linie na základě doporučených postupů vycházejících ze studie NAPOLI‑1 – nal‑IRI + 5‑FU + FA (viz schéma 3). Pacientka ji zahájila v srpnu 2024 a v listopadu 2024 CT ukázala parciální regresi. Přednášející poznamenal, že v praxi se potvrzuje, že tento režim léčby je spojen také s menší toxicitou oproti FOLFIRINOX.
Pacientka ovšem byla z léčby již velmi unavená, s ohledem na výsledky tedy byly po dohodě s ní nastaveny na období od března do října 2025 terapeutické prázdniny.
V říjnu 2025 došlo k progresi metastázy v játrech, léčba proto znovu pokračovala.
V době konání PragueONCO 2026 byla na únor 2026 plánována CT trupu po 16. cyklu.
Uplatnění režimu s nal‑IRI
Přednášející poznamenal, že za posledních deset let selhalo 21 studií a uspěly dvě – obě testovaly nal‑IRI a vedly k jeho schválení ve dvou indikacích (NAPOLI 1 s nal‑IRI + 5‑FU/LV a NAPOLI 3 s NALIRIFOX) [4,8]. Mimo toho byl ještě zaznamenán úspěch u udržovací terapie olaparibem (2019).
CHT stále představuje základ léčby ve všech jejích fázích a režim s nal‑IRI se uplatňuje v 1. i dalších liniích. Ve 2. linii tvoří standard pro pacienty, u nichž došlo k progresi po terapii založené na gemcitabinu. Přednášející potvrdil, že určení vhodného režimu je často obtížné (komorbidity, předléčenost, nežádoucí účinky…) a vždy je potřeba zvážit klinické hodnocení. I u karcinomů slinivky může pomoci rozšířit možnosti léčby molekulární profilování (BRCA, KRAS, MMR/MSI, BRAF, …). Velmi apeloval na kvalitní podpůrnou terapii (výživa, tlumení bolesti aj.).
Ivosidenib jako cesta k delšímu přežití pacientky s CCA a mIDH1 – kazuistika
Jak již bylo řečeno, karcinom žlučových cest patří mezi nádory se špatnou prognózou. MUDr. Zdeněk Linke, primář Onkologické kliniky 2. LF UK a FN Motol, Praha, k tomu doplnil, že jen velmi málo pacientů s metastatickým onemocněním přežije pět let a u 78 procent pacientů dojde k progresi na režimu gem + cis v 1. linii léčby. V 2. linii už zbývá jen málo možností. Přednášející vyzdvihl, že i u tohoto nádoru má zásadní roli molekulární profilování. Za nejběžnější genetické změny u CCA označil IDH1 a FGFR2, jako řídicí pak mutaci IDH1, přičemž cílenou léčbou je lze ovlivnit. Slovy dr. Linkeho se přitom jedná především o 2. linii léčby. U nádorů s mutací IDH1 lze dosáhnout zdvojnásobení mediánu OS ivosidenibem (podle dat z jeho registrační studie), který je na českém trhu dostupný (přes paragraf 16) od listopadu 2023. Za tu dobu jím již bylo léčeno 18 pacientů, 78 procent ve 2. linii, pět bylo v době konání PragueONCO 2026 aktuálně na léčbě. Možnosti ivosidenibu dr. Linke přiblížil na příkladu z praxe. „Tato pacientka byla na této léčbě rok. A jednalo se o rok kvalitního života, na rozdíl od předchozí chemoterapie,“ předeslal.
Popis případu
Žena narozená v r. 1955 podstoupila dne 19. 11. 2021 biopsii jednoho z mnoha jaterních ložisek primárně metastazujícího nádoru. Metastázy se nacházely i v plicích, v lymfatických uzlinách v podjaterní krajině. Histologie doložila cholangiocelulární karcinom. Pacientka byla HER2 negativní, mikrosatelitově stabilní (MSS) a PD‑L1 pozitivní.
Dne 6. 12. 2021 zahájila paliativní léčbu CHT režimem cisplatina + gemcitabin, který navodil parciální remisi (PR) zjištěnou v únoru 2022. Neměla výraznější kumulativní toxicitu a na léčbě setrvala dlouho (téměř 2 roky) – naposledy byla PR potvrzena v červenci 2023, v říjnu 2023 se již ukázala nová jaterní ložiska a došlo k růstu plicních metastáz.
Vzhledem k PD‑L1 pozitivitě byl revizním lékařem schválen nivolumab, ten užívala od 8. 11. 2023 v dávce 240 mg každé dva týdny. Po páté aplikaci 5. 1. 2024 byla zjištěna progrese jaterních ložisek a regrese plicních metastáz, stav byl hodnocen jako možná pseudoprogrese. Po osmé aplikaci 21. 2. 2024 se potvrdila progrese jaterních ložisek a podjaterní uzliny, a tedy progrese nemoci, což vedlo k ukončení 2. linie.
Od 5. 3. 2024 pacientka dostávala paliativní chemoterapii FOLFOX. Souběžně bylo rovněž zažádáno o molekulární biologii nádoru (NGS), která ještě nebyla v úvodním panelu vyšetření. U IDH1 byla detekována hot spot patogenní varianta R132, u IDH2 patogenní varianta neprokázána. Již 23. května 2024 ukázala PET/CT morfologickou i metabolickou progresi jaterních metastáz a dvě nové jaterní metastázy (primární progrese).
Dne 29. 5. 2024 proto byla podána žádost (par. 16) o úhradu ivosidenibu. Pro případ neschválení byla připravena terapie FOLFIRI. Revizní lékař požadoval prokázat efektivitu ivosidenibu i ve vyšší než 2. linii, která byla doložena daty z registrační studie – 47 procent pacientů bylo léčeno ve 3. a dalších liniích [5], a 15. 7. 2024 byla úhrada schválena.
Od 20. 7. 2024 pacientka denně užívala ivosidenib v dávce 250 mg tbl. 2–0–0, přičemž z jejího subjektivního pohledu měl nulovou toxicitu. Laboratorně přetrvávala anémie G1, jinak byla toxicita také nulová.
První hodnoticí PET/CT vyšetření proběhlo 2. 10. 2024 a většina jaterních ložisek se nacházela v morfologické i metabolické regresi, plicní a uzlinové metastázy zůstávaly bez změny – stav byl hodnocen jako parciální remise.
Druhé hodnoticí PET/CT vyšetření pacientka podstoupila 3. 1. 2025, a to s výsledkem trvání PR (jaterní ložiska i plicní a uzlinové metastázy zůstávaly bez změny a významně klesla metabolická aktivita).
Až 4. hodnoticí PET/CT vyšetření z 26. 6. 2025 ukázalo progresi choroby (stávající jaterní ložiska se zvětšila a objevila se nová, plicní i uzlinová ložiska byla bez změny morfologické i metabolické). Léčba ivosidenibem tedy byla 3. 7. 2025 ukončena.
Dne 9. 7. 2025 pacientka zahájila paliativní chemoterapii FOLFIRI.
Po čtyřech cyklech proběhlo kontrolní vyšetření. PET/CT 26. 9. 2025 ukázala primární progresi nemoci; výraznou progresi metabolickou a morfologickou i co do počtu nádorových ložisek jater, plicní a uzlinové metastázy zůstávaly bez změny.
Proto od konce září 2025 žena podstupuje optimální podpůrnou péči. Poslední kontrola proběhla 23. 12. 2025. Po dohodě s pacientkou a podle jejích preferencí byl nasazen p.o. kapecitabin.
Přednášející konstatoval, že kazuistika potvrzuje benefit ivosidenibu u pacientů s CCA – PFS 12 měsíců při podání ve 4. linii léčby.
Cesta k maximalizaci šancí pacienta
MUDr. Linke zdůraznil, že molekulární profilování nádorů by mělo být prováděno co nejdříve – při diagnostice CCA, před 1. linií léčby nebo během ní, aby se maximalizovala šance na co nejdelší pozitivní klinickou odpověď a pacient byl schopen terapie. Až polovina pacientů s CCA podle jeho slov může mít léčebně zacílitelnou mutaci a profitovat z takovéto léčby.
Bylo tedy možné shrnout, že včasné molekulární testování je nutnost, protože představuje klíč k identifikaci zacílitelných mutací a personalizované léčbě – tvoří podklad pro nejúčinnější možnost terapie. Nicméně u většiny nádorů se jedná o cestu pro omezený počet pacientů (CRC, PAC ~20 %, CCA ~ 50 %). CHT ± anti‑EGFR/anti‑VEGF tak stále zůstává páteří léčebných režimů nádorů GIT.
Precizní léčba představuje nezastupitelnou součást léčebné mozaiky – nenahrazuje CHT, ale doplňuje, pacientovi přináší výrazný profit. Kombinace s CHT působí synergicky – zlepšuje přežití a kvalitu života. Obojí je součástí individualizovaného přístupu k pacientovi, přičemž personalizovaná léčba jediná dává pacientovi naději na vyléčení nebo co nejdelší přežití.

Literatura: 1. Suehnholz SP, Nissan MH, Zhang H, et al. Quantifying the Expanding Landscape of Clinical Actionability for Patients with Cancer. Cancer Discov. 2024;14(1):49–65. 2. Systém pro vizualizaci onkologických dat. [online]. [cit. 2026‑01‑15]. Dostupné z: www.svod.cz. 3. Prager GW, Taieb J, Fakih M, et al.; SUNLIGHT Investigators. Trifluridine‑Tipiracil and Bevacizumab in Refractory Metastatic Colorectal Cancer. N Engl J Med. 2023;388(18):1657–1667. 4. Wang‑Gillam A, Hubner RA, Siveke JT, et al. NAPOLI‑1 phase 3 study of liposomal irinotecan in metastatic pancreatic cancer: Final overall survival analysis and characteristics of long‑term survivors. Eur J Cancer. 2019;108:78–87. 5. Abou‑Alfa GK, Macarulla T, Javle MM, et al. Ivosidenib in IDH1‑mutant, chemotherapy‑refractory cholangiocarcinoma (ClarIDHy): a multicentre, randomised, double‑blind, placebo‑controlled, phase 3 study. Lancet Oncol. 2020;21(6):796–807. 6. Zhu AX, Macarulla T, Javle MM, et al. Final Overall Survival Efficacy Results of Ivosidenib for Patients With Advanced Cholangiocarcinoma With IDH1 Mutation: The Phase 3 Randomized Clinical ClarIDHy Trial. JAMA Oncol. 2021;7(11):1669–1677. 7. Conroy T, Hammel P, Hebbar M, et al.; Canadian Cancer Trials Group and the Unicancer‑GI–PRODIGE Group. FOLFIRINOX or Gemcitabine as Adjuvant Therapy for Pancreatic Cancer. N Engl J Med. 2018;379(25):2395–2406. 8. Wainberg ZA, Melisi D, Macarulla T, et al. NALIRIFOX versus nab‑paclitaxel and gemcitabine in treatment‑naive patients with metastatic pancreatic ductal adenocarcinoma (NAPOLI 3): a randomised, open‑label, phase 3 trial. Lancet. 2023;402(10409):1272–1281.