Sekundární žilní insuficience – posttrombotický syndrom
Sekundární žilní insuficience je stav, kdy dojde k poruše žilního návratu na podkladě patologického procesu, který může proběhnout intraluminálně či extraluminálně, resp. intravenózně/extravenózně. Obě situace nám zohledňuje i poslední revize klinické klasifikace chronického žilního onemocnění CEAP (C – klinické projevy, E – etiologie, A – anatomická distribuce, P – patofyziologie), kde v položce etiologie (E) se správně uvádí: E si = etiologie sekundární intravenózní, E se = etiologie sekundární extravenózní.1
Jednou z podob sekundární žilní insuficience je tzv. posttrombotický syndrom (PTS) – chronické onemocnění, které se vyvíjí u 20–50 % pacientů po hluboké žilní trombóze (DVT).2 PTS má nepříznivý vliv na zdraví a kvalitu života a je též spojen s nemalými náklady jak ze systému zdravotní péče, tak ze zdrojů samotného postiženého jednotlivce.
Většina klinických studií a doporučených postupů týkajících se DVT se zaměřuje na účinnost léčby a prevenci recidivy DVT a žilní tromboembolie (VTE) v krátkodobém (3 měsíce) až střednědobém (12 měsíců) horizontu po DVT. V posledních 10–15 letech se však PTS stále více zdůrazňuje jako častý a významný následek DVT. Nedávné studie zlepšily porozumění epidemiologii, rizikovým faktorům a zdravotním a ekonomickým dopadům PTS. Byla zveřejněna doporučení pro standardizaci a definice PTS pro klinické studie.3
Co je PTS a proč je důležitý
PTS je klinická porucha spojená s bolestí a postižením, jež jsou důsledkem chronické žilní nedostatečnosti po DVT. PTS je nejčastější komplikací DVT. Vyskytuje se u 20–50 % pacientů do dvou let od stanovení diagnózy DVT,4,5 a to i v případě, že jsou pacienti adekvátně léčeni antikoagulační terapií. V 5–10 % případů je jeho forma závažná. V průměru se tedy asi 6 z 10 pacientů s DVT zotaví bez jakýchkoli zbytkových příznaků, 3 z 10 pacientů mají určitý stupeň PTS a u 1 z 10 až 1 z 20 pacientů se vyvine závažný PTS, který může zahrnovat bércové ulcerace. Celková odhadovaná incidence VTE je 0,7–2 případy na 1 000 osoboroků a s věkem se zvyšuje,6,7 takže více než třetina případů se vyskytuje u osob starších 60 let.8 VTE představuje rostoucí problém veřejného zdraví v důsledku zvýšené průměrné délky života, rostoucího podílu starších osob v populaci a očekávaného nárůstu prevalence PTS.
Vzhledem k vysoké prevalenci a chronicitě je PTS nákladným onemocněním. Kanadská studie odhadla, že celkové náklady na jednoho pacienta s PTS za dvouleté období byly téměř o 50 % vyšší než u pacientů s DVT bez PTS.9 Vysoké náklady spojené s PTS dokazují i poměrně hojně americké studie.10–12 Náklady jsou zvláště vysoké u pacientů, u kterých došlo ke vzniku chronických bércových ulcerací. Výrazný socioekonomický dopad dokazuje též celá řada sociálních studií.13–16
Klinické projevy PTS a jeho základní patofyziologie
Klinické projevy PTS jsou podobné jako u primární žilní nedostatečnosti a zahrnují řadu symptomů a příznaků, které se u jednotlivých pacientů liší.17 Mezi typické symptomy patří bolest nohou, pocit těžkých nohou, vnímání tahu v končetinách nebo únava a otoky nohou. Mezi nejtypičtější příznaky patří otoky, lipodermatoskleróza, tmavé zbarvení bérců. Typický je též rozvoj corona phlebectatica, postupný rozvoj kožních změn a v nejkrajnějším případě vznik bércové ulcerace. Závažnost příznaků a známek se pohybuje od minimálního nepohodlí a kosmetických problémů až po závažné klinické projevy, jako je chronická bolest, neléčitelné otoky a vředy.18 Intenzita příznaků a symptomů se v průběhu dne mění, respektive zvyšuje.
Předpokládá se, že PTS se vyvíjí po DVT v důsledku žilní hypertenze (tj. zvýšeného žilního tlaku).19 K žilní hypertenzi přispívají dva patologické mechanismy: přetrvávající (akutní, poté reziduální) žilní obstrukce (RVO) a žilní reflux způsobený poškozením žilních chlopní.20 Rozvoj zánětlivých procesů v žilní stěně a jejím okolí je prakticky ve shodě jako v případě primární žilní insuficience. Je zde předpoklad existence genetické predispozice k PTS způsobené genovými polymorfismy spojenými hlavně s remodelací žilní stěny.21
Diagnostika PTS
Neexistuje žádný zlatý standard laboratorních, zobrazovacích nebo funkčních testů, který by stanovil diagnózu PTS. PTS se diagnostikuje primárně na základě klinických příznaků. Jde o přítomnost typických symptomů a subjektivních pocitů vnímaných pacientem s předchozí DVT. Symptomy PTS se mohou vyskytovat v různých kombinacích a mohou být trvalé nebo přerušované. Symptomy se obvykle zhoršují při stání, po statické zátěži ve vertikální poloze. Někdy se mohou zhoršit i po déletrvající chůzi. Naopak se zmírňují při odpočinku, elevaci končetin a horizontální poloze. U některých pacientů může trvat několik měsíců, než odeznějí počáteční bolest a otok spojené s akutní DVT, proto by diagnóza PTS měla být odložena až po odeznění akutní fáze (tj. 3–6 měsíců). Příznaky PTS se obvykle objevují během 3–6 měsíců po DVT, ale mohou se objevit až za 2 roky po DVT.22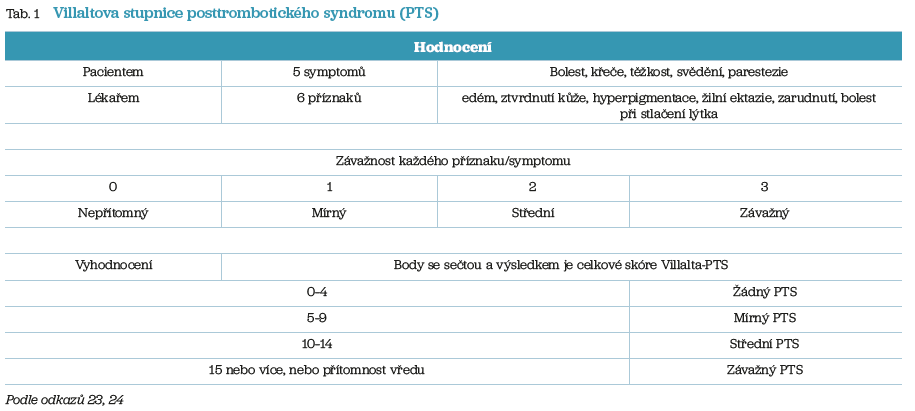
Villaltova stupnice PTS (někdy nazývaná Villalta–Prandoni škála)23 byla přijata Mezinárodní společností pro trombózu a hemostázu (ISTH) jako standard pro diagnostiku a hodnocení závažnosti PTS v klinických studiích.24 Jednotlivé části stupnice (5 symptomů a 6 příznaků) jsou hodnoceny na 4bodové stupnici závažnosti a body se sčítají, aby se získalo celkové skóre; skóre 4 označuje PTS (tab. 1). Villaltova stupnice PTS se ukázala jako platná, reprodukovatelná, citlivá na klinické změny a snadno použitelná.25 Pro popis stavu CVD je pak určena klasifikace CEAP. Ta má však jen popisný charakter a neslouží pro určení závažnosti postižení. Existují i další popisné systémy, které jsou však vhodné pro klinické studie, nikoli pro běžnou praxi.
Známé rizikové faktory PTS
Prozatím není možné přesně předpovědět absolutní riziko PTS u konkrétního pacienta s DVT. Jsou však známy konkrétní rizikové faktory, které pravděpodobnost rozvoje PTS zvyšují.
Rizikové faktory zřejmé v době diagnózy DVT:
- Vyšší věk zvyšuje riziko PTS.
- Zvýšený index tělesné hmotnosti (BMI) zvyšuje riziko PTS.
- Předchozí primární žilní nedostatečnost zvyšuje riziko PTS.26,27
- Riziko PTS je 2–3krát vyšší po proximální žilní trombóze (s postižením ilických žil nebo vena femoralis communis) než po distální (lýtkové) DVT. Zdá se, že to, zda byla DVT neprovokovaná, nebo sekundární (např. v důsledku nedávné operace, traumatu, imobilizace nebo aktivního nádorového onemocnění), nemá vliv na riziko vzniku PTS.5,24
- Pohlaví a dědičná trombofilie nepředstavují zvýšení rizikovosti PTS.24,28
- Riziko PTS se zvyšuje (až dvojnásobně), pokud je úroveň antikoagulace nedostatečná během prvních tří měsíců léčby. Toto platí zvláště pro antagonisty vitaminu K.29,30
- Recidivující ipsilaterální DVT zvyšuje riziko PTS 4–6krát.4,5
- Symptomy DVT přetrvávající v intervalu delším než jeden měsíc od bezprostřední akutní fáze DVT představují zvýšené riziko následného rozvoje PTS.5,31
- Reziduální trombóza prokázaná ultrazvukovým vyšetřením (např. 3–6 měsíců po akutní DVT) je spojena s 1,5–2násobně vyšším rizikem PTS.32
- Zvýšené hodnoty D‑dimerů v týdnech až měsících po DVT mohou být mírným rizikovým faktorem pro PTS.33
DVT a přímá orální antikoagulancia
Existují systematické přehledy a metaanalýzy, které naznačují, že léčba DVT přímými perorálními antikoagulancii (DOAC) je spojena s nižším rizikem rozvoje posttrombotického syndromu než léčba warfarinem, resp. antagonisty vitaminu K. Z dohledatelných studií vycházejí výsledky nejlépe pro rivaroxaban. Pro dabigatran se rozdíl oproti warfarinu neprokázal a pro edoxaban je náznak přínosu, ale data jsou omezená a výsledky nejednoznačné. Přímý důkaz ve smyslu velké randomizované studie navržené primárně k prevenci PTS podle volby antikoagulancia zatím chybí. Publikovaná data jsou výsledky observačních studií či post hoc analýz. Celkově jde tedy o „středně kvalitní“ sílu, resp. význam dat podporujících DOAC (zejména rivaroxaban) proti antagonistům vitaminu K pro snížení rizika PTS.34–38
Prevence PTS po DVT
- Primární prevence DVT
K prevenci VTE u vysoce rizikových pacientů a v rizikových situacích je doporučeno použití farmakologické nebo mechanické tromboprofylaxe.39–41
- Prevence recidivy DVT
Jelikož ipsilaterální recidiva DVT představuje významný rizikový faktor PTS, je klíčovým cílem prevence recidivy DVT zajištění optimální antikoagulace s odpovídající intenzitou a délkou trvání pro počáteční DVT.42
- Elastické kompresní punčochy
Elastické kompresní punčochy (KEP) mohou díky snížení otoků a žilní hypertenze pravděpodobně hrát roli v prevenci PTS. Existují však protichůdné údaje o dlouhodobé účinnosti KEP v prevenci PTS. Dvě malé randomizované otevřené studie uvádějí, že nošení elastických kompresních punčoch o délce A–D, tedy po koleno, o kompresi 30–40 mm Hg po dobu nejméně dvou let po proximální DVT, bylo účinné v prevenci PTS.24,43 Na základě těchto údajů doporučují konsenzuální pokyny založené na důkazech používání KEP po dobu nejméně dvou let po DVT k prevenci PTS.42,44 Jedna rozsáhlá (n = 803) multicentrická randomizovaná, placebem kontrolovaná studie však neprokázala žádný přínos kompresních punčoch aktivně nošených po dobu dvou let po proximální DVT pro prevenci PTS: míra PTS, recidivy VTE a skóre QoL (kvalita života) byly ve skupině s aktivně nošenými punčochami a ve skupině s placebem podobné.24 Též sekundární analýza této studie neprokázala žádný rozdíl ve skóre bolesti během prvních 60 dnů po DVT ve skupině s punčochami a ve skupině s placebem. Placebem kontrolovaný zaslepený design této studie je důležitou metodologickou silnou stránkou vzhledem k subjektivní povaze hodnocení PTS.45
- Včasná obnova průchodnosti pánevního řečiště
Riziko rozvoje PTS je vyšší u proximální DVT. Pokud jde o trombózu pánevního řečiště, je nutná snaha o co nejlepší obnovu žilní drenáže v této oblasti. Zde se uplatňují moderní endovaskulární postupy, které jsou poskytovány ve specializovaných centrech. Katetrizační trombolýza (CDT) nebo farmakomechanická CDT jsou bezpečnější a účinnější než systémová trombolytická terapie a jsou slibným prostředkem prevence PTS především po proximální DVT.46 V jedné multicentrické randomizované, kontrolované studii skromného rozsahu (n = 189) bylo použití CDT u pacientů s akutní DVT postihující ilické žíly nebo vena femoralis communis spojeno s 26% snížením rizika vzniku PTS během dvou let sledování, s dodatečnou 3% mírou závažného krvácení.24
Nejlepší současné přístupy k léčbě prokázaného PTS
Kompresní terapie
Kompresní terapie je obecně doporučována. Její efekt se dostavuje především po zmírnění otoků. Velký význam má při léčbě bércové ulcerace.
Farmakoterapie
Byly provedeny čtyři randomizované studie s cílem vyhodnotit účinnost „venoaktivních“ léků na PTS: tři paralelní studie47–49 a jedna křížová studie.59 Celkově jsou však existující důkazy, které podporují použití venoaktivních léků k léčbě PTS, nízké kvality, protože studie byly omezeny vysokou mírou nesrovnalostí a nepřesností.50 Právě nehomogenita jednotlivých studií, malý počet probandů, krátká doba sledování jsou faktory, proč venoaktivní látky nebývají při léčbě PTS ve větší mře doporučovány, ačkoliv je známo, že jsou lidé, kteří při jejich užívání pozitivní efekt vnímají.
Cvičení a životní styl
Dvě malé studie hodnotily účinnost cvičení při léčbě PTS. Ve studii s 30 pacienty s chronickou žilní nedostatečností (polovina z nich měla v anamnéze DVT) vedl šestiměsíční program posilování svalů nohou ke zlepšení funkce a síly lýtkových svalů.51 V kanadské pilotní studii provedené ve dvou centrech vedl šestiměsíční program cvičení zaměřený na posílení a protažení svalů dolních končetin a celkovou kardiovaskulární kondici ke zmírnění závažnosti PTS, zlepšení kvality života, síly a protažení svalů dolních končetin, přičemž nedošlo k žádným nežádoucím účinkům.52 Dostupné informace ukazují, že cvičení může být pro pacienty s PTS prospěšné.
Mezi obecné rady, které jsou relevantní pro všechny pacienty s chronickou žilní nedostatečností, patří: podporovat žilní návrat tím, že se vyhýbáte sedavému životnímu stylu, při sezení si nohy položíte na stoličku nebo při ležení v posteli nohy zvednete; vyhýbat se dlouhodobému vystavení teplu; udržovat zdravou, neobézní tělesnou hmotnost a používat zvlhčující krém, aby se zabránilo vysušení kůže.24
Léčba žilních vředů
U 5–10 % pacientů s DVT se vyvine závažný PTS, který může zahrnovat defekty na nohou. Posttrombotické žilní vředy se léčí kompresivní terapií, která zahrnuje mezioborový přístup. Základem je lokální ošetřování defektů, důsledná, účinná kompresní terapie. Vhodné je doplnění eliminace refluxu v rámci povrchového žilního systému miniinvazivními postupy. Jako základ přetrvává snaha o obnovení žilního návratu a snaha o zprůchodnění obliterovaných končetinových žil, zvláště proximálních.24
Chirurgická nebo endovaskulární léčba PTS
Chirurgické nebo endovaskulární zákroky, jako jsou oprava žilních chlopní, žilní bypass a žilní stenty, k léčbě vhodně vybraných pacientů s PTS mají potenciál snížit výskyt posttrombotických projevů, které lze připsat obstrukci hlubokých žil nebo žilnímu refluxu (VR).53,54 Jejich provedení je indikováno až na základě posouzení konkrétního stavu na specializovaném pracovišti, které se danými postupy zabývá a rutinně je provádí.
Vyskytuje se PTS po DVT horních končetin?
Po DVT horních končetin se u 15 až 25 % pacientů rozvine PTS.55,56 Stejně jako u PTS dolních končetin může PTS horních končetin snížit kvalitu života a funkčnost končetin. Není překvapivé, že PTS dominantní paže je spojen s horší kvalitou života a postižením než PTS nedominantní paže.57 Chybějí údaje, které by sloužily jako vodítko pro léčbu PTS horních končetin. Neexistují žádné studie týkající se kompresních rukávů nebo obvazů k prevenci nebo léčbě PTS horních končetin a není známo, zda trombolýza, endovaskulární nebo chirurgická léčba trombózy v rámci horní končetiny vedou k nižšímu výskytu PTS než standardní antikoagulace samotná.
Vyskytuje se PTS po DVT u dětí?
Incidence PTS u dětí s DVT je uváděna ve výši až 15–25 %.58,59 Neexistují žádné pediatrické studie, které by hodnotily bezpečnost a účinnost terapií k prevenci nebo léčbě PTS.
Závěr
Posttrombotický syndrom je častou komplikací DVT, která může snížit kvalitu života a vést k chronickému funkčnímu postižení. V tomto článku jsme se pokusili poskytnout informace týkající se klíčových aspektů diagnostiky, rizikových faktorů, prevence a léčby PTS. Jak z textu vyplývá, léčba PTS není jednoduchá a v mnoha situacích nemáme jednoznačný doporučený postup. Je nutné vyhodnocovat situaci každého jednotlivce individuálně.
MUDr. Lukáš Hnátek, Ph.D.
AngioCor – Centrum žilních onemocnění, Zlín
E‑mail: hnatek.lukas@gmail.com
Literatura
- Lurie F, Passman M, Meisner M, et al. The 2020 update of the CEAP classification system and reporting standards. J Vasc Surg Venous Lymphat Disord 2020;8:342–352.
- Rabinovich A, Kahn SR. How I treat postthrombotic syndrome. Blood 2009;114:4624–4631.
- Kahn SR, Partsch H, Vedantham S, et al. Definition of post‑thrombotic syndrome of the leg for use in clinical investigations: a recommendation for standardization. J Thromb Haemost 2009;7:879–883.
- Prandoni P, Lensing AWA, Cogo A, et al. The long‑term clinical course of acute deep venous thrombosis. Ann Intern Med 1996;125:1–7.
- Kahn SR, Shrier I, Julian JA, et al. Determinants and time course of the post‑thrombotic syndrome after acute deep venous thrombosis. Ann Intern Med 2008;149:698–707.
- Spencer FA, Emery C, Joffe SW, et al. Incidence rates, clinical profile, and outcomes of patients with venous thromboembolism: The Worcester VTE study. J Thromb 2009;28:401–409.
- Tagalakis V, Patenaude V, Kahn SR, Suissa S. Incidence of and mortality from venous thromboembolism in a real‑world population: the Q‑VTE study cohort. Am J Med 2013;126:832.e813–821.
- Naess IA, Christiansen SC, Romundstad P, et al. Incidence and mortality of venous thrombosis: a population‑based study. J Thromb Haemost 2007;5: 692–699.
- Guanella R, Ducruet T, Johri M, et al. Economic burden and cost determinants of deep vein thrombosis during 2 years following diagnosis: a prospective evaluation. J Thromb Haemost 2011;9:2397–2405.
- MacDougall DA, Feliu AL, Boccuzzi SJ, Lin J. Economic burden of deep‑vein thrombosis, pulmonary embolism, and postthrombotic syndrome. Am J Health Syst Pharm 2006;63:S5–S15.
- Caprini JA, Botteman MF, Stephens JM, et al. Economic burden of long‑term complications of deep vein thrombosis after total hip replacement surgery in the United States. Value Health 2003;6:59–74.
- Bergan JJ, Schmid‑Schonbein GW, Smith PD, et al. Chronic venous disease. N Engl J Med 2006;355:488–498.
- van Korlaar I, Vossen C, Rosendaal F, et al. Quality of life in venous disease. Thromb Haemost 2003;90:27–35.
- Kahn SR, Ducruet T, Lamping DL, et al. Prospective evaluation of health‑related quality of life in patients with deep venous thrombosis. Arch Intern Med 2005;165:1173–1178.
- Broholm R, Sillesen H, Damsgaard MT, et al. Postthrombotic syndrome and quality of life in patients with iliofemoral venous thrombosis treated with catheter‑directed thrombolysis. J Vasc Surg 2011;54(6 Suppl):18S–25S.
- Kahn SR, Shbaklo H, Lamping DL, et al. Determinants of health‑related quality of life during the 2 years following deep vein thrombosis. J Thromb Haemost 2008;6:1105–1112.
- Kahn SR, Ginsberg JS. Relationship between deep venous thrombosis and the postthrombotic syndrome. Arch Int Med 2004;164:17–26.
- Prandoni P, Kahn SR. Post‑thrombotic syndrome: prevalence, prognostication and need for progress. Br J Haematol 2009;145:286–295.
- Kolbach DN, Neumann HA, Prins MH. Definition of the post‑thrombotic syndrome, differences between existing classifications. Eur J Vasc Endovasc Surg 2005;30:404–414.
- Vedantham S. Valvular dysfunction and venous obstruction in the post‑thrombotic syndrome. Thromb Res 2009;123(4 Suppl):S62–S65.
- Bharath V, Kahn SR, Lazo‑Langner A. Genetic polymorphisms of vein wall remodeling in chronic venous disease: a narrative and systematic review. Blood 2014;124:1242–1250.
- Roumen‑Klappe EM, den Heijer M, Janssen MC, et al. The post‑thrombotic syndrome: incidence and prognostic value of non‑invasive venous examinations in a six‑year follow‑up study. Thromb Haemost 2005;94:825–830.
- Villalta S, Bagatella P, Piccioli A, et al. Assessment of validity and reproducibility of a clinical scale for the post thrombotic syndrome. Haemostasis 1994;24(1 Suppl):158a.
- Kahn SR, Galanaud JP, Vedantham S, Ginsberg JS. Guidance for the prevention and treatment of the post‑thrombotic syndrome. J Thromb Thrombolysis 2016;41:144–153. DOI 10.1007/s11239‑015‑1312‑5
- Kahn SR. Measurement properties of the Villalta scale to define and classify the severity of the post‑thrombotic syndrome. J Thromb Haemost 2009;7: 884–888.
- Galanaud JP, Holcroft CA, Rodger MA, et al. Predictors of post‑thrombotic syndrome in a population with a first deep vein thrombosis and no primary venous insufficiency. J Thromb Haemost 2013;11:474–480.
- Bouman AC, Smits JJ, Ten Cate H, Ten Cate‑Hoek AJ. Markers of coagulation, fibrinolysis and inflammation in relation to post‑thrombotic syndrome. J Thromb Haemost 2012;10:1532–1538.
- Rabinovich A, Cohen JM, Prandoni P, Kahn SR. Association between thrombophilia and the post‑thrombotic syndrome: a systematic review and meta‑analysis. J Thromb Haemost 2014;12:14–23.
- van Dongen CJ, Prandoni P, Frulla M, et al. Relation between quality of anticoagulant treatment and the development of the postthrombotic syndrome. J Thromb Haemost 2005;3:939–942.
- Chitsike RS, Rodger MA, Kovacs MJ, et al. Risk of postthrombotic syndrome after subtherapeutic warfarin anticoagulation for a first unprovoked deep vein thrombosis: results from the REVERSE study. J Thromb Haemost 2012;10:2039–2044.
- Roberts LN, Patel RK, Chitongo PB, et al. Presenting D‑dimer and early symptom severity are independent predictors for post‑thrombotic syndrome following a first deep vein thrombosis. Br J Haematol 2013;160:817–824.
- Prandoni P, Frulla M, Sartor D, et al. Vein abnormalities and the post‑thrombotic syndrome. J Thromb Haemost 2005;3:401–402.
- Rabinovich A, Cohen JM, Kahn SR. The predictive value of markers of fibrinolysis and endothelial dysfunction in the post thrombotic syndrome. A systematic review. Thromb Haemost 2014;111:1031–1040.
- Björck F, et al. Direct oral anticoagulants versus vitamin K antagonists and risk of post‑thrombotic syndrome: Systematic review and meta‑analysis. TH Open 2022;6:e147–e156.
- Guo W, et al. Direct oral anticoagulants vs vitamin K antagonists in preventing post‑thrombotic syndrome: A systematic review and network meta‑analysis. J Thromb Thrombolysis 2022;54:12–22.
- Prandoni P, et al. Extended follow‑up of patients with DVT from the RE‑COVER trials: Dabigatran vs warfarin and prevalence of post‑thrombotic syndrome. J Thromb Haemost 2015;13:1951–1961.
- Kakkos SK, et al. Rivaroxaban and the long‑term risk of post‑thrombotic syndrome after DVT – real‑world comparative cohort. Phlebology 2021;36:777–785.
- Ageno W, et al. Edoxaban vs warfarin and long‑term outcomes after venous thromboembolism: Post‑hoc analysis. Thromb Haemost 2020;120:1834–1843.
- Gould MK, Garcia DA, Wren SM, et al. Prevention of VTE in nonorthopedic surgical patients: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence‑Based Clinical Practice Guidelines. Chest 2012;141(2 Suppl):e227S–e277S.
- Falck‑Ytter Y, Francis CW, Johanson NA, et al. Prevention of VTE in orthopedic surgery patients: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence‑Based Clinical Practice Guidelines. Chest 2012;141(2 Suppl):e278S–e325S.
- Kahn SR, Lim W, Dunn AS, et al. Prevention of VTE in Nonsurgical Patients: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence‑Based Clinical Practice Guidelines. Chest 2012;141(2 Suppl):e195S–e226S.
- Kearon C, Akl EA, Comerota AJ, et al. Antithrombotic therapy for VTE disease: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence‑Based Clinical Practice Guidelines. Chest 2012;141(2 Suppl):e419S–e494S.
- Brandjes DPM, Buller HR, Heijboer H, et al. Randomised trial of effect of compression stockings in patients with symptomatic proximal‑vein thrombosis. Lancet 1997;349:759–762.
- Kearon C, Kahn SR, Agnelli G, et al. Antithrombotic therapy for venous thromboembolic disease: ACCP evidence‑based clinical practice guidelines (8th edition). Chest 2008; 133(6 Suppl):454S–545S.
- Kahn SR, Shapiro S, Ducruet T, et al. Graduated compression stockings to treat acute leg pain associated with proximal DVT: A randomised controlled trial. Thromb Haemost 2014;112:1137–1141.
- Watson L, Broderick C, Armon MP. Thrombolysis for acute deep vein thrombosis. Cochrane Database Syst Rev 2016;1:CD002783.
- de Jongste AB, Jonker JJ, Huisman MV, et al. A double blind three center clinical trial on the short‑term efficacy of 0‑(beta‑hydroxyethyl)‑rutosides in patients with postthrombotic syndrome. Thromb Haemost 1989;62:826–829.
- Coccheri S, Andreozzi GM, D’Addato M, Gensini GF.4) Effects of defibrotide in patients with chronic deep insufficiency. The PROVEDIS study. Int Angiol 2004;23:100–107.
- Frulla M, Marchiori A, Sartor D, et al Elastic stockings, hydroxyethylrutosides or both for the treatment of post‑thrombotic syndrome. Thromb Haemost 2005;93:183–185.
- Cohen JM, Akl EA, Kahn SR. Pharmacologic and compression therapies for postthrombotic syndrome: a systematic review of randomized controlled trials. Chest 2012;141:308–320.
- Padberg JR, Johnston MV, Sisto SA. Structured exercise improves calf muscle pump function in chronic venous insufficiency: a randomized trial. J Vasc Surg 2004;39:79–87.
- Kahn SR, Shrier I, Shapiro S, et al. Six‑month exercise training program to treat post‑thrombotic syndrome: a randomized controlled two‑centre trial. CMAJ 2011;183:37–44.
- Neglen P, Hollis KC, Raju S. Combined saphenous ablation and iliac stent placement for complex severe chronic venous disease. J Vasc Surg 2006;44: 828–833.
- Nayak L, Hildebolt CF, Vedantham S. Postthrombotic syndrome: feasibility of a strategy of imaging‑guided endovascular intervention. J Vasc Interv Radiol 2012;23:1165–1173.
- Elman ER, Kahn SR. The post‑thrombotic syndrome after upper extremity deep venous thrombosis: a systematic review. Thromb Res 2006;117:609–614.
- Prandoni P, Bernardi E, Marchiori A, et al. The long term clinical course of acute deep vein thrombosis of the arm: prospective cohort study. BMJ 2004;329:484–485.
- Kahn SR, Elman EA, Bornais C, et al. Post‑thrombotic syndrome, functional disability and quality of life after upper extremity deep venous thrombosis in adults. Thromb Haemost 2005;93:499–502.
- Goldenberg NA, Donadini MP, Kahn SR, et al. Postthrombotic syndrome in children: a systematic review of frequency of occurrence, validity of outcome measures, and prognostic factors. Haematologica 2010;95:1952–1959.
- Monagle P, Chan AK, Goldenberg NA, et al. Antithrombotic therapy in neonates and children: antithrombotic therapy and prevention of thrombosis, 9th ed: American College of Chest Physicians Evidence‑Based Clinical Practice Guidelines. Chest 2012;141(2 Suppl):e737S–e801S.