Sortis u rizikových pacientů: kdy volit vyšší dávku atorvastatinu?
Atorvastatin patří mezi nejčastěji předepisované statiny v primární i sekundární prevenci kardiovaskulárních (KV) onemocnění. U rizikových pacientů je volba optimální dávky klíčová k dosažení doporučených cílových hodnot LDL cholesterolu (LDL‑C) a pro minimalizaci reziduálního KV rizika. Tento článek shrnuje současné poznatky a doporučení týkající se indikací k použití vyšších dávek atorvastatinu (40–80 mg) u pacientů s vysokým a velmi vysokým KV rizikem.
Kdo jsou „rizikoví pacienti“?
 Pacienti s vysokým a velmi vysokým KV rizikem (tab. 1) vykazují výrazně zvýšenou pravděpodobnost vzniku závažných KV příhod v horizontu deseti let. Do skupiny velmi vysokého rizika řadíme
Pacienti s vysokým a velmi vysokým KV rizikem (tab. 1) vykazují výrazně zvýšenou pravděpodobnost vzniku závažných KV příhod v horizontu deseti let. Do skupiny velmi vysokého rizika řadíme
osoby s prokázaným aterosklerotickým KV onemocněním, jako je ischemická choroba srdeční (ICHS), cévní mozková příhoda (CMP) nebo periferní arteriální onemocnění. Mezi velmi rizikové pacienty dále patří diabetici s orgánovým postižením, dlouhodobě nemocní diabetici 1. typu s trváním onemocnění nad 20 let, pacienti s pokročilým chronickým onemocněním ledvin (odhadovaná glomerulární filtrace [eGFR] < 30 ml/min/1,73 m²) nebo osoby s odhadovaným rizikem podle skórovacích systémů SCORE2 > 10 %.1
Skupinu vysokého rizika tvoří pacienti s výrazně zvýšeným jednotlivým rizikovým faktorem, jako je těžká hypertenze či velmi vysoká koncentrace LDL‑C, diabetici bez orgánového postižení, ale s dalšími rizikovými faktory nebo delším trváním onemocnění a osoby se středně sníženou funkcí ledvin (eGFR 30–59 ml/min/1,73 m²). Pro tuto skupinu platí odhad rizika SCORE2 v rozmezí 5–10 %.1
Individualizace dávkování statinů dle rizikového profilu
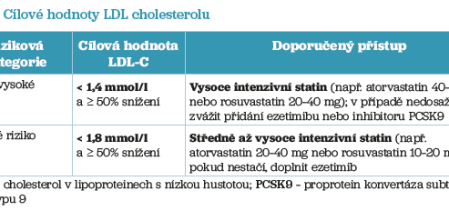
Volba intenzity hypolipidemické léčby by měla být přizpůsobena celkovému KV riziku pacienta a stanovenému cíli v podobě
hodnoty LDL‑C (tab. 2). U velmi rizikových pacientů se doporučuje cílová koncentrace LDL‑C pod 1,4 mmol/l a snížení o minimálně 50 % oproti výchozím hodnotám. Pro tyto pacienty je indikována vysoce intenzivní statinová terapie, nejčastěji atorvastatinem v dávce 40–80 mg nebo rosuvastatinem 20–40 mg denně.1
Pacienti s vysokým KV rizikem mají cílovou hodnotu LDL‑C < 1,8 mmol/l, jíž je obvykle dosaženo středně intenzivní dávkou atorvastatinu (20–40 mg) nebo rosuvastatinu (10–20 mg). Pokud monoterapie statinem nestačí, doporučuje se přidání ezetimibu nebo inhibitoru PCSK9 (inhibitor proprotein konvertázy subtilisin/kexin typu 9).1,2
Evidence pro použití vyšších dávek atorvastatinu
Velké klinické studie jednoznačně prokázaly, že vyšší dávky atorvastatinu prokazatelně snižují riziko výskytu KV příhod oproti nižším dávkám:
- Studie TNT (Treating to New Targets) porovnala atorvastatin v dávkách 10 mg a 80 mg u pacientů se stabilní ICHS. Vyšší dávka vedla ke snížení rizika výskytu KV příhod o 22 % (poměr rizik [HR] 0,78; p < 0,001).3
- Studie PROVE‑IT TIMI 22 ukázala, že intenzivní terapie atorvastatinem 80 mg po akutním koronárním syndromu (AKS) byla účinnější než léčba pravastatinem 40 mg s výraznějším snížením hodnoty LDL‑C (1,6 mmol/l vs. 2,5 mmol/l) a nižším počtem KV příhod.4
- Metaanalýzy potvrdily, že každé snížení hodnoty LDL‑C o 1 mmol/l je spojeno s přibližně 22% snížením rizika výskytu KV událostí.5
Kombinace atorvastatinu s ezetimibem
Kombinace atorvastatinu s ezetimibem představuje významný terapeutický krok u pacientů, kteří monoterapií statinem nedosahují cílových hodnot LDL‑C. Ezetimib selektivně inhibuje střevní absorpci cholesterolu blokádou transportéru NPC1L1, čímž doplňuje účinek statinu, který blokuje endogenní syntézu cholesterolu.2
Přidání ezetimibu ke statinu snižuje hodnotu LDL‑C o dalších 20–25 % oproti samotnému statinu.2 Studie IMPROVE‑IT demonstrovala, že tato kombinace vedla nejen k výraznějšímu poklesu hodnoty LDL‑C, ale i k dalšímu snížení výskytu závažných KV příhod. 2 Kombinace atorvastatinu a ezetimibu je obecně dobře tolerována.
Algoritmus dosažení cílových hodnot LDL cholesterolu
Podle doporučení ESC/EAS (Evropská kardiologická společnost / Evropská společnost pro aterosklerózu) (2019, aktualizace 2023) by léčba měla postupovat takto:1
- Zahájení intenzivní statinové terapie: atorvastatin 40–80 mg nebo rosuvastatin 20–40 mg denně s cílem snížit hodnotu LDL‑C o ≥ 50 %.
- Kontrola hodnoty LDL‑C po 4–6 týdnech: pokud není dosaženo cíle (< 1,4 mmol/l nebo < 1,0 mmol/l po opakované příhodě), přechod na další krok.
- Přidání ezetimibu 10 mg denně: kombinace se statinem sníží hodnotu LDL‑C o dalších 20–25 %. Vhodné i při intoleranci vysoké dávky statinu.
- Přidání inhibitoru PCSK9 (evolokumab, alirokumab): pokud i po přidání ezetimibu není cíle dosaženo, je možné pokračovat přidáním inhibitorů PCSK9, které snižují hodnotu LDL‑C o dalších 50–60 % a prokazatelně snižují výskyt KV příhod.6,7
Nové možnosti zahrnují inklisiran (siRNA proti PCSK9) a kyselinu bempedoovou, které představují zajímavé alternativy pro pacienty s intolerancí statinů nebo nedostatečnou odpovědí na léčbu.8,9
Tolerance vyšších dávek atorvastatinu a praktické úvahy
Obavy z nežádoucích účinků, zejména svalových obtíží (myopatií), bývají častým důvodem, proč lékaři váhají s nasazením vyšších dávek statinu. Nicméně data z klinických studií i běžné praxe ukazují, že atorvastatin v dávce 80 mg je většinou dobře tolerován. Výskyt myalgií je mírně vyšší ve srovnání s nižšími dávkami, ale závažná myopatie či rhabdomyolýza jsou vzácné (< 0,1 %).10
Je důležité pacienty na možné obtíže upozornit a aktivně se jich při kontrolách dotazovat. Pokud se svalové bolesti objeví, lze provést základní laboratorní vyšetření (CK, jaterní testy) a podle nálezů upravit postup. Při intoleranci lze zvažovat modifikaci dávkování, například 40 mg obden, nebo přidání ezetimibu ke střední dávce statinu. Individualizovaný přístup je vždy klíčový, aby léčba byla efektivní i bezpečná.
Kazuistika z klinické praxe
58letý muž, obézní (index tělesné hmotnosti [BMI] 29 kg/m2), kuřák s anamnézou ICHS (stav po NSTEMI před 2 lety), diabetu 2. typu na léčbě perorálními antidiabetiky (PAD) a arteriální hypertenzí. Při vstupním vyšetření byla hodnota LDL‑C 3,2 mmol/l, triglyceridů 2,1 mmol/l, glykovaného hemoglobinu (HbA1c) 58 mmol/mol a eGFR 65 ml/min/1,73 m². Pacient užíval kyselinu acetylsalicylovou (ASA) 100 mg, atorvastatin 20 mg, ramipril 5 mg a metformin 2 g denně.
Vzhledem k anamnéze infarktu myokardu a diabetu byl hodnocen jako velmi rizikový, s cílovou hodnotou LDL‑C < 1,4 mmol/l a nutností poklesu stávající hodnoty LDL‑C o ≥ 50 %. Proto byla dávka atorvastatinu navýšena na 80 mg denně. Při kontrole po šesti týdnech došlo k poklesu hodnoty LDL‑C na 1,7 mmol/l (−47 %), tedy stále nad cílovou hodnotou. Do léčby byl proto přidán ezetimib 10 mg denně. Po dalších šesti týdnech dosáhl pacient hodnoty LDL‑C 1,2 mmol/l, čímž byl cíl splněn. Při následném sledování po šesti měsících byly hodnoty stabilní, pacient byl bez svalových obtíží, a navíc se mírně zlepšila kompenzace diabetu díky dodržování dietních opatření.
Tento příklad ukazuje, že intenzivní statinová terapie je u velmi rizikových pacientů nezbytným prvním krokem a v případě nedosažení cíle je vhodné bez zbytečného odkladu přidat do medikace ezetimib. Pravidelné kontroly lipidového profilu a tolerance léčby jsou zásadní součástí dlouhodobé péče.
Závěr
U pacientů s vysokým a velmi vysokým KV rizikem by měla být intenzivní statinová léčba standardem péče. Volba vyšší dávky atorvastatinu (40–80 mg) je indikována u pacientů, kteří vyžadují výrazné snížení hodnoty LDL‑C pro prevenci KV příhod. Kombinace s ezetimibem a případně inhibitory PCSK9 umožňuje efektivně dosáhnout přísnějších lipidových cílů a snížit tak KV morbiditu i mortalitu. Klinická rozhodnutí musejí být individualizována podle rizikového profilu, lipidových parametrů a preferencí pacienta.
MUDr. Vlastimil Černíček
Kardiologické oddělení, Krajská nemocnice T. Bati, Zlín
E‑mail: v.cernicek@seznam.cz
Literatura
- Mach F, Baigent C, Catapano AL, et al. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J 2020;41:111–188.
- Cannon CP, Blazing MA, Giugliano RP, et al. Ezetimibe added to statin therapy after acute coronary syndromes. N Engl J Med 2015;372:2387–2397.
- LaRosa JC, Grundy SM, Waters DD, et al. Intensive lipid lowering with atorvastatin in patients with stable coronary disease. N Engl J Med 2005;352:1425–1435.
- Cannon CP, Braunwald E, McCabe CH, et al. Intensive versus moderate lipid lowering with statins after acute coronary syndromes. N Engl J Med 2004;350:1495–1504.
- Cholesterol Treatment Trialists’ Collaboration. Efficacy and safety of more intensive lowering of LDL cholesterol: meta‑analysis of individual data. Lancet 2010;376:1670–1681.
- Sabatine MS, Giugliano RP, Keech AC, et al. Evolocumab and clinical outcomes in patients with cardiovascular disease. N Engl J Med 2017;376:1713–1722.
- Schwartz GG, Steg PG, Szarek M, et al. Alirocumab and cardiovascular outcomes after acute coronary syndrome. N Engl J Med 2018;379:2097–2107.
- Ray KK, Wright RS, Kallend D, et al. Two phase 3 trials of inclisiran in patients with elevated LDL cholesterol. N Engl J Med 2020;382:1507–1519.
- Nissen SE, Lincoff AM, Brennan D, et al. Bempedoic acid and cardiovascular outcomes in statin‑intolerant patients. N Engl J Med 2023;388:1353–1364.
- Stroes ES, Thompson PD, Corsini A, et al. Statin‑associated muscle symptoms: impact on statin therapy—European Atherosclerosis Society consensus panel statement on assessment, aetiology and management. Eur Heart J 2015;36:1012–1022.