Vinpocetin – nejenom neuroprotektivum
Vinpocetin (chemický název: ethylapovinkaminát) je polosyntetický derivát vinkaminu, alkaloidu přirozeně se vyskytujícího v rostlině barvínek menší (Vinca minor). Poprvé jej syntetizoval v roce 1975 maďarský chemik Csaba Szántay, přičemž průmyslová výroba vinpocetinu byla zahájena o tři roky později. Vinpocetin vykazuje schopnost zlepšovat cerebrální průtok krve a zároveň působí neuroprotektivně. V zemích střední a východní Evropy je již po několik desetiletí úspěšně využíván v léčbě cerebrovaskulárních poruch, poruch paměti souvisejících s věkem, tinnitu, vertiga a dalších stavů s obdobnou patofyziologií.
Úvod
Vinpocetin (14‑ethoxykarbonyl‑(3a,16a‑ethyl)‑14,15‑eburnamin) je léčivá látka odvozená od vinkaminu, alkaloidu získávaného z rostliny barvínek menší (Vinca minor), která se přirozeně vyskytuje na vlhkých, živinami bohatých stanovištích. Díky své schopnosti snadno pronikat hematoencefalickou bariérou se vinpocetin uplatňuje v léčbě a prevenci různých neurologických a psychiatrických poruch, zejména cévních mozkových příhod (CMP), poruch paměti a demencí. Jeho mechanismus účinku zahrnuje zlepšení cerebrální mikrocirkulace, zvýšení využití glukózy a kyslíku v mozkové tkáni a modulaci neurotransmiterových systémů. Vinpocetin byl vyvinut v Maďarsku koncem 70. let 20. století a pod obchodním názvem Cavinton se postupně rozšířil do terapeutického užívání v mnoha zemích světa. Třebaže nejčastěji je ve svém využití skloňován primárně jako nootropikum, nezřídka se s ním setkáváme v jiných indikacích, včetně senzorických poruch, vaskulárních onemocnění, vertiga, tinnitu či bolestí hlavy.
Stručně k farmakologii
Obvyklý režim dávkování spočívá v užití 5 až 10 mg vinpocetinu perorálně 3× denně, z důvodu relativně krátkého biologického poločasu (1 až 2 hodiny).1,2 Po užití se vinpocetin snadno vstřebává z gastrointestinálního traktu3 a rovněž dobře proniká přes hematoencefalickou bariéru4. Vrcholových plazmatických koncentrací je dosahováno již přibližně za 1 hodinu.2,5 Distribuční objem (Vd) má hodnotu 3,2 ± 0,9 l/kg, což odráží jeho vysokou distribuci ve tkáni.1 Vinpocetin je rychle a rozsáhle metabolizován především na svůj deesterifikovaný derivát – kyselinu apovinkaminovou – a další minoritní metabolity. Celková plazmatická clearance vinpocetinu je 0,88 ± 0,20 l/h/kg.3 Obecně platí, že v terapeutických dávkách má vinpocetin lineární farmakokinetiku, respektive nedochází k akumulaci léčiva.2
Mechanismus účinku vinpocetinu je komplexní a lze jej charakterizovat jako pleiotropní, tedy zahrnující více farmakologických cílů a účinků. Jedním z hlavních mechanismů je inhibice fosfodiesterázy typu 1 (PDE‑1), enzymu zodpovědného za rozklad cyklických nukleotidů cAMP (cyklický adenosinmonofosfát) a cGMP (cyklický guanosinmonofosfát). Vinpocetin vykazuje vyšší afinitu k podtypům PDE‑1A a PDE‑1B než k PDE‑1C, což vede k potlačení vazokonstrikce, omezení kardiovaskulární remodelace a ke zlepšení neuronální signalizace.
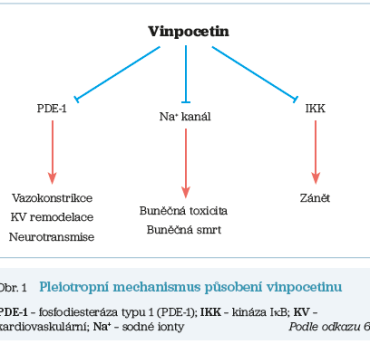 Dalším významným účinkem je blokáda napěťově řízených sodíkových kanálů (Na+), přičemž hodnota IC50 se pohybuje v rozmezí 10–50 μM. Tato inhibice přispívá ke snížení buněčné excitability a zátěže, čímž se snižuje riziko apoptózy. Vinpocetin rovněž inhibuje kinázu IκB (IKK), klíčový enzym v regulaci zánětlivé odpovědi prostřednictvím signální dráhy nukleárního faktoru kappa B (NF‑κB). Hodnota IC50 pro tento účinek je přibližně 17 μM, což naznačuje potenciál vinpocetinu jako modulátoru neurozánětlivých procesů (obr. 1).6
Dalším významným účinkem je blokáda napěťově řízených sodíkových kanálů (Na+), přičemž hodnota IC50 se pohybuje v rozmezí 10–50 μM. Tato inhibice přispívá ke snížení buněčné excitability a zátěže, čímž se snižuje riziko apoptózy. Vinpocetin rovněž inhibuje kinázu IκB (IKK), klíčový enzym v regulaci zánětlivé odpovědi prostřednictvím signální dráhy nukleárního faktoru kappa B (NF‑κB). Hodnota IC50 pro tento účinek je přibližně 17 μM, což naznačuje potenciál vinpocetinu jako modulátoru neurozánětlivých procesů (obr. 1).6
Celkově lze vinpocetin považovat za multifunkční molekulu s neuroprotektivními, vazodilatačními a protizánětlivými vlastnostmi, které jsou relevantní pro jeho využití v terapii neurologických onemocnění.
Vinpocetin a nervový systém
Vinpocetin byl původně vyvinut jako léčivo určené k terapii neurologických onemocnění spojených s poruchami mozkové cirkulace, zejména CMP a demencí. V obou případech hraje klíčovou roli mozková ischemie, což vysvětluje opakovaně potvrzovaný přínos vinpocetinu u stavů charakterizovaných nedostatečným prokrvením mozku, a to jak v preklinických7, tak i v klinických studiích8,9.
Od svého uvedení do klinické praxe se vinpocetin osvědčil i u dalších neurodegenerativních onemocnění, jako je Parkinsonova choroba, Huntingtonova choroba či Alzheimerova demence. V mozku působí jako cerebrální vazodilatátor, čímž zlepšuje průtok krve, a zároveň podporuje mozkový metabolismus prostřednictvím zvýšeného příjmu a využití kyslíku a glukózy, včetně stimulace produkce adenosintrifosfátu (ATP) v neuronech. V některých neuronových populacích a nervových zakončeních byl navíc prokázán jeho antioxidační účinek, který přispívá k ochraně před neurotoxicitou vápníku a sodíku.6
Farmakodynamické účinky vinpocetinu byly hodnoceny v rámci dvojitě zaslepené studie s použitím pozitronové emisní tomografie (PET) u pacientů s chronickou ischemickou CMP (n = 13), kterým byl vinpocetin podáván intravenózně po dobu 14 dnů. Studie sledovala změny regionálního a globálního cerebrálního průtoku krve (CBF) a metabolického obratu glukózy (CMRglc) spolu s dalšími fyziologickými a klinickými parametry. Zatímco globální CMRglc se výrazně nezměnil, globální CBF se zvýšil a regionální hodnoty CMRglc i CBF vykazovaly významné změny, přičemž nejvýraznější byly zaznamenány u pacientů léčených vinpocetinem. Největší zvýšení regionálního průtoku krve bylo pozorováno v thalamu a nucleus caudatus (o 36 a 37 %), což odpovídá oblastem s nejvyšší absorpcí značeného vinpocetinu v jiných PET studiích. Výsledky naznačují, že dvoutýdenní intravenózní podávání vinpocetinu může účinně přispět k redistribuci mozkového průtoku krve u pacientů s chronickou ischemickou CMP.10
Souhrnně lze konstatovat, že vinpocetin vykazuje neuroprotektivní účinky, které jsou výsledkem kombinace jeho vazodilatačního působení na cévy a přímého ovlivnění neuronálních a gliových buněk. Protektivní účinky vinpocetinu se projevují nejen v mozku, ale i v dalších orgánech postižených ischemickým procesem, včetně sítnice11, jater12, ledvin13 a kůže14.
Protizánětlivé vlastnosti vinpocetinu
Ačkoliv vinpocetin se svým mechanismem účinku výrazně odlišuje od klasických nesteroidních antiflogistik, jež působí inhibicí cyklooxygenázy, jeho protizánětlivé vlastnosti jsou dnes již dobře dokumentovány. Tyto účinky se projevují na úrovni různých buněčných typů, včetně endoteliálních buněk, buněk hladké svaloviny cév, monocytů, makrofágů, neutrofilů, epiteliálních buněk, mikroglie a dendritických buněk.15–17
Protizánětlivý efekt vinpocetinu je zprostředkován přímou inhibicí kinázy IκB (IKK), což vede ke stabilizaci komplexu IκB–NF‑κB a k následnému potlačení transkripce genů kódujících zánětlivé mediátory. Tím dochází k omezení aktivace NF‑κB signální dráhy, která hraje klíčovou roli v regulaci imunitní odpovědi a produkci prozánětlivých cytokinů.
Indikace
Aktuálně je v České republice vinpocetin dostupný ve formě tablet a koncentrátu pro infuzní roztok. Tablety jsou určeny k symptomatické léčbě cerebrovaskulárních poruch různého původu, jako jsou ischemická hypoperfuze, různé formy ischemických hypoperfuzních stavů, vaskulární demence. Využity mohou být rovněž ke snížení psychických a neurologických následků poruchy prokrvení mozku.
V infuzi je vinpocetin určen pro dospělé a adolescenty k léčbě následků cirkulačních poruch centrálního nervového systému (CNS). Používá se k léčbě psychických i neurologických příznaků oběhových poruch CNS (poruch paměti, afázie, apraxie, motorických poruch, závrati, bolestí hlavy atd.). V infuzi je indikován při všech formách akutní i chronické insuficience mozkových cév, jako např. při tranzitorních ischemických příhodách, přechodných ischemických neurologických poruchách, progresivním iktu, kompletním iktu, při postapoplektických stavech, při multiinfarktové demenci, při cerebrální arterioskleróze, při posttraumatických stavech, hypertenzní encefalopatii aj.
V oftalmologii lze vinpocetin infuzně podat k léčbě vaskulárních poruch choroidey a sítnice vyvolaných arteriosklerózou anebo cévním spasmem, pro léčení degenerace makuly a sekundárního glaukomu vyvolaného parciálními trombózami a cévními uzávěry.
V otologii je vinpocetin v infuzi indikován k léčbě sluchových poruch vaskulárního anebo toxického (iatrogenního) původu, senzorineurální ztráty sluchu a závratě labyrintového původu.
Dávkování
Tabletové formy (5 nebo 10 mg) se obvykle užívají po jídle, a to 3krát denně. Při nutnosti intravenózní léčby je jako iniciální dávka doporučováno 20–30 mg vinpocetinu denně. V případě potřeby je možné denní dávku postupně zvyšovat až na 1 mg/kg tělesné hmotnosti, podle tolerance pacienta, a rozděleně do tří dávek s intervalem 5–6 hodin.
Klinické zkušenosti
Z perspektivy běžné klinické praxe je důležité, že popsaný protizánětlivý účinek vinpocetinu byl popsán i v multicentrické studii zahrnující 60 nemocných s okluzí v přední části Willisova okruhu a rozvíjejícím se iktem mozkové cirkulace a s nástupem mrtvice.18 Pacienti léčení vinpocetinem měli nejen lepší obnovu neurologických funkcí a zlepšené klinické výsledky, ale též sníženou aktivaci signalizace NF‑kB a expresi prozánětlivých mediátorů. Přínos takovéto léčby je možné logicky očekávat i u stavů spojených s kognitivním deficitem navozeným zánětem či infekcí, včetně dnes mediálně vděčného onemocnění covid‑19 či u postcovidového syndromu.19
Účinky vinpocetinu byly rovněž testovány u pacientů s Parkinsonovou chorobou. Do této studie bylo přijato 89 pacientů s Parkinsonovou chorobou a 42 zdravých kontrol. Všichni pacienti byli náhodně zařazeni buď do skupiny s tradiční terapií (n = 46), nebo do skupiny s vinpocetinem (n = 43), zaslepeným způsobem. Obě léčby byly podávány po dobu 14 dnů. Podávání vinpocetinu snížilo hodnoty mRNA toll‑like receptorů TLR2/4, stejně jako proteinové koncentrace navazujících signálních molekul, MyD88 a NF‑kappaB; navíc snížilo hodnoty exprese zánětlivých cytokinů v séru, tumor nekrotizujícího faktoru alfa (TNFα) a monocytového chemotaktického proteinu 1 (MCP‑1). Vinpocetin naopak zvýšil hodnoty mRNA TLR3 (toll‑like receptory), stejně jako koncentrace proteinů navazujících signálních molekul TRIF‑β a IRF‑3 a sérové koncentrace protizánětlivých cytokinů – interleukinu (IL) 10 a IL‑8. Autoři studie se domnívají, že zaznamenaný vliv na TLR, které jsou zapojeny do geneze zánětu, se může příznivě promítnout do patogeneze onemocnění, včetně pozitivního vlivu na kognitivní funkce.20
Relativně nedávno bylo zjištěno, že vinpocetin působí synergicky s dexamethasonem u onkologických pacientů trpících kognitivní poruchou.21 Na druhou stranu ve dvojitě zaslepené, randomizované klinické studii nebyly u zdravých dobrovolníků nebo pacientů s epilepsií pozorovány žádné významné kognitivní přínosy pro kognici.22
Recentně publikované přehledové práce popisují roli vinpocetinu v léčbě ischemické CMP a jeho účinky na stav nemocných po prodělané příhodě.23,24 V jedné menší klinické studii příznivě působil na zlepšení sluchu u pacientů s jeho senzorineurálně podmíněnou ztrátou.25
Přímé klinické studie cíleně hodnotící účinnost vinpocetinu při léčbě bolestí hlavy bohužel postrádáme. Přesto jeho příznivý vliv na cerebrální hemodynamiku a neurozánětlivé procesy vedl k úvahám o možném využití tohoto přípravku i u stavů s podobnými patofyziologickými mechanismy. Ve výše zmíněné metaanalýze randomizovaných kontrolovaných studií u pacientů s akutní ischemickou CMP vinpocetin významně snížil míru postižení a zlepšil kognitivní funkce.24 Vzhledem k překryvu vaskulárních a zánětlivých drah mezi CMP a migrénou tyto výsledky poskytují racionální základ pro další výzkum.
Navíc některé kazuistiky a menší observační studie naznačují, že vinpocetin může zmírňovat příznaky bolesti hlavy u pacientů s chronickou cerebrovaskulární insuficiencí nebo u bolestí hlavy po prodělané CMP, ačkoli robustní klinická data zatím chybějí.26
Analogické zkušenosti se týkají i tinnitu. Animální modely tinnitu, indukovaného podáním salicylátu nebo akustickým traumatem, prokázaly zvýšené hodnoty prozánětlivých cytokinů TNFα a IL‑1β v oblasti sluchové kůry a mozkového kmene. Farmakologická blokáda TNFα v těchto modelech vedla k prevenci rozvoje chování odpovídajícího tinnitu a k obnově normální synaptické funkce. Vzhledem k tomu, že vinpocetin prokazatelně potlačuje expresi TNFα a aktivaci mikroglie, lze předpokládat, že může mít obdobné protektivní účinky i v rámci sluchového systému.27,28 V kontextu výše popsaného mechanismu účinku vinpocetinu by tento mohl být zvláště přínosný u pacientů, jejichž tinnitus souvisí s neurozánětlivými nebo vaskulárními příčinami.
Vinpocetin je v klinické praxi využíván též u pacientů s vertigem vaskulárního původu, chronickým pocitem závratě či vestibulárními příznaky po CMP. V těchto případech může vinpocetin podpořit centrální kompenzační mechanismy a zlepšit cerebrální perfuzi, což může přispět ke zmírnění vertiginózních symptomů.29 Díky příznivému bezpečnostnímu profilu a minimálním sedativním účinkům představuje vinpocetin vhodnou alternativu nebo doplněk ke konvenčním vestibulárním supresivům, zejména u starších pacientů nebo u osob s polyfarmakoterapií, kde je třeba minimalizovat riziko lékových interakcí a nežádoucích účinků. Rozsáhlejší klinické studie v této oblasti nicméně scházejí.
Bezpečnostní aspekty léčby
Vinpocetin je obecně dobře snášen, včetně starší populace, s nízkým výskytem nežádoucích účinků. Mezi časté nežádoucí účinky patří gastrointestinální poruchy a bolesti hlavy; závažné nežádoucí účinky jsou vzácné.
Vinpocetin vykazoval slabý inhibiční účinek na CYP2C9, kde hodnota inhibiční koncentrace IC50 je 68,96 μM, zatímco hodnoty IC50 pro CYP3A4, CYP2C19, CYP2D6 a CYP2E1 byly v rozmezí 100 μM, což ukázalo, že vinpocetin neměl žádné zjevné inhibiční účinky na tyto cytochromy.30
Kontraindikace
Kontraindikací pro terapeutické využití vinpocetinu je kromě známé přecitlivělosti na kteroukoliv z obsažených látek konkrétního léčivého přípravku přítomnost akutní fáze hemoragického iktu, závažné arytmie, krvácivých stavů či těžké formy ischemické choroby srdeční. Kontraindikován je rovněž u těhotných a kojících žen.
Závěr
Výše popsané postřehy jasně dokládají pestrou paletu účinků vinpocetinu ve vztahu k nervovému systému. Současně však přibývají i doklady o jeho kladném vlivu na kardiální, respektive kardiovaskulární funkce. Vinpocetin tak nemá jediný unikátní cíl, působí pleiotropně.
Jeho vícečetný účinek, včetně vazodilatace, antioxidace, protizánětlivého působení, antitrombotických vlastností a antiremodelace, působí terapeuticky synergicky, čímž pokrývá multifaktoriálně podmíněná cerebrovaskulární a kardiovaskulární onemocnění.
Vinpocetin může být vhodnou volbou pro pacienty s akutní nebo chronickou ischemickou cévní mozkovou příhodou, kteří potřebují zlepšit cerebrální perfuzi a metabolismus, zejména pak v případě zhoršené schopnosti se koncentrovat, eventuálně při doprovodném narušení kognitivních funkcí.
Doc. MUDr. Jiří Slíva, Ph.D., MBA
Ústav farmakologie, 3. LF UK, Praha
E‑mail: jiri.sliva@lf3.cuni.cz
Literatura
- Miskolczi P, Vereczkey L, Szalay L, Göndöc C. Effect of age on the pharmacokinetics of vinpocetine (Cavinton) and apovincaminic acid. Eur J Clin Pharmacol 1987;33:185–189.
- Miskolczi P, Kozma K, Polgár M, Vereczkey L. Pharmacokinetics of vinpocetine and its main metabolite apovincaminic acid before and after the chronic oral administration of vinpocetine to humans. Eur J Drug Metab Pharmacokinet 1990;15:1–5.
- Vereczkey L. Pharmacokinetics and metabolism of vincamine and related compounds. Eur J Drug Metab Pharmacokinet 1985;10:89–103.
- Polgár M, Vereczkey L, Nyáry I. Pharmacokinetics of vinpocetine and its metabolite, apovincaminic acid, in plasma and cerebrospinal fluid after intravenous infusion. J Pharm Biomed Anal 1985;3:131–139.
- Lohmann A, Dingler E, Sommer W, et al. Bioavailability of vinpocetine and interference of the time of application with food intake. Arzneimittelforschung 1992;42:914–917.
- Zhang YS, Li JD, Yan C. An update on vinpocetine: New discoveries and clinical implications. Eur J Pharmacol 2018;819:30–34.
- Jincai W, Tingfang D, Yongheng Z. Effects of vinpocetine and ozagrel on behavioral recovery of rats after global brain ischemia. J Clin Neurosci 2014;21:661–663.
- Zhang W, Huang Y, Li Y, et al. Efficacy and Safety of Vinpocetine as Part of Treatment for Acute Cerebral Infarction: A Randomized, Open‑Label, Controlled, Multicenter CAVIN (Chinese Assessment for Vinpocetine in Neurology) Trial. Clin Drug Investig 2016;36:697–704.
- Bönöczk P, Panczel G, Nagy Z. Vinpocetine increases cerebral blood flow and oxygenation in stroke patients: a near infrared spectroscopy and transcranial Doppler study. Eur J Ultrasound 2002;15:85–91.
- Szilágyi G, Nagy Z, Balkay L et al. Effects of vinpocetine on the redistribution of cerebral blood flow and glucose metabolism in chronic ischemic stroke patients: a PET study. J Neurol Sci 2005;229‑230:275–284.
- Nivison‑Smith L, Khoo P, Acosta ML, Kalloniatis M. Pre‑treatment with vinpocetine protects against retinal ischemia. Exp Eye Res 2017;154:126–138.
- Zaki HF, Abdelsalam RM. Vinpocetine protects liver against ischemia‑reperfusion injury. Can J Physiol Pharmacol 2013;91:1064–1070.
- Fattori V, Borghi SM, Guazelli CFS, et al. Vinpocetine reduces diclofenac‑induced acute kidney injury through inhibition of oxidative stress, apoptosis, cytokine production, and NF‑κB activation in mice. Pharmacol Res 2017;120:10–22.
- Xiao‑Xiao T, Sen‑Min W, Ding‑Sheng L. Effects of vinpocetine on random skin flap survival in rats. J Reconstr Microsurg 2013;29:393–398.
- Jeon KI, Xu X, Aizawa T. Vinpocetine inhibits NF‑kappaB‑dependent inflammation via an IKK‑dependent but PDE‑independent mechanism. Proc Natl Acad Sci U S A 2010;107:9795–9800.
- Ruiz‑Miyazawa KW, Pinho‑Ribeiro FA, Zarpelon AC, et al. Vinpocetine reduces lipopolysaccharide‑induced inflammatory pain and neutrophil recruitment in mice by targeting oxidative stress, cytokines and NF‑κB. Chem Biol Interact 2015;237:9–17.
- Feng X, Wang Y, Hao Y, et al. Vinpocetine Inhibited the CpG Oligodeoxynucleotide‑induced Immune Response in Plasmacytoid Dendritic Cells. Immunol Invest 2017;46:263–273.
- Zhang F, Yan C, Wei C, et al. Vinpocetine Inhibits NF‑κB‑Dependent Inflammation in Acute Ischemic Stroke Patients. Transl Stroke Res 2018;9:174–184.
- Golovacheva VA, Tabeeva GR, Kuznetsov IV. Cognitive impairment in COVID‑19: associations, pathogenesis and treatment questions. Neurology Neuropsychiatry Psychosomatics 2021;13:123–129.
- Ping Z, Xiaomu W, Xufang X, Liang S. Vinpocetine regulates levels of circulating TLRs in Parkinson‘s disease patients. Neurol Sci 2019;40:113–120.
- Zhang P, Cao Y, Chen S, Shao L. Combination of Vinpocetine and Dexamethasone Alleviates Cognitive Impairment in Nasopharyngeal Carcinoma Patients following Radiation Injury. Pharmacology 2021;106:37–44.
- Meador KJ, Leeman‑Markowski B, Medina AE, et al. Vinpocetine, cognition, and epilepsy. Epilepsy Behav 2021;119:107988.
- Al‑Kuraishy HM, Al‑Gareeb AI, Naji MT, Al‑Mamorry F. Role of vinpocetine in ischemic stroke and poststroke outcomes: A critical review. Brain Circ 2020;6:1–10.
- Panda PK, Ramachandran A, Panda P, Sharawat IK. Safety and Efficacy of Vinpocetine as a Neuroprotective Agent in Acute Ischemic Stroke: A Systematic Review and Meta‑Analysis. Neurocrit Care 2022;37:314–325.
- Gutiérrez‑Farfán I, Reyes‑Legorreta C, Solís‑Olguín M, et al. Evaluation of vinpocetine as a therapy in patients with sensorineural hearing loss: A phase II, open‑label, single‑center study. J Pharmacol Sci 2021;145:313–318.
- Medvedeva LA, Gnezdilov AV, Zagorul‘ko OI et al. Efficacy of neuroprotectors in patients with tension headaches. Neurosci Behav Physiol 2007;37:523–526.
- Adcock K, Vanneste S. Neuroinflammation in Tinnitus. Curr Otorhinolaryngol Rep 2022;10:322–328.
- Shulman A, Wang W, Luo H, et al. Neuroinflammation and Tinnitus. Curr Top Behav Neurosci 2021;51:161–174.
- Svab G, Doczi J, Gerencser AA, et al. The Mitochondrial Targets of Neuroprotective Drug Vinpocetine on Primary Neuron Cultures, Brain Capillary Endothelial Cells, Synaptosomes, and Brain Mitochondria. Neurochem Res 2019;44:2435–2447.
- Kong L, Song C, Ye L, et al. The Effect of Vinpocetine on Human Cytochrome P450 Isoenzymes by Using a Cocktail Method. Evid Based Complement Alternat Med 2016;2016:5017135.