Doporučené postupy European Thyroid Association pro použití přípravků s levothyroxinem v monoterapii k optimalizaci léčby hypotyreózy
Časopis European Thyroid Journal nedávno uveřejnil doporučení expertní pracovní skupiny European Thyroid Association (ETA), které obsahuje soubor návrhů k optimalizaci léčby levothyroxinem v monoterapii s důrazem na individualizaci léčby (Centanni M, et al. ETA guidelines for the use of levothyroxine sodium preparations in monotherapy to optimize the treatment of hypothyroidism. Eur Thyroid J 2025).1
Levothyroxin sodný (LT4) v monoterapii představuje hlavní pilíř léčby hypotyreózy a frekvence jeho užívání se v průběhu času zvyšuje. Nicméně při svém „reálném“ využití čelí několika potenciálním problémům, a proto může být jeho klinická účinnost omezena. Někteří pacienti totiž nedosahují terapeutických cílů, kterými je úleva od symptomů a kontrola koncentrace sérového tyreotropního hormonu (TSH). Proto ETA ustanovila expertní pracovní skupinu, která prozkoumala dostupná data a formulovala doporučení na základě dostupných důkazů a expertních posudků. Následně vypracovala soubor návrhů k optimalizaci léčby levothyroxinem v monoterapii s důrazem na individualizaci léčby. Dále jsou zde diskutovány nutriční, farmakologické a patologické faktory, které mohou vést ke zvýšené potřebě levothyroxinu se zvláštním zaměřením na možnost použití tekutých forem a měkkých gelových kapslí s LT4.
Klíčová sdělení
- Levothyroxin sodný má úzký terapeutický index s možnými nežádoucími účinky vyplývajícími z nadměrné nebo nedostatečné léčby.
- Významná část pacientů užívajících levothyroxin nedosahuje terapeutického cíle (například koncentrace sérového TSH v mezích referenčního intervalu).
- Individualizace léčby je povinná a měla by zohledňovat cílové hodnoty koncentrace TSH, antropometrické charakteristiky a komorbidity pacientů.
- Terapie levothyroxinem vyžaduje efektivní vztah mezi lékařem a pacientem, aby byla zajištěna compliance s touto dlouhodobou léčbou.
- Znalost hlavních příčin zvýšené potřeby levothyroxinu (nutričních, farmakologických a patologických) je klíčová pro výběr optimální dávky a lékové formy levothyroxinu pro konkrétního pacienta.
K zapamatování
- U kompenzovaných pacientů bez klinických kontraindikací by měla být dlouhodobá léčba prováděna stejným přípravkem s levothyroxinem. Je důležité se vyhnout generické záměně na úrovni lékárny. (Doporučení ETA 3)
- Všechny přípravky s levothyroxinem mají podle Souhrnu údajů o přípravku (SPC) stejné podmínky užívání – 30 minut, ideálně 60 minut před jídlem nebo před spaním; tj. 3 a více hodin po večeři. (Doporučení ETA 4)
- Přípravky s levothyroxinem vyžadují pečlivou kontrolu podmínek skladování přípravků s levothyroxinem. (Doporučení ETA 1)
- Je nutný pečlivý anamnestický rozhovor o lécích, které pacienti užívají souběžně s levothyroxinem. (Doporučení ETA 8)
- U těhotných žen léčených levothyroxinem se provádí monitoring koncentrací TSH, volného a celkového thyroxinu (T4) alespoň v každém trimestru. (Doporučení ETA 9a)
- Použití tekutých roztoků levothyroxinu nebo měkkých gelových kapslí jako první volby lze zvážit u pacientů, kteří mají riziko malabsorpce tabletových přípravků LT4. (Doporučení ETA 16a, b)
- Ve specifických případech u pacientů s poruchou gastrointestinální absorpce, enterálně krmených a u novorozenců lze zvážit přednostní užití tekutých přípravků s levothyroxinem. (Doporučení ETA 16c).
POZN RED.: V ČR nejsou tekuté formy (roztok) LT4 dostupné.
Úvod
Levothyroxin sodný (LT4) v monoterapii představuje hlavní pilíř léčby hypotyreózy a jeho užívání se v průběhu času zvyšuje, jde o jeden z nejčastěji předepisovaných léků na světě.2
Léčbu levothyroxinem charakterizují tři hlavní rysy:
- a) obvykle se jedná o celoživotní léčbu;
- b) levothyroxin je lék s úzkým terapeutickým indexem;
- c) několik rušivých faktorů může bránit dosažení terapeutického cíle, konkrétně dosažení koncentrace TSH v séru v referenčních mezích při absenci symptomů hypotyreózy.
Podle koncentrace TSH v séru jako markeru adekvátní produkce hormonů štítné žlázy u pacientů s primární hypotyreózou se téměř polovina pacientů léčených LT4 z celosvětového pohledu zdá být nedostatečně nebo nadměrně léčena.3
Pacienti s nadměrnou léčbou LT4 jsou vystaveni chronickému nadbytku jodtyroninů v citlivých cílových tkáních, zejména v srdci a kostech4, zatímco nedostatečně léčení pacienti mohou pociťovat mírné a nespecifické příznaky, které je obtížné odlišit od příznaků jiných klinických stavů5.
Kromě toho je většina uživatelů LT4 léčena na základě jediné mírně zvýšené koncentrace TSH v séru a často nevhodným způsobem.6
Dodržování léčby je dalším náročným aspektem terapie LT4. Špatná adherence k léčbě byla dlouhodobě považována za hlavní příčinu selhání léčby LT4.7 K dalším faktorům vedoucím k suboptimální suplementaci patří LT4 nutriční, farmakologické nebo patologické interference.8–10 Farmaceutické společnosti zpřístupnily nové formy LT4, jejichž cílem je tyto problémy překonat.11
S ohledem na tato fakta je zřejmé, že je zapotřebí doporučení pro optimalizaci léčby monoterapií levothyroxinem.
Charakteristika přípravku
Dostupnou lékovou formou thyroxinu je pentahydrát sodné soli levothyroxinu (LTSS), představený již v roce 1949.12
Hormony štítné žlázy a jejich metabolity jsou hydrofobní, což se zvyšuje s vyšším stupněm jodace, a jsou špatně rozpustné při neutrálním fyziologickém pH. Jsou rozpustnější a stabilnější v roztoku při alkalickém pH. Při velmi nízkém pH se jejich rozpustnost také zvyšuje, ale pak se rychleji rozkládají.
LT4 je jedním z produktů, které jsou z trhu stahovány nejčastěji, zejména kvůli problémům s udržením účinnosti během doby exspirace.13
Vzhledem k tomu, že LTSS se řadí mezi deset nejvíce předepisovaných léků na celém světě, jsou bezpečnost, stabilita a spolehlivost těchto přípravků vysoce náročné pro výrobu, skladování, dodržení doby exspirace, distribuci a dodržení léčebného režimu pacienty žijícími v různých socioekonomických a regionálních podmínkách.
Doporučení 1
Postupná dehydratace pentahydrátu sodné soli levothyroxinu vyžaduje pečlivou kontrolu skladovacích podmínek hormonu.
Slabé doporučení. Kvalita důkazů (ØØØO). Shoda: 8/8.
Další doporučení ve specifických situacích (podstatně kráceno)
Pacient s nedostatečnou compliance
Hypotyreóza často vyžaduje celoživotní léčbu LT4, u které je spolupráce pacientů zásadní pro terapeutický úspěch, což se odráží v sérové koncentraci TSH. Přestože Světová zdravotnická organizace (WHO) uvádí, že průměrná míra adherence k dlouhodobé léčbě je přibližně 50 %, léčba hypotyreózy je považována za jeden z klinických stavů, u kterých je compliance lepší.14
V roce 1991 Ain a kol. zkoumali otázku compliance vs. malabsorpce léků u perzistující hypotyreózy a zjistili normální procento absorpce podaného LT4.15 Nedostatečná compliance a často i úmyslné nedodržování léčby patří mezi několik faktorů, které brání dosažení eutyreózy.7
Lékař je tedy postaven před otázku, zda stav pacienta může také souviset s gastrointestinálními problémy nebo s interferencí jídla a/nebo jiných léků.10
Test absorpce LT4 se ukázal jako účinný a bezpečný způsob posouzení refrakterní hypotyreózy a poskytuje spolehlivé informace pro odlišení malabsorpce LT4 od „pseudomalabsorpce“, což je stav úmyslného nebo neúmyslného nedodržování léčebného režimu.16
Doporučení 2
2a) Pokud dávka levothyroxinu potřebná k normalizaci hodnoty sérového TSH přesáhne 1,5–1,7 μg/kg/den u dospělých pacientů s hypotyreózou s thyroid in situ nebo 1,8–2,0 μg/kg/den u pacientů po thyreoidektomii, vždy prozkoumejte nízkou adherenci k léčbě, nebo dokonce pseudomalabsorpci.
Silné doporučení. Kvalita důkazů (ØØOO). Shoda 8/8.
2b) U pacientů refrakterních na levothyroxin by měl být (po vlivu vyloučení potravy, léků a známých komorbidit) proveden test absorpce levothyroxinu.
Silné doporučení. Kvalita důkazů (ØØØO). Shoda 8/8.
Náklady na léčbu tyroxinem
Levothyroxin sodný je k dispozici ve formě tablet nebo gelových kapslí či jako roztok, respektive jako prášek k přípravě roztoku; cena se může lišit v závislosti na formě, typu zdravotního pojištění a zemi. Kromě toho byly potvrzeny nepřímé náklady na záměnu konkrétního přípravku nebo lékových forem (náklady na lékařskou péči a vyšší spotřeba zdrojů zdravotní péče).17,18
K dispozici je řada generických přípravků s LT4, avšak jejich účinnost se může lišit. Není zaručeno, že pacient vždy dostane stejný generický lék od stejného výrobce.19 Ve studii (Brito JP, et al.)20 zahrnující přibližně 16 000 pacientů není přechod mezi generiky spojen s klinicky významnými změnami koncentrace TSH, což jiné studie nepotvrzují.17,19,21,22 Studie Brita byla založena na „databázi administrativních záznamů propojených s výsledky laboratorních testů“. Tento přístup proto může skrývat několik matoucích bodů. Práce byla provedena na generických přípravcích používaných především ve Spojených státech amerických a mnohem méně v Evropě.
Předmětem diskuse jsou i důsledky přechodu mezi originálním a generickým přípravkem a mezi různými lékovými formami LT4. V evropských zemích způsobil přechod z jedné značky levothyroxinu na jinou určité zdravotní problémy.21 Mezi tyto nežádoucí účinky patřily bolesti hlavy, svalová únava, deprese, úzkost, vypadávání vlasů a nespavost. Existuje i nejistota ohledně bioekvivalence LT4 některých generik s léky originálního typu, protože byly u pacientů nalezeny určité rozdíly v koncentracích TSH.17,21,22
Užívání stejného přípravku s LT4 navíc vede k významnému snížení nákladů na lékařskou péči.17,22 Při přechodu z originálního léku na generikum může dojít ke zvýšeným nákladům na zdravotní péči, a další nárůst znamenala častá změna dávky.18
Pacienti si proto musejí být vědomi toho, že v lékárně může dojít ke generické záměně LT4, a musejí požádat o vydání předepsaného (stejného) léčiva.
POZN. RED.: V ČR může předepisující lékař na recept napsat „Nezaměňovat“. Informace SÚKL
Společné prohlášení Evropské asociace štítné žlázy (ETA) a Mezinárodní federace štítné žlázy (TFI) potvrdilo, že po změně přípravku s LT4 bioekvivalenční data nezaručují pokračující eutyreózu.21
Doporučení 3
U pacientů s optimální biochemickou hormonální substitucí a bez klinických kontraindikací by měla být zachována současná léčba stejným přípravkem s levothyroxinem. Pokud je nutná jakákoli změna, pak s ohledem na klinickou situaci se doporučuje měření hodnot FT4 a TSH po 6 týdnech.
Silné doporučení. Kvalita důkazů (ØØØO). Shoda 8/8.
Hledání minimální účinné dávky
Načasování léčby LT4
Několik studií zkoumalo vliv načasování podání LT4 na koncentraci TSH v séru, která je považována za nejlepší marker produkce hormonů štítné žlázy. Obecný závěr říká, že režimy nalačno a režimy před spaním jsou spojeny s hodnotami koncentrace TSH v referenčních intervalech.23–26
Doporučení 4
Pracovní skupina doporučuje, aby načasování podávání levothyroxinu odpovídalo životnímu stylu pacienta. Interval mezi podáváním léků a jídla nebo pití nesmí být v žádném případě kratší než 30 minut. Pro dosažení optimální terapeutické účinnosti by však měl být levothyroxin užíván důsledně buď 60 minut před snídaní, nebo před spaním (3 nebo více hodin po večeři).
Silné doporučení. Kvalita důkazů (ØØØO). Shoda 8/8.
Interference s potravou
Optimální absorpce LT4 je nalačno, přičemž 62–82 % dávky se vstřebá během prvních tří hodin po požití.27
U některých druhů potravin a doplňků stravy bylo pozorováno, že snižují absorpci LT4, a to včetně sóji, kávy, vápníku a grapefruitu (tabulka 1).10,28
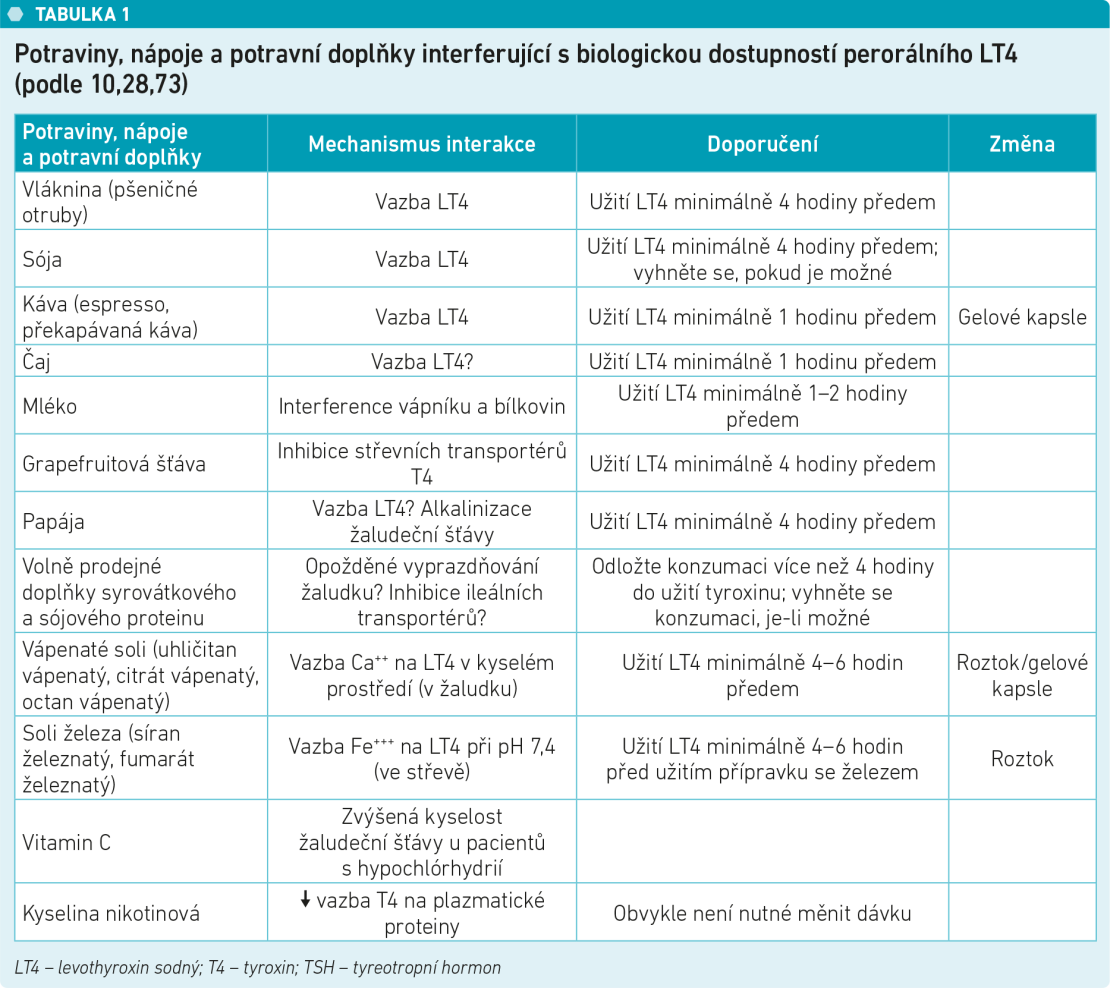
Přestože k absorpci perorálního LT4 dochází převážně v jejunu a ileu45, pacienti s žaludečními poruchami potřebují vyšší dávky T429.
Doporučení 5
U dříve dobře kontrolovaných pacientů s hypotyreózou léčenou LT4 může být nález změněného testu funkce štítné žlázy (TFT) způsoben přechodnou interferencí v důsledku určitého jídla nebo změněných stravovacích návyků. Pracovní skupina doporučuje u netěhotných pacientek před zvýšením dávky LT4 znovu provést TFT.
Silné doporučení. Kvalita důkazů (ØØØO). Shoda 8/8.
Minimální účinná dávka LT4
Dávka LT4 potřebná k udržení eutyreózy je taková, která zmírňuje příznaky hypotyreózy a udržuje koncentraci TSH v séru v referenčním rozmezí.30 Dávku LT4 potřebnou k udržení TSH u konkrétního pacienta může ovlivnit několik faktorů. Existují konzistentní důkazy o tom, že potřebu dávky LT4 může ovlivnit skutečná tělesná hmotnost/hmotnost bez tukové tkáně/ideální tělesná hmotnost, věk, etiologie hypotyreózy, stupeň zvýšení koncentrace TSH v séru před léčbou a těhotenství.
Doporučení 6
Při určování počáteční dávky levothyroxinu a výpočtu denní potřeby je třeba zvážit hmotnost pacienta, svalovou hmotu, těhotenský stav, etiologii hypotyreózy, věk a obecný klinický kontext.
Silné doporučení. Kvalita důkazů (ØØØO). Shoda 8/8.
Nežádoucí účinky nedostatečné a nadměrné léčby
WHO zařadila levothyroxin mezi léky s úzkým terapeutickým indexem, protože i malé změny v dávce LT4 mohou vést k podstatným změnám koncentrace TSH v séru.31
Observační studie pacientů s hypotyreózou léčených LT4 prokázaly, že téměř polovina pacientů má nízké nebo vysoké koncentrace TSH v séru, což svědčí o nadměrné nebo nedostatečné substituci2, což může být spojeno nepříznivými zdravotními následky, včetně ischemické choroby srdeční, srdečních arytmií, srdečního selhání a fraktur4,32,33. Tato rizika byla výraznější u pacientů s trvale extrémními koncentracemi TSH v séru (< 0,1 mU/l nebo > 10,0 mU/l).
Doporučení 7
7a) Pracovní skupina doporučuje, aby byla dávka levothyroxinu u pacientů s primární hypotyreózou upravena tak, aby se dosáhlo koncentrace sérového TSH v rámci referenčního intervalu dané populace. Jakmile je dosaženo cílové hodnoty koncentrace TSH, složité režimy a drobné úpravy dávky LT4 za účelem zlepšení kvality života nebo modulace tělesné hmotnosti nejsou užitečné a nedoporučují se.
Silné doporučení. Kvalita důkazů (ØØØ). Shoda 8/8.
7b) Koncentrace sérového TSH se zvyšuje s věkem. Je třeba usilovat o individualizaci léčby v souladu s věkem subjektu a stupněm komorbidit. U starších osob (nad 70 let) s hypotyreózou léčenou LT4 by měl být přijat uvolněnější referenční interval TSH.
Slabé doporučení. Kvalita důkazů (ØØØO). Shoda 8/8.
Interakce tyroxinu s léky a polyfarmacie
Užívání léků, které interagují a/nebo interferují s různými lékovými formami levothyroxinu, může představovat významný problém při léčbě pacientů v „reálném“ prostředí. O této skutečnosti existuje robustní evidence.8–10,34–36
Tabulka 2 uvádí léky, které pravděpodobně ovlivňují biologickou dostupnost LT4, a jejich aplikace může vyžadovat úpravu dávkování LT4. Některá běžně předepisovaná léčiva sekvestrují hormon ve střevním obsahu, čímž výrazně snižují biologickou dostupnost LT4 (podrobně v tabulce).
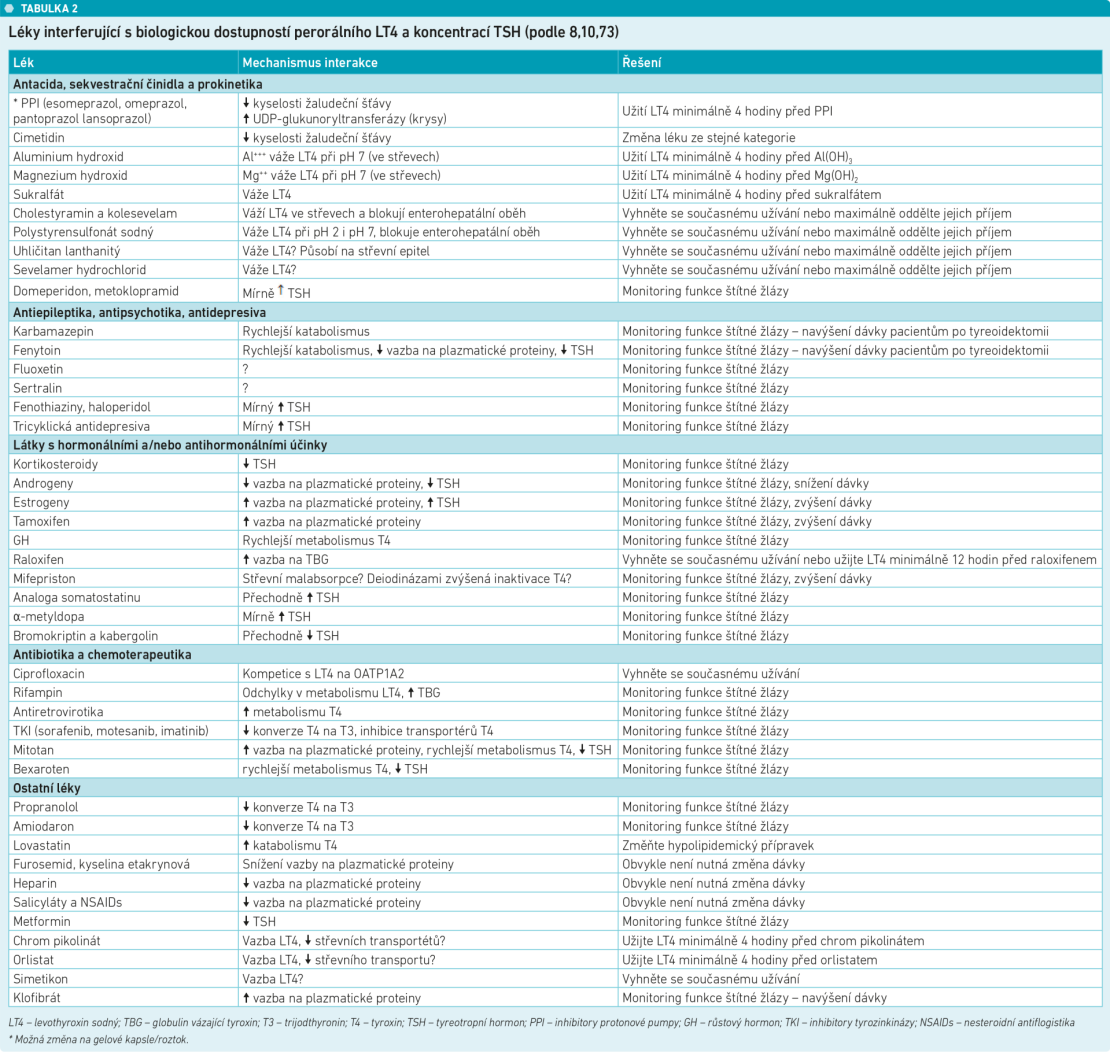
Navíc volně prodejné proteinové doplňky mohou dokonce interferovat s absorpcí LT4, například syrovátkový protein zřejmě zpomaluje reakci organických aniontových transportérů v ileu.37 Doplňky stravy obsahující železnaté soli nebo léčba železnatými přípravky snižují biologickou dostupnost LT4 adsorpcí LT4.28 Bylo prokázáno, že suplementace pikolinátu chromitého, předepisovaného ke kontrole tělesné hmotnosti, snižuje biologickou dostupnost LT4 až o 17 %.38
Lékaři by proto měli být dobře obeznámeni se všemi výše uvedenými prokázanými a předpokládanými interakcemi lék-lék, doplněk-lék a potrava-lék (tabulky 1 a 2).
Doporučení 8
Pracovní skupina doporučuje pečlivý anamnestický rozhovor o lécích, které pacienti léčení LT4 užívají. V ideálním případě by nejlepší možností bylo, pokud je to možné, přerušit užívání interferujícího léčiva. V opačném případě se doporučuje naplánovat vhodnou časovou prodlevu mezi podáváním levothyroxinu a interferujícího léku (viz tabulku 2). V případech očekávané interference v důsledku léků předepsaných na dobu delší než 2 týdny terapie lze dávku levothyroxinu upravit po dobu léčby interferujícím lékem.
Silné doporučení. Kvalita důkazů (ØØOO). Shoda 8/8.
Pacienti ve zvláštních situacích
Ačkoli neexistuje mnoho recenzovaných publikací týkajících se zvláštních situací a použití různých forem LT4, je nutné mít o nich povědomí, protože jsou klinicky relevantní a důležité pro správnou léčbu. Vzhledem k tomuto nedostatku vědeckých důkazů jsou níže uvedená tvrzení založena převážně na názorech expertů.
Těhotenství a perorální antikoncepční hormonální přípravky
Těhotenství je fyziologicky spojeno s vyšší potřebou produkce T4 v důsledku řady faktorů, včetně zvýšené produkce distribučních proteinů hormonů štítné žlázy (zejména TBG) v játrech, dodávání T4 do rostoucí fetoplacentární jednotky a zvýšené degradace T4 placentárním D3. U pacientek na substituční terapii LT4 lze tuto zvýšenou potřebu uspokojit pouze zvýšenou substituční dávkou s následným poporodním snížením dávky na hodnoty před otěhotněním. Léčba hypotyreózy během těhotenství je však stále komplikovaná.39,40
Doporučení 9
9a) Pracovní skupina doporučuje monitorovat TSH, volný a celkový T4 u těhotných žen s hypotyreózou léčených LT4 alespoň v každém trimestru.
Silné doporučení. Kvalita důkazů (ØØOO). Shoda 8/8.
Léčba neplodnosti
Metody asistované reprodukce zahrnují stimulaci ovulace vysokými dávkami gonadotropinů. Nedávný systematický přehled a metaanalýza dokumentují dlouhodobě předpokládaný výsledek, že tato léčba vede ke snížení koncentrace volného T4 a zvýšení koncentrace TSH u žen s normální funkcí štítné žlázy před stimulací. To je způsobeno rychlým nárůstem produkce proteinu vázajícího hormony štítné žlázy, který je rychlejší než nárůst v normálním těhotenství a jehož rozsah je určen délkou a intenzitou ovariální stimulace.41
9b) Substituce LT4 během léčby neplodnosti ovariální stimulací může vyžadovat předchozí zvýšení substituční dávky, aby se koncentrace TSH udržely na hodnotách < 2,5 mIU/l a aby se koncentrace T4 přizpůsobily velmi strmému vzestupu hodnot proteinů vázajících hormony štítné žlázy.
Slabé doporučení. Kvalita důkazů (ØOOO). Shoda 8/8.
Centrální hypotyreóza
U hypotalamo-hypofyzární hypotyreózy nebo centrálního/sekundárního myxedému je hypofunkce štítné žlázy způsobena selháním produkce TSH v hypofýze. Biologicky inaktivní TSH je však většinou měřitelný jen imunoesejemi TSH, a proto je monitorace sérového TSH nepoužitelná při diagnostice centrální hypotyreózy. Důkazy podporující toto doporučení jsou obsaženy v předchozích pokynech ETA a nezměnily se.42
Doporučení 10
Pracovní skupina doporučuje, aby substituce LT4 u centrální hypotyreózy byla monitorována měřením koncentrace volného T4, nikoli však koncentrace TSH.
Silné doporučení. Kvalita důkazů (ØØØO). Shoda 8/8.
Starší pacienti
U starších pacientů bylo popsáno několik různých variant patofyziologie štítné žlázy.43,44 Mezi ně patří snížená hmotnost svalové hmoty, snížená absorpce T4 a dejodace, stejně jako přítomnost komorbidit a užívání léků.14,42,51 V populační studii mělo 70 % pacientů starších 80 let sérovou koncentraci TSH vyšší než 4,5 mU/l (v 97,5 percentilu 7,49 mU/l).45 Aby se zabránilo chybné diagnóze subklinických poruch štítné žlázy, měl by se použít věkově specifický referenční interval.
Léčba starších pacientů se proto obvykle doporučuje pouze pacientům s přetrvávajícími koncentracemi TSH > 10 mU/l, zatímco v léčbě u koncentrací TSH v rozmezí 7–10 mU/l je nutné u rozhodnutí zohlednit aktuální stav konkrétního pacienta.46
U starších pacientů by měla léčba LT4 začínat nízkými dávkami (12,5–25 μg/kg/den) v závislosti na křehkosti a komorbiditách pacienta.47 U těchto pacientů se doporučuje snížená terapeutická dávka LT4 ve srovnání s mladšími jedinci, ale nejsou k dispozici důkazy v podobě klinických randomizovaných studií. Byly pozorovány škodlivé účinky jak nadměrné, tak i nedostatečné substituce.48,49 Proto je nanejvýš důležité vyhnout se u starších pacientů s hypotyreózou nadměrné substituční léčbě LT4 a spíše udržovat koncentraci TSH na horní hranici referenčního rozmezí, aby se chránilo stárnoucí srdce.
Doporučení 11
Zahájení léčby levothyroxinem u starších pacientů se subklinickou hypotyreózou s koncentracemi TSH mezi 7 a 10 mU/l by mělo být přizpůsobeno konkrétnímu pacientovi a léčba musí zohledňovat srdeční a kostní komorbidity.
Silné doporučení. Kvalita důkazů (ØØOO). Shoda 8/8.
Obézní pacienti
U obézních pacientů je běžné zvýšení koncentrace sérového TSH, které není způsobeno selháním tyreoidální produkce a po úbytku hmotnosti se vrací k normálu.50 Celková tělesná hmotnost je však v klinické praxi nejčastěji používaným měřítkem pro stanovení dávky, což vede k vyššímu dávkování LT4 ve srovnání s neobézními pacienty.51
Doporučení 12
Pracovní skupina doporučuje, aby byla dávka LT4 u obézních pacientů pečlivě upravena podle tělesné hmotnosti s ohledem na změny poměru mezi tělesnou hmotností bez zahrnutí tukové tkáně.
Silné doporučení. Kvalita důkazů (ØØØO). Shoda 8/8.
Pacienti po tyreoidektomii
Po tyreoidektomii se může vyskytnout řada problémů s dávkováním LT4, které závisí především na základním onemocnění štítné žlázy, tj. onkologickém, autoimunitním onemocnění štítné žlázy nebo u difuzní strumy bez ovlivnění produkce hormonů. U některých pacientů je poměrně snadné nastavit správnou dávku LT4, tj. u pacientů operovaných pro autoimunitní onemocnění štítné žlázy (Gravesova nebo Hashimotova choroba), ale u jiných to může být náročnější, například po operaci karcinomu štítné žlázy. Zdá se však, že kvalita života závisí více na stupni hypotyreózy než na rozsahu resekce (úplná nebo částečná tyreoidektomie).52
Značné procento (od dvou třetin do tří čtvrtin) pacientů po tyreoidektomii vyžaduje úpravu dávky LT4.53 Tělesná hmotnost bez tuku není jedinou proměnnou pro odhad terapeutické dávky LT4 po tyreoidektomii, a to vzhledem k vymizení produkce trijodtyroninu (T3).54,55
Doporučení 13
Výpočet dávky LT4 u pacientů po tyreoidektomii musí zohlednit tělesnou hmotnost, základní onemocnění štítné žlázy a rozsah resekce štítné žlázy.
Silné doporučení. Kvalita důkazů (ØØOO). Shoda 8/8.
Pacienti v bezvědomí a pacienti s onemocněním štítné žlázy, které nepostihuje štítnou žlázu
Pacienti na jednotce intenzivní péče (JIP) jsou obzvláště problematičtí, protože často nemohou užívat tablety perorálně. V těchto situacích pacienti potřebují jinou cestu podání, buď intravenózní LT4, nebo – pokud mají gastrostomickou sondu – perorální tekutou formu. U substituovaných pacientů dochází k perifernímu snížení konverze T4 na T3 a ke zvýšení hodnoty reverzního (neaktivního) T3, což se rutinně neměří. Proto se mohou vyskytnout jak centrální, tak periferní změny, které nesouvisejí se samotnou substitucí. Nejlepší strategií je v této situaci pokračovat v podávání pravidelné substituční dávky a zdržet se měření testů funkce štítné žlázy.56
Doporučení 14
Pracovní skupina doporučuje zachovat léčebnou dávku LT4 u pacientů na JIP a u pacientů s netyreoideálním onemocněním nezávisle na výsledcích krevních testů, které v této situaci nelze přesně interpretovat. Pokud je nutná změna způsobu podání, je zapotřebí použít odpovídající úpravu dávky.
Silné doporučení. Kvalita důkazů (ØOOO). Shoda 8/8.
Komorbidity a zvýšená potřeba perorálního levothyroxinu
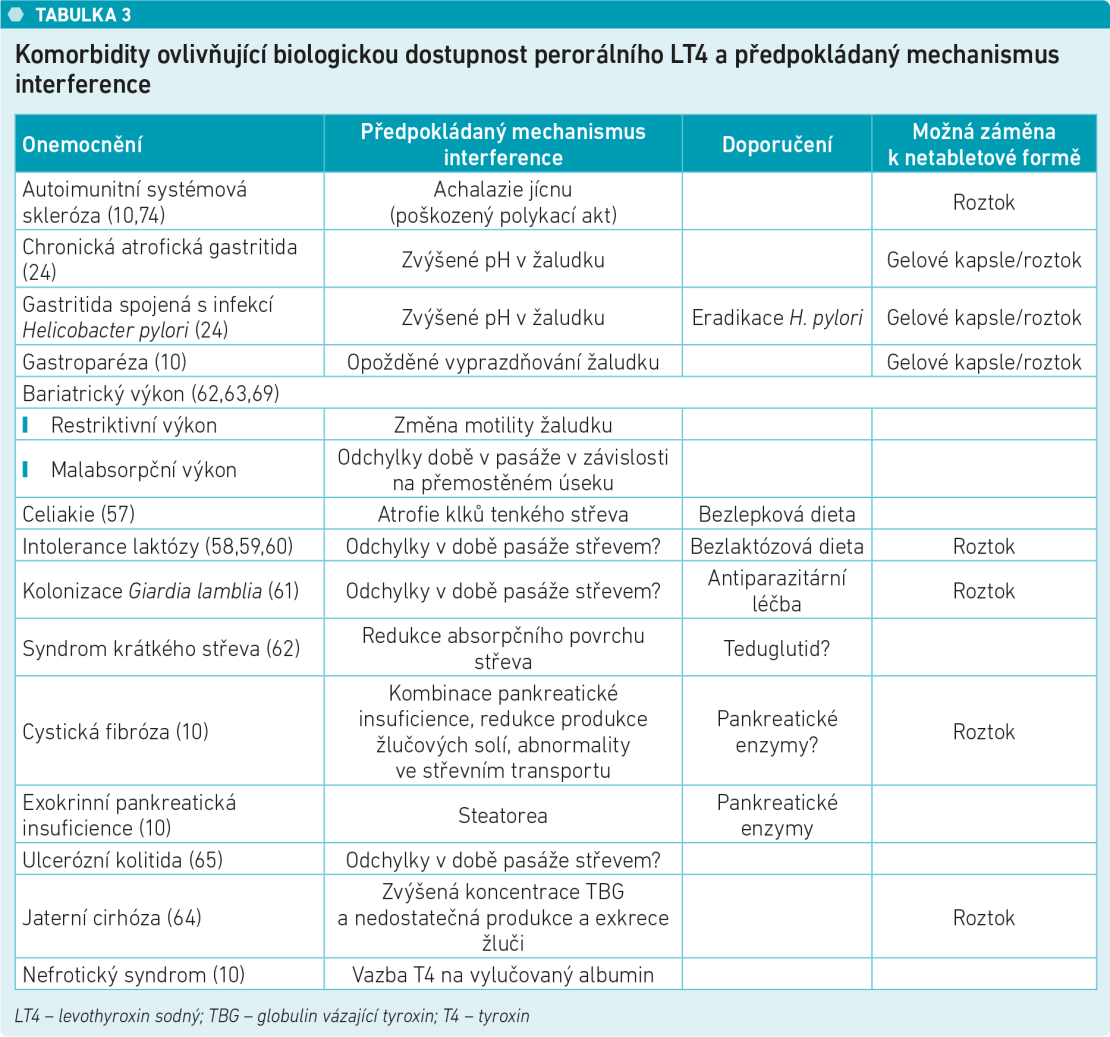
Řada poruch postihujících gastrointestinální trakt byla označena jako faktory ovlivňující biologickou dostupnost levothyroxinu.10 V souvislosti s komorbiditami ovlivňujícími potřebu LT4 se zmiňují celiakie57, malabsorpce laktózy58,59 60, zánětlivé poškození a apoptóza slizničních buněk způsobená prvokem Giardia intestinalis61, chirurgické výkony, včetně bariatrických62,63,69, jaterní cirhóza64, cystická fibróza, nefrotický syndrom a enteropatie se ztrátou bílkovin10. Zvýšená potřeba levothyroxinu byla pozorována také u pacientů s ulcerózní kolitidou65 a chronickou atrofickou gastritidou24 (viz tabulku 3).
Doporučení 15
Pokud je zjevná dlouhodobá potřeba změny dávky LT4, doporučuje se specifické diagnostické vyšetření interferujících komorbidit.
Silné doporučení. Kvalita důkazů (ØØØO). Shoda 8/8.
Hlavní rozdíly mezi tabletami a tekutými a měkkými kapslemi LT4
Ve snaze překonat výše uvedené problémy s absorpcí v gastrointestinálním traktu (jako je interference s potravou a léky či závislost na pH) byly vyrobeny a jsou komerčně dostupné netabletové formy LT4, tj. tekutý roztok (LS) a měkké gelové kapsle (SG), avšak nejsou dostupné ve všech zemích.13 Biologická dostupnost LT4 z tablet je závislá na rozpadu tablet v žaludečním lumen a vyžaduje kyselé pH žaludeční šťávy.10 Roztok LT4 se připravuje s glycerolem, SG představují gelovou formu a obsahují LT4 rozpuštěný ve vodě a glycerinu.66 Nedávná studie in vivo prokázala, že na rozdíl od tablet je biologická dostupnost měkkých kapslí nezávislá na pH žaludeční šťávy.67
Doporučení 16
16a) Po poradě s pacienty o správném užívání léčby LT4 lze u pacientů s hypotyreózou a s opakovanými hodnotami TSH nad referenčním rozmezím zvážit přechod z tablet na tekutý roztok nebo měkké gelové kapsle LT4 v nezměněné dávce.
Silné doporučení. Kvalita důkazů (ØØOO). Shoda 8/8.
Dostupné údaje o srovnání účinnosti různých lékových forem LT4
V této oblasti bylo publikováno jen málo randomizovaných klinických studií. Většina studií shromáždila malé série pacientů pozorovaných po krátkou dobu, s různými a nesrovnatelnými designy a s vysokým rizikem zkreslení výběru populace a interpretace výsledků. Metaanalýzu konkrétně zaměřenou na tuto problematiku publikovali Virili a kol.68 Cílem této studie bylo zjistit, zda přechod léčby LT4 z tablet na LS zlepšil koncentrace TSH. Bylo zkoumáno šest studií a souhrnné průměrné snížení hodnoty TSH činilo 4,23 mU/L (95% CI: 3,69–4,77) po přechodu z tablet na LS s mírnou heterogenitou mezi studiemi. Žádné prospektivní studie systematicky neporovnávaly tekuté a gelové formy levothyroxinu s pevnými formami ve vztahu ke klinickým výsledkům.
16b) Zvažte použití tekutého roztoku LT4 nebo měkkých tobolek jako léku první volby u pacientů s rizikem malabsorpce tablet LT4.
Silné doporučení. Kvalita důkazů (ØØOO). Shoda 8/8.
Existuje specifická skupina pacientů, kteří by mohli mít prospěch z užívání netabletové formy přípravků s LT4?
Na základě vlastností netabletových přípravků s LT4 a dostupné literatury lze identifikovat čtyři specifické kategorie pacientů s hypotyreózou, kteří by mohli mít prospěch z užívání netabletových léků s LT4:
- Pacienti s hypotyreózou, kteří podstoupili bariatrickou operaci.20,63,69
- Hypotyreózní kojenci a děti. Použití LS prokázalo u pacientů této věkové skupiny dobrou účinnost a určité výhody oproti tabletové formě.70,71
- Pacienti s hypotyreózou, kteří vyžadují výživu sondou během hospitalizace na jednotce intenzivní péče.72
- Poslední skupinu představují pacienti se všemi příčinami změny pH žaludeční šťávy.
16c) Pracovní skupina doporučuje, aby výše uvedené kategorie pacientů s hypotyreózou (s poruchou gastrointestinální absorpce, enterálně krmení a kojenci) mohly přednostně používat tekuté přípravky LT4.
Silné doporučení. Kvalita důkazů (ØØOO). Shoda 8/8.
Literatura
- Centanni M, et al. ETA guidelines for the use of levothyroxine sodium preparations in monotherapy to optimize the treatment of hypothyroidism. Eur Thyroid J 2025;14:e250123. doi: 10.1530/ETJ-25-0123.
- Jonklaas J, et al. Levothyroxine prescriptions trends may indicate a downtrend in prescribing. Ther Adv Endocrinol Metab 2020 11. 2042018820920551. (https://doi.org/10.1177/2042018820920551)
- Eligar V, et al. Thyroxine replacement: a clinical endocrinologist’s viewpoint. Ann Clin Biochem 2016;53:421–433. (https://doi.org/10.1177/0004563216642255)
- Biondi B, et al. Subclinical hyperthyroidism. N Engl J Med 2018;378:2411–2419. (https://doi.org/10.1056/nejmcp1709318)
- Feldt-Rasmussen U, et al. Risks of suboptimal and excessive thyroid hormone replacement across ages. J Endocrinol Investig 2024;47:1083–1090. (https://doi.org/10.1007/s40618-023-02229-7)
- Brito JP, et al. Levothyroxine use in the United States, 2008–2018. JAMA Intern Med 2021;181:1402–1405. (https://doi.org/10.1001/jamainternmed.2021.2686)
- Robertson HM, et al. Factors contributing to high levothyroxine doses in primary hypothyroidism: an interventional audit of a large community database. Thyroid 2014;24:1765–1771. (https://doi.org/10.1089/thy.2013.0661)
- Benvenga S. L-T4 therapy in the presence of pharmacological interferents. Front Endocrinol 2020;11:607446. (https://doi.org/10.3389/fendo.2020.607446)
- Centanni M, et al. Diagnosis and management of treatment-refractory hypothyroidism: an expert consensus report. J Endocrinol Investig 2017;40:1289–1301. (https://doi.org/10.1007/s40618-017-0706-y)
- Virili C, et al. Gastrointestinal malabsorption of thyroxine. Endocr Rev 2019;40:118–136. (https://doi.org/10.1210/er.2018-00168)
- Liu H, et al. Levothyroxine: conventional and novel drug delivery formulations. Endocr Rev 2023;44:393–416. (https://doi.org/10.1210/endrev/bnac030)
- Chalmers JR, et al. 715. The synthesis of thyroxine and related substances. Part V. A synthesis of L-thyroxine from L-tyrosine. J Chem Soc 1949;3424–3433. (https://doi.org/10.1039/jr9490003424)
- Kaur N, et al. Levothyroxine sodium pentahydrate tablets – formulation considerations. J Pharm Sci 2021;110:3743–3756. (https://doi.org/10.1016/j.xphs.2021.08.006)
- Briesacher BA, et al. Comparison of drug adherence rates among patients with seven different medical conditions. Pharmacotherapy 2008;28:437–443.
- Ain KB, et al. Pseudomalabsorption of levothyroxine. JAMA 1991;266:2018–2120.
- Caron P, et al. The use of levothyroxine absorption tests in clinical practice. J Clin Endocrinol Metab 2023;108:1875–1888.(https://doi.org/10.1210/clinem/dgad132)
- Hennessey JV. Levothyroxine bioequivalence: are the guidelines flawed? Nat Clin Pract Endocrinol Metab 2006;2:474–475. (https://doi.org/10.1038/ncpendmet0273).
- Ernst FR, et al. The economic impact of levothyroxine dose adjustments: the CONTROL HE study. Clin Drug Investig 2017;37:71–83. (https://doi.org/10.1007/s40261-016-0462-3)
- Qian J, et al. Real world evidence in effectiveness, safety, and cost savings of generic levothyroxine: a systematic review. Endocrine 2021;74:228–234. (https://doi.org/10.1007/s12020-021-02833-8)
- Brito JP, et al. Association between generic-to-generic levothyroxine switching and thyrotropin levels among US adults. JAMA Intern Med 2022;182:418–425. (https://doi.org/10.1001/jamainternmed.2022.0045)
- Fliers E, et al. European Thyroid Association (ETA) and Thyroid Federation International (TFI) joint position statement on the interchangeability of levothyroxine products in EU countries. Eur Thyroid J 2018;7:238–242. (https://doi.org/10.1159/000493123)
- Hennessey JV. The emergence of levothyroxine as a treatment for hypothyroidism. Endocrine 2017;55:6–18. (https://doi.org/10.1007/s12020-016-1199-8)
- Bach-Huynh TG, et al. Timing of levothyroxine administration affects serum thyrotropin concentration. J Clin Endocrinol Metab 2009;94:3905–3912. (https://doi.org/10.1210/jc.2009-0860).
- Skelin M, et al. Effect of timing of levothyroxine administration on the treatment of hypothyroidism: a three-period crossover randomized study. Endocrine 2018;62:432–439. (https://doi.org/10.1007/s12020-018-1686-1)
- de Mello RB, et al. Evaluation of bedtime vs morning levothyroxine intake to control hypothyroidism in older patients: a pragmatic crossover randomized clinical trial. Front Med 2022;9:828762. (https://doi.org/10.3389/fmed.2022.828762)
- Nandhra GK, et al. Gastrointestinal transit times in health as determined using ingestible capsule systems: a systematic review. J Clin Med 2023;12:5272.
- Hays MT. Localization of human thyroxine absorption. Thyroid 1991;1:241–248. (https://doi.org/10.1089/thy.1991.1.241)
- Wiesner A, et al. Levothyroxine interactions with food and dietary supplements – a systematic review. Pharmaceuticals 2021;14:206. (https://doi.org/10.3390/ph14030206)
- Centanni M, et al. Thyroxine in goiter, Helicobacter pylori infection, and chronic gastritis. N Engl J Med 2006;354:1787–1795. (https://doi.org/10.1056/NEJMoa043903)
- Mateo RCI, et al. Thyroxine and treatment of hypothyroidism: seven decades of experience. Endocrine 2019;66:10–17. (https://doi.org/10.1007/s12020-019-02006-8)
- Ettleson MD, et al. Serum thyrotropin and triiodothyronine levels in levothyroxine-treated patients. J Clin Endocrinol Metab 2023;108:e258–e266. (https://doi.org/10.1210/clinem/dgac725)
- Thayakaran R, et al. Thyroid replacement therapy, thyroid stimulating hormone concentrations, and longterm health outcomes in patients with hypothyroidism: longitudinal study. BMJ 2019;366:el4892. (https://doi.org/10.1136/bmj.l4892)
- Evron JM, et al. Association of thyroid hormone treatment intensity with cardiovascular mortality among US veterans. JAMA Netw Open 2022;5:e2211863.
- Skelin M, et al. Effect of timing of levothyroxine administration on the treatment of hypothyroidism: a three-period crossover randomized study. Endocrine 2018;62:432–439.
- Caron P, et al. Factors influencing the levothyroxine dose in the hormone replacement therapy of primary hypothyroidism in adults. Rev Endocr Metab Disord 2021;23:463–483. (https://doi.org/10.1007/s11154-021-09691-9)
- Montanelli L, et al. Drugs and other substances interfering with thyroid function. In Thyroid Diseases. Pathogenesis, Diagnosis, and Treatment, P Vitti & L Hegedüs (Eds). pp 733–763. Springer, 2018. (https://doi.org/10.1007/978-3-319-45013-1_27)
- Kumarathunga PADM, et al. Over-the-counter protein supplement resulting in impaired thyroxine absorption in a hypothyroid patient. Endocrinol Diabetes Metab Case Rep 2021;2021:21-0070. (https://doi.org/10.1530/EDM-21-0070)
- John-Kalarickal J, et al. New medications which decrease levothyroxine absorption. Thyroid 2007;17:763–765. (https://doi.org/10.1089/thy.2007.0060)
- Lazarus J, et al. 2014 European thyroid association guidelines for the management of subclinical hypothyroidism in pregnancy and in children. Eur Thyroid J 2014;3:76–94. (https://doi.org/10.1159/000362597)
- Alexander EK, et al. Guidelines of the American Thyroid Association for the diagnosis and management of thyroid disease during pregnancy and the postpartum. Thyroid 2017;27:315–389. (https://doi.org/10.1089/thy.2016.0457)
- Busnelli A, et al. Impact of thyroid autoimmunity on assisted reproductive technology outcomes and ovarian reserve markers: an updated systematic review and metaanalysis. Thyroid 2022;32:1010–1028. (https://doi.org/10.1089/thy.2021.0656)
- Persani L, et al. 2018 European Thyroid Association (ETA) Guidelines on the diagnosis and management of central hypothyroidism. Eur Thyroid J 2018;7:225–237. (https://doi.org/10.1159/000491388)
- van Heemst D. The ageing thyroid: implications for longevity and patient care. Nat Rev Endocrinol 2024;20:5–15. (https://doi.org/10.1038/s41574-023-00911-7)
- Peeters RP. Thyroid hormones and aging. Hormones 2008;7:28–35. (https://doi.org/10.14310/horm.2002.1111035)
- Surks MI, et al. Age-specific distribution of serum thyrotropin and antithyroid antibodies in the US population: implications for the prevalence of subclinical hypothyroidism. J Clin Endocrinol Metab 2007;92:4575–4582. (https://doi.org/10.1210/jc.2007-1499)
- Ross DS. Treating hypothyroidism is not always easy: when to treat subclinical hypothyroidism, TSH goals in the elderly, and alternatives to levothyroxine monotherapy. J Intern Med 2022;291:128–140. (https://doi.org/10.1111/joim.13410)
- Roos A, et al. The starting dose oflevothyroxine in primary hypothyroidism treatment: a prospective, randomized, double-blind trial. Arch Intern Med 2005;165:1714–1720.(https://doi.org/10.1001/archinte.165.15.1714)
- Lillevang-Johansen M, et al. Over- and under-treatment of hypothyroidism is associated with excess mortality: a register-based cohort study. Thyroid 2018;28:566–574. (https://doi.org/10.1089/thy.2017.0517).
- Effraimidis G, et al. Levothyroxine therapy in elderly patients with hypothyroidism. Front Endocrinol 2021;12:641560. doi: 10.3389/fendo.2021.641560. eCollection 2021.
- Neves JS, et al. Effect of weight loss after bariatric surgery on thyroid-stimulating hormone levels in patients with morbid obesity and normal thyroid function. Obes Surg 2018;28:97–103. (https://doi.org/10.1007/s11695-017-2792-5)
- Papoian V, et al. Evaluation of thyroid hormone replacement dosing in overweight and Obese patients after a thyroidectomy. Thyroid 2019;29:1558–1562. (https://doi.org/10.1089/thy.2019.0251)
- Yaniv D, et al. Quality of life following lobectomy versus total thyroidectomy is significantly related to hypothyroidism. J Surg Oncol 2022;126:640–648. (https://doi.org/10.1002/jso.26983)
- Miccoli P, et al. Levothyroxine therapy in thyrodectomized patients. Front Endocrinol 2021;11:626268. (https://doi.org/10.3389/fendo.2020.626268)
- Gullo D, et al. Levothyroxine monotherapy cannot guarantee euthyroidism in all athyreotic patients. PLoS One 2011;6:e22552. (https://doi.org/10.1371/journal.pone.0022552)
- Luongo C, et al. Type 2 deiodinase Thr92Ala polymorphism and aging are associated with a decreased pituitary sensitivity to thyroid hormone. Thyroid 2023;33:294–300. (https://doi.org/10.1089/thy.2022.0472)
- Feldt-Rasmussen U. Laboratory measurement of thyroid-related hormones, proteins, and autoantibodies in serum. In Werner and Ingbar’s the Thyroid: A Fundamental and Clinical Text, pp 868–907. Eds LE Braverman, DS Cooper & P Kopp. Philadelphia: Lippincott, Williams & Wilkins, 2020.
- Virili C, et al. Atypical celiac disease as cause of increased need for thyroxine: a systematic study. J Clin Endocrinol Metab 2012;97:E419–E422. (https://doi.org/10.1210/jc.2011-1851).
- Castellana M, Castellana C, Giovanella L, et al. Prevalence of gastrointestinal disorders having an impact on tablet levothyroxine absorption: should this formulation still be considered as the first-line therapy? Endocrine 2020;67:281–290. (https://doi.org/10.1007/s12020-019-02185-4)
- Asik M, et al. Decrease in TSH levels after lactose restriction in Hashimoto’s thyroiditis patients with lactose intolerance. Endocrine 2014;46:279–284. (https://doi.org/10.1007/s12020-013-0065-1)
- Cellin IM, et al. Systematic appraisal of lactose intolerance as cause of increased need for oral thyroxine. J Clin Endocrinol Metab 2014;99:E1454–E1458. (https://doi.org/10.1210/jc.2014-1217)
- Seppel T, et al. Chronic intestinal giardiasis with isolated levothyroxine malabsorption as reason for severe hypothyroidism – implications for localization of thyroid hormone absorption in the gut. Exp Clin Endocrinol Diabetes 1996;104:180–182. (https://doi.org/10.1055/s-0029-1211442)
- Stone E, et al. L-thyroxine absorption in patients with short bowel. J Clin Endocrinol Metab 1984;59:139–141. (https://doi.org/10.1210/jcem-59-1-139)
- Gadiraju S, et al. Levothyroxine dosing following bariatric surgery. Obes Surg 2016;26:2538–2542. (https://doi.org/10.1007/s11695-016-2314-x)
- Benvenga S, et al. Increased requirement of replacement doses of levothyroxine caused by liver cirrhosis. Front Endocrinol 2018;9:150. (https://doi.org/10.3389/fendo.2018.00150)
- Virili C, et al. Ulcerative colitis as a novel cause of increased need for levothyroxine. Front Endocrinol 2019;10:233. (https://doi.org/10.3389/fendo.2019.00233)
- Virili C, et al. Novel thyroxine formulations: a further step toward precision medicine. Endocrine 2019;66:87–94. (https://doi.org/10.1007/s12020-019-02049-x)
- Virili C, et al. Daily requirement of softgel thyroxine is independent from gastric juice pH. Front Endocrinol 2022;13:1002583. (https://doi.org/10.3389/fendo.2022.1002583)
- Virili C, et al. Levothyroxine therapy: changes of TSH levels by switching patients from tablet to liquid formulation. A systematic review and meta-analysis. Front Endocrinol 2018;9:10.(https://doi.org/10.3389/fendo.2018.00010)
- Fallahi P, et al. TSH normalization in bariatric surgery patients after the switch from L-Thyroxine in tablet to an oral liquid formulation. Obes Surg 2017;27:78–82. (https://doi.org/10.1007/s11695-016-2247-4)
- Peroni E, et al. Congenital hypothyroidism treatment in infants: a comparative study between liquid and tablet formulations of levothyroxine. Horm Res Paediatr 2014;81:50–54. (https://doi.org/10.1159/000356047)
- Cassio A, et al. Comparison between liquid and tablet formulations of levothyroxine in the initial treatment of congenital hypothyroidism. J Pediatr 2013;162:1264–1269.e2. (https://doi.org/10.1016/j.jpeds.2012.11.070)
- Pirola I, Daffini L, Gandossi E, et al. Comparison between liquid and tablet levothyroxine formulations in patients treated through enteral feeding tube. J Endocrinol Investig 2014;37:583–587. (https://doi.org/10.1007/s40618-014-0082-9)
- Liu H, et al. Medications and food interfering with the bioavailability of levothyroxine: a systematic review. Ther Clin Risk Manag 2023;19:503–523. https://doi.org/10.2147/TCRM.S414460)
- Lobasso A, et al. Severe Hypothyroidism due to the Loss of Therapeutic Efficacy of l-Thyroxine in a Patient with Esophageal Complication Associated with Systemic Sclerosis. Front Endocrinol (Lausanne) 2017;8:241. doi: 10.3389/fendo.2017.00241. PMID: 28979239; PMCID: PMC5611405.