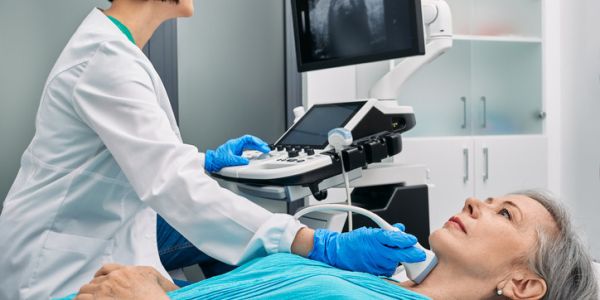
Vliv levothyroxinu sodného na výsledek těhotenství a psychomotorický vývoj potomstva pacientek se subklinickou hypotyreózou během těhotenství
Cílem citované práce [1] bylo zkoumat vliv levothyroxinu sodného (L-T4) na výsledek těhotenství a psychomotorický vývoj potomstva pacientek se subklinickou hypotyreózou (SCH) během těhotenství.
Prospektivně byly vybrány těhotné ženy s trváním gestace kratším než 12 týdnů, které podstoupily první prenatální vyšetření v období od ledna 2019 do prosince 2019. Podle koncentrace hormonů štítné žlázy byly ženy rozděleny do skupiny léčené L-T4 (n = 63), neléčené (n = 64) a kontrolní skupiny (n = 54). Tyto tři skupiny byly porovnávány v kritériích: průběh a výsledky těhotenství, stav dítěte po narození a vývoj do jednoho roku.
Byly zjištěny významné rozdíly, zejména co se týče potratů a výskytu gestačního diabetes mellitus (GDM): míra potratů a výskyt GDM v neléčené skupině byly vyšší než v kontrolní skupině (p < 0,05). Rozdíl mezi skupinou léčených žen a kontrolní skupinou ohledně potratů a GDM nebyl statisticky významný (p > 0,05). Rozdíl mezi skupinami ohledně tělesné hmotnosti potomků při narození a v jednom roce dítěte nebyl statisticky významný (p > 0,05). Avšak byl nalezen statisticky významný rozdíl (p < 0,05) u jednoletých dětí v individuální akční energii, fyzickém stavu, řečových schopnostech a lidských interakcích. Vývojový kvocient (DQ) jednoletého dítěte byl u léčené skupiny a kontrolní skupiny vyšší než u neléčené skupiny (p < 0,05). Pearsonova korelační analýza ukázala, že koncentrace tyreostimulačního hormonu (TSH) v léčené skupině nekorelují s úrovní vývojového kvocientu potomstva u jednoletých dětí (p > 0,05).
Tablety L-T4 mohou nejen zlepšit výsledek těhotenství u pacientek se SCH během těhotenství, ale také hrát pozitivní roli ve zlepšování neurokognitivního vývoje jejich potomků.
Úvod
Subklinická hypotyreóza během těhotenství je endokrinní onemocnění, které je charakterizováno sníženou sekrecí hormonů štítné žlázy a zvýšením koncentrace TSH. Mateřská štítná žláza se během těhotenství nachází fyziologicky ve specifickém období a koncentrace tyreoideálních hormonů hraje klíčovou roli v udržení normálního těhotenství a v růstu a vývoje plodu. První studie ukázaly, že [2,3] nedostatek hormonů štítné žlázy během těhotenství nesouvisí pouze s těhotenskými komplikacemi a porodnickými výsledky, jako je spontánní potrat, předčasný porod a poporodní krvácení, ale také s poruchami kognitivního vývoje potomků. Následné studie u žen se SCH během těhotenství a u jejich potomků přitáhly pozornost a několika výzkumníků [4,5], kteří se se domnívají, že je velmi důležité udržovat optimální hodnoty tyreoideálních hormonů v průběhu gravidity.
Evropská asociace pro štítnou žlázu (European Thyroid Association, ETA) [6] se domnívá, že všechny těhotné ženy se SCH by měly být během těhotenství léčeny L-T4. Americká asociace pro štítnou žlázu (American Thyroid Association, ATA) [7] doporučuje léčbu L-T4 pro SCH u těhotných žen s přetrváváním protilátek proti tyreoidální peroxidáze (TPO-Ab). V nepřítomnosti protilátek ATA léčbu nedoporučuje ani nezakazuje.
Současné názory na léčbu SCH pomocí L-T4 během těhotenství však nejsou zcela konzistentní. Tato studie proto analyzovala výsledky těhotenství, fyzickou konstituci potomstva a vývojový kvocient, aby se zjistilo, zda intervence L-T4 může hrát roli v průběhu těhotenství, jeho výsledku a ve vývoji dítěte.
Prospektivně byly do studie zařazeny těhotné ženy, jejichž těhotenství trvalo méně než dvanáct týdnů. Nábor trval od ledna do prosince 2019.
Kritéria pro zařazení: splnění diagnostických kritérií Doporučených postupů pro diagnostiku a léčbu onemocnění štítné žlázy v těhotenství a po porodu [8], normální jednočetné těhotenství a bez předchozí anamnézy nepříznivého průběhu těhotenství.
Kritéria pro vyloučení: další závažná onemocnění postihující endokrinní systém, rodinná anamnéza onemocnění štítné žlázy a těhotenství po asistované reprodukci.
Studijní populace
Podle koncentrace hormonů štítné žlázy byly pacientky rozděleny do skupin: léčené L-T4 (n = 63) (2,5 mIU/l < TSH ≤ 4,0 mIU/l s pozitivní reakcí na TPO-Ab; TSH ≥ 4,0 mIU/l), neléčené skupiny (n = 64) (2,5 mIU/l < TSH ≤ 4,0 mIU/l s negativní reakcí na TPO-Ab) a kontrolní skupiny (n = 54) (TSH ≤ 2,5 mIU/l). Mezi těmito třemi skupinami nebyl zjištěn statisticky významný rozdíl ve výchozích datech (p > 0,05).
Počáteční dávka L-T4 byla stanovena podle výše koncentrace TSH podle Doručených postupů pro diagnostiku a léčbu onemocnění štítné žlázy v těhotenství a po porodu [8]. Při koncentraci TSH > horní hranice normy specifické pro těhotenství (2,5 mIU/l) činila počáteční dávka L-T4 50 μg/den; u TSH > 8,0 mIU/l pak 75 μg/den. Tablety se užívaly jednou denně nalačno ráno. Dávka byla titrována podle cílové koncentrace sérového TSH, která byla v prvním, druhém a třetím trimestru těhotenství udržována na 0,1–2,5 mIU/l, 0,2–3,0 ml U/l a 0,3–3,0 mIU/l. Podávání léků bylo na konci těhotenství ukončeno a funkce štítné žlázy byla pravidelně kontrolována až k návratu do normálního rozmezí.
Komplikace a výsledky těhotenství a neuropsychický vývoj potomstva ve věku jednoho roku byly sledovány prostřednictvím ambulantní služby, telefonu a WeChat.
Metodologii a statistické zpracování podrobně uvádí práce Qiana a kol. [1].
Výsledky
Rozdíl mezi skupinami v míře potratů a GDM byl statisticky významný: míra potratů a výskyt GDM v neléčené skupině byly vyšší než v kontrolní skupině (p < 0,05). Rozdíl mezi léčenou a kontrolní skupinou v míře potratů a GDM nebyl statisticky významný (p > 0,05). Rozdíl mezi skupinami v počtu předčasných porodů a počtu donošených dětí s nízkou porodní hmotností nebyl statisticky významný (p > 0,05).
Nebyl zjištěn statisticky významný rozdíl v hmotnosti jak při narození, tak v jednom roce (p > 0,05).
V jednom roce dítěte nebyl rozdíl v individuální akční energii, fyzickém vývoji, řečových schopnostech a v komunikačních dovednostech mezi třemi skupinami statisticky významný (p < 0,05). Avšak vývojový kvocient ve věku jednoho roku v léčené skupině a kontrolní skupině byl vyšší než v neléčené skupině (p < 0,05).
Podle Pearsonovy korelační analýzy nejevila koncentrace TSH u těhotných žen v léčené skupině a výše DQ u jednoletých potomků žádnou korelaci (p > 0,05).
Diskuse
Současné studie se domnívají, že SCH během těhotenství může zvýšit množství nepříznivých výsledků těhotenství, jako jsou předčasný porod, potrat a komplikace v těhotenství [9].
O vlivu léčby SCH pomocí L-T4 bylo publikováno několik studií [10–12], které se zásadně neliší v klíčových výsledcích, ale ve statistické významnosti.
Autoři studie uvádějí [12], že k léčbě těhotných žen se SCH lze použít levothyroxin, vitamin B12 a kyselinu listovou. Pravidelné sledování glykemie, lipidemie a koncentrace homocysteinu může přispět k odvrácení nepříznivých důsledků SCH na těhotenství. Autoři se současně domnívají, že příčinou nekonzistentního výsledku po léčbě L-T4 jsou rozdíly v genetickém pozadí, životním prostředí mezi různými studijními populacemi a nekonzistentní rozsah referenčních hodnot TSH.
První a druhý trimestr těhotenství jsou fází rychlého vývoje nervové soustavy plodu, pro nějž jsou hormony štítné žlázy dodávány převážně placentárním transportem [13]. Nedostatečná koncentrace hormonů štítné žlázy vede k poruše zrání fetálních kortikálních, pyramidových a gliových buněk. Účast hormonu štítné žlázy na výskytu a tvorbě neuronů v hipokampu a somatosenzorické oblasti kortexu byla potvrzena v předchozích studiích [14]. Dále se zkoumalo, zda gestační SCH žen bude mít dlouhodobý vliv na vývoj kognitivních schopností jejich potomků. Někteří vědci zjistili [15], že SCH během těhotenství může mít vliv na vývoj inteligence ve věku sedmi a osmi let a ve srovnání s potomky těhotných žen s normální funkcí štítné žlázy je inteligenční kvocient (IQ) potomků neléčených těhotných žen s SCH snížen o sedm procentních bodů.
Standardizovaná léčba subklinické hypotyreózy s nepřítomností TPO-Ab během těhotenství a udržení koncentrace TSH na 4,0–10,0 mIU/l před 8. týdnem těhotenství mohou významně zlepšit úroveň kognitivního vývoje potomstva ve věku 2 let [16]. Výsledky této studie ukazují [1], že DQ jednoletých dětí v léčené a kontrolní skupině je vyšší než u neléčené skupiny, což naznačuje, že léčba L-T4 má pozitivní význam. Léčba L-T4 během gravidity může do určité míry zabránit poškození kognitivních funkcí potomstva způsobenému deficitem mateřských hormonů štítné žlázy.
Závěrem lze říci, že L-T4 může nejen zlepšit výsledek těhotenství u žen se subklinickou hypotyreózou, ale také hrát pozitivní roli ve zlepšení vývoje kognitivních funkcí jejich potomků. Proto jsou včasný screening funkce štítné žlázy u matky a její přiměřená léčba užitečné jak pro výsledky těhotenství, tak pro psychomotorický vývoj dítěte.
Limitací studie je relativně malá velikost vzorku, což může vést ke zkreslení výsledků. Zkoumána je pouze úroveň vývojového kvocientu potomstva ve věku jednoho roku. Vliv levothyroxinu sodného na dlouhodobý vývojový kvocient potomstva je třeba ověřit rozsáhlými a prospektivními studiemi, aby bylo možné optimalizovat léčebné schéma.
Literatura
- Qian X, et al. Effect of Levothyroxine Sodium Tablets on Pregnancy Outcome and Offspring Development Quotient of SCH during Pregnancy. J Healthc Eng 2022;2022:9001881. doi: 10.1155/2022/9001881. PMID: 35388329; PMCID: PMC8979691.
- Sullivan SA. Hypothyroidism in pregnancy. Clin Obst Gynecol 2019;62:308–319. doi: 10.1097/grf.0000000000000432.
- Karcaaltincaba D, et al. Prevalences of subclinical and overt hypothyroidism with universal screening in early pregnancy. Arch Gynecol Obst 2020;301:681–686. doi: 10.1007/s00404-020-05462-0.
- Beharier O, et al. Maternal hypothyroidism during pregnancy and the risk for infectious morbidity of the offspring. Am J Perinatol 2020;37:291–295. doi: 10.1055/s-0039-3400980.]
- Wang B, et al. Oral and intestinal microbial features in pregnant women with hypothyroidism and their correlations with pregnancy outcomes. Am J Physiol Endocrinol Metab 2020;319:E1044–E1052. doi: 10.1152/ajpendo.00234.2020.]
- Luster M, et al. European perspective on 2015 American thyroid association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer: proceedings of an interactive international symposium. Thyroid 2019;29:7–26. doi: 10.1089/thy.2017.0129.
- Jonklaas J, et al. Guidelines for the treatment of hypothyroidism: prepared by the American Thyroid Association task force on thyroid hormone replacement. Thyroid 2014;24:1670–1751. doi: 10.1089/thy.2014.0028.
- Shan ZY, Teng WP. Interpretation of key points of guidance for diagnosis and treatment of thyroid diseases during pregnancy and postpartum (2nd edition). Chin J Endocrin Metab 2019;35:636–665.
- Runkle I, et al. Early levothyroxine treatment for subclinical hypothyroidism or hypothyroxinemia in pregnancy: the st carlos gestational and thyroid protocol. Front Endocrinol 2021;12:743057. doi: 10.3389/fendo.2021.743057.
- Rao M, et al. Effect of levothyroxine supplementation on pregnancy loss and preterm birth in women with subclinical hypothyroidism and thyroid autoimmunity: a systematic review and meta-analysis. Hum Rep Update 2019;25:344–361. doi: 10.1093/humupd/dmz003.
- Kianpour M, et al. Thyroid-stimulating hormone (TSH) serum levels and risk of spontaneous abortion: a prospective population-based cohort study. Clin Endocrinol 2019;91:163–169. doi: 10.1111/cen.13979.
- Han L, et al. Laboratory characteristics analysis of the efficacy of levothyroxine on subclinical hypothyroidism during pregnancy: a single-center retrospective study. Bioengineered 2021;12:4183–4190. doi: 10.1080/21655979.2021.1955589.
- Araujo APB, et al. The role of astrocytes in the development of the cerebellum. Cerebellum 2019;18:1017–1035. doi: 10.1007/s12311-019-01046-0.
- Liu YY, Brent GA. The role of thyroid hormone in neuronal protection. Compr Physiol 2021;11:2075–2095. doi: 10.1002/cphy.c200019.
- Lucaccioni L, et al. Long term outcomes of infants born by mothers with thyroid dysfunction during pregnancy. Acta BioMed 2020;92:e2021010. doi: 10.23750/abm.v92i1.9696.
- Chen J, et al. Subclinical hypothyroidism with negative for thyroid peroxidase antibodies in pregnancy: intellectual development of offspring. Thyroid 2022; 32:449–458. doi: 10.1089/thy.2021.0374.
CZ-EUT-00151

