Cystická fibróza 2026: Kde jsme a kam směřujeme?
Cystická fibróza (CF) byla ještě donedávna onemocněním s velmi nepříznivou prognózou – většina pacientů se nedožívala dospělosti. Pokrok v posledních dvou dekádách ale zásadně změnil přirozený průběh choroby. Díky cílené terapii dnes mohou nově diagnostikované děti dosahovat téměř normální délky života. Klíčové milníky vývoje léčby a současné terapeutické možnosti přiblížil 9. února během online setkání vedoucí výzkumu léčiv pro CF ve společnosti Vertex Pharmaceuticals Fredrick Van Goor, Ph.D.
Od symptomatické léčby k terapii samotné příčiny
Pacienti s cystickou fibrózou v minulosti často umírali už v kojeneckém věku, a to především v důsledku malabsorpce a střevní neprůchodnosti. Zavedení substituce pankreatických enzymů tedy představovalo první významný krok ke zlepšení přežití. Jenže pak se hlavní příčinou mortality pacientů s touto chorobou stala plicní onemocnění. Klinické studie a jejich primární cíle u osob ve věku 12 let a starších se proto zaměřovaly na plicní funkce. Zásadní změnu přinesl vývoj modulátorů CFTR, které cílí na samotnou příčinu onemocnění. V současné době lze říci, že cystická fibróza díky inovativní terapii – modulátorům CFTR – představuje chronické celoživotní onemocnění s potenciálem dožití kolem 70 nebo 80 let. Modulátory CFTR cíleně ovlivňují funkci CFTR proteinu, a tím zasahují samotnou příčinu cystické fibrózy. Vedou ke snížení počtu hospitalizací, potřeby transplantací i závislosti na symptomatické terapii a prodlužují přežití. „A právě proto je cílem zahájit léčbu co nejdříve, aby se předešlo rozvoji nevratného poškození orgánů už v raném věku,“ zdůraznil Van Goor. Dlouhodobou vizí je pak minimalizace symptomů a redukce potřeby zdravotní péče, kdy by bylo možné pacientovi podat moderní léčbu v podobě jediného léku, a snížit tak i počet návštěv nemocnic na jednu návštěvu lékaře ročně. „Naší vizí je, aby lidé mohli žít svůj plnohodnotný život, aniž by se museli potýkat s komplikacemi, které onemocnění cystickou fibrózou přináší,“ dodává Van Goor. Už dnes je podle jeho slov patrný úbytek pacientů s CF, kteří potřebují časté hospitalizace. Nejnovější trojkombinace rovněž redukuje nutnost užívání intravenózních či perorálních antibiotik, což je dobré znamení – právě infekce, na jejichž léčbu jsou určena, způsobují plicní exacerbace, které vedou k poškození dýchacích cest.
CFTR a koncentrace chloridů v potu
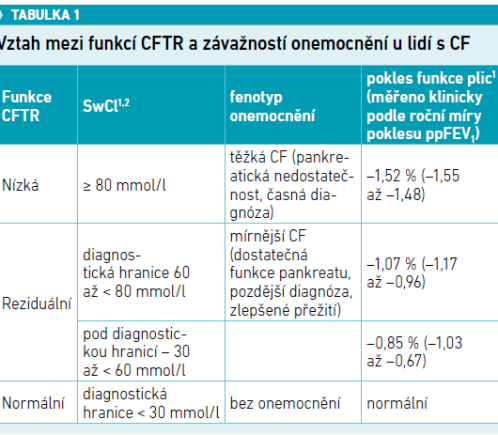 Vývoj účinné léčby by nebyl možný bez důkladného porozumění biologické podstatě onemocnění. To trvalo téměř tři desetiletí – od roku 1991 až do roku 2018. Během těchto let byla nejprve popsána cystická fibróza a následně byl identifikován gen CFTR (transmembránový regulátor cystické fibrózy) a popsány defekty v proteinu, který je tímto genem kódován. Měřítkem funkce CFTR jsou chloridy v potu (SwCl), právě jejich vysoká koncentrace patří mezi diagnostická kritéria CF (> 60 mmol/l). Existuje totiž několik prahových hodnot, které od SwCl odvozují tíži onemocnění (viz tabulku 1).
Vývoj účinné léčby by nebyl možný bez důkladného porozumění biologické podstatě onemocnění. To trvalo téměř tři desetiletí – od roku 1991 až do roku 2018. Během těchto let byla nejprve popsána cystická fibróza a následně byl identifikován gen CFTR (transmembránový regulátor cystické fibrózy) a popsány defekty v proteinu, který je tímto genem kódován. Měřítkem funkce CFTR jsou chloridy v potu (SwCl), právě jejich vysoká koncentrace patří mezi diagnostická kritéria CF (> 60 mmol/l). Existuje totiž několik prahových hodnot, které od SwCl odvozují tíži onemocnění (viz tabulku 1).
U těžké CF se porucha zhoršuje rychleji než u mírnějších forem (60 až 80 mmol/l), kdy je stále dostatečná funkce slinivky břišní. Tito pacienti jsou obvykle diagnostikováni později. Zároveň je u nich předpoklad vyššího věku dožití, protože jejich plicní funkce neklesá tak rychle. Mezi první mety výzkumu patřilo dosažení prahových hodnot od těžké po mírnou formu, což se zdařilo prostřednictvím prvních dvojkombinací korektorů a potenciátorů. „Dnes je naším cílem dostat se pod 30 mmol/l, tedy na úroveň, která odpovídá normální funkci CFTR,“ uvedl Van Goor.
Vývoj modulátorů CFTR
Vývoj cílené léčby cystické fibrózy (CF) je výsledkem rozsáhlého a dlouhodobého výzkumného úsilí. V rámci vysokoprůchodového screeningu (high‑throughput screening, HTS) bylo testováno více než milion molekul, z nichž pouze malá část postoupila do klinického hodnocení. „Na korektorech nové generace pracujeme již více než deset let,“ uvedl vedoucí výzkumu léčiv společnosti Vertex. Zdůraznil také význam pacientské komunity: „Celkový počet účastníků klinických studií jasně ukazuje, jak zásadní roli při vývoji těchto terapií sehrála komunita. Jedná se o obrovské úsilí nejen ze strany center provádějících testování, ale i samotných pacientů s CF, kteří se studií účastnili.“ Postupně bylo zjištěno, že k ovlivnění různých poruch způsobených mutacemi genu CFTR je nezbytná kombinovaná terapie. Přes vývoj první i druhé dvojkombinace modulátorů CFTR se tedy výzkum posunul ke vzniku trojkombinační terapie, která stojí na dvou korektorech a jednom potenciátoru. „Ukázalo se, že všechny tři tyto léky nebo sloučeniny se vážou na různá místa na proteinu. A to bylo nečekané,“ poznamenal Fredrick Van Goor. Vyzdvihl přitom význam vysoce výkonných screeningových testů, protože pouhým pohledem na chybu v proteinu nešlo k tomuto zjištění dojít. Velkým úspěchem je dnes fakt, že trojkombinační léčba má potenciál obnovit funkci CFTR u přibližně 95 procent pacientů.
Současné výzvy a budoucí směry
Výzvou zůstává výše zmíněných zbývajících pět procent pacientů s CF, kteří v současné době nemají přístup k modulátorům CFTR nebo z nich nemohou mít prospěch kvůli genotypu CF.
V současnosti se proto výzkum zaměřuje na další terapeutické přístupy, zejména na léčbu založenou na mRNA (např. VX‑522), novou generaci modulátorů CFTR a genovou terapii. Společnost Vertex na genové terapii dlouhodobě spolupracuje se společností Moderna a dosavadním výsledkem je molekula VH‑522 s nevirovým lipidem, která je aktuálně testována v klinických studiích. Významnou výzvou zůstává efektivní doručení léčiva do plicního prostředí zatíženého hlenem a zánětem. Další oblastí výzkumu je optimalizace léčby u nejmladších pacientů. „Léčba nejmenších dětí vyžaduje nejen nové lékové formy, ale i nové biomarkery,“ upozornil. Další pokrok pak bude záviset na rozvoji personalizované medicíny, genových terapií a hlubším porozumění dlouhodobým dopadům léčby.
Literatura:
1. McKone EF, Velentgas P, Swenson AJ, et al. Association of sweat chloride concentration at time of diagnosis and CFTR genotype with mortality and cystic fibrosis phenotype. J Cyst Fibros. 2015 Sep;14(5):580–586.
2. Farrell PM, White TB, Ren CL, et al. Diagnosis of Cystic Fibrosis: Consensus Guidelines from the Cystic Fibrosis Foundation. J Pediatr. 2017 Feb;181S:S4–S15.
Fredrick Van Goor, Ph.D.
Vedoucí výzkumu léků pro pacienty s cystickou fibrózou (CF) ve Vertex Pharmaceuticals a člen týmu pro strategii onemocnění CF, který odpovídá za mezioborovou strategii a realizaci programu. Vedl biologickou část týmu, který objevil a vyvinul ivakaftor, lumakaftor/ivakaftor, tezakaftor/ivakaftor, elexakaftor/tezakaftor/ivakaftor a vanzakaftor/tezakaftor/deutivakaftor – dosavadních pět schválených přípravků společnosti Vertex, jež léčí samotnou příčinu onemocnění až u 95 % lidí s CF – stejně jako další experimentální léky na CF, které jsou v současnosti v klinickém vývoji. V současné době vede výzkumné aktivity zaměřené na objevování a vývoj genetických terapií, jejichž cílem je léčit a potenciálně vyléčit základní příčinu CF.
Fredrick Van Goor a dva jeho kolegové ze společnosti Vertex byli oceněni Průlomovou cenou v oblasti biologických věd za rok 2024 (Breakthrough Prize in Life Sciences) a Wileyho cenou za biomedicínské vědy za rok 2023 (Wiley Prize in Biomedical Sciences) za objev transformačních kombinovaných lékových terapií, které léčí základní příčinu CF. Dále obdržel ocenění Jerry Cahill Legacy Award od nadace Boomer Esiason Foundation (2019), Respiratory Innovator Award (2018) a Doris F. Tulcin Research Award za mimořádné přínosy ve výzkumu cystické fibrózy (2013).