Jak vytěžit maximum z vyšších linií léčby kolorektálního karcinomu a karcinomu pankreatu

Na programu letošního 15. ročníku PragueONCO konaného 24. ledna 2024 bylo i sympozium zaměřené na nové léčebné strategie u metastatického kolorektálního karcinomu a metastatického karcinomu pankreatu a jejich skutečný přínos v reálné klinické praxi.
Sympozium otevřel prof. Gerald Prager z Lékařské univerzity ve Vídni, který se věnoval možnostem léčby vyšších linií u metastatického kolorektálního karcinomu (mCRC). Připomněl, že nejprve je snahou zmenšit velikost nádoru a ideálně jej změnit z neresekovatelného na resekovatelný. Cílem dalších léčebných linií pak je dostat onemocnění pod kontrolu, prodloužit přežití, a když ne zlepšit, tak alespoň udržet kvalitu života nemocných. Tomu by měla odpovídat i sekvence jednotlivých terapeutických modalit. „Ve třetí linii léčby mCRC je více než 90 procent pacientů již předléčeno cílenou terapií. To samozřejmě omezuje volbu dalšího postupu. Proto jsou tak důležité výsledky klinické studie SUNLIGHT,“ uvedl prof. Prager s tím, že tato studie hodnotila účinnost a bezpečnost kombinace trifluridin/tipiracil (FTD/TPI) + bevacizumab (bev) u předléčených nemocných s mCRC.
Studie fáze III zahrnovala pacienty ve věku ≥ 18 let s histologicky potvrzeným mCRC, ECOG PS 0/1, kteří byli léčeni maximálně jedním až dvěma předchozími režimy včetně fluoropyrimidinů, irinotekanu, oxaliplatiny, monoklonálními protilátkami proti VEGF a/nebo monoklonálními protilátkami proti EGFR pro RAS nemutované nádory. Pacienti byli náhodně rozděleni v poměru 1 : 1 na ty, kteří dostávali FTD/TPI + bev vs. FTD/TPI v monoterapii (skupina FTD/TPI). Primárním cílovým ukazatelem bylo celkové přežití (OS), sekundárními cílovými ukazateli bylo přežití bez progrese (PFS) a bezpečnost léčby, včetně doby do zhoršení skóre výkonnosti. Do každé skupiny bylo zařazeno celkem 246 pacientů.
Výsledky ukázaly, že medián celkového přežití činil 10,8 měsíce ve skupině s kombinací a 7,5 měsíce ve skupině FTD/TPI (poměr rizika úmrtí 0,61; 95% interval spolehlivosti [CI] 0,49–0,77; p < 0,001). „Takovéto výsledky jsme u třetí linie léčby dosud neviděli, podstatné je, že komparátorem zde nebylo jako u jiných studií placebo, ale aktivní léčba. Ukázalo se, že přidání bevacizumabu k FTD/TPI přináší benefit dokonce i u pacientů s mutací RAS,“ uvedl prof. Prager. Medián PFS byl 5,6 měsíce ve skupině s kombinací a 2,4 měsíce ve skupině FTD/TPI (poměr rizika pro progresi onemocnění nebo úmrtí 0,44; 95% CI 0,36–0,54; p < 0,001). Z přidání bevacizumabu k FTD/TPI benefitovali pacienti ze všech podskupin studie. „V pokročilejších liniích léčby je vždy klíčové udržení pacienta v uspokojivém výkonnostním stavu. Ve studii SUNLIGHT vidíme, že při využití kombinační terapie udržujeme pacienty déle v dobrém ECOG PS,“ popsal prof. Prager. Medián doby do zhoršení skóre ECOG z 0 nebo 1 na 2 nebo více byl 9,3 měsíce ve skupině s kombinací a 6,3 měsíce ve skupině FTD/TPI (poměr rizika 0,54; 95% CI 0,43–0,67). Ke statisticky signifikantnímu zlepšení došlo i při hodnocení podílu nemocných, u nichž došlo ke kontrole onemocnění (76,7 % u kombinované léčby vs. 47 % ve skupině FTD/TPI).
Pokud jde o bezpečnost léčby, nebyly zaznamenány významné rozdíly mezi oběma skupinami. Nejčastějšími nežádoucími účinky v obou skupinách byly neutropenie, nauzea a anémie. Nebyla hlášena žádná úmrtí související s léčbou (Prager et al., N Engl J Med 2023;388:1657–1667).
Na základě pacienty hlášených výsledků ovlivnila kombinovaná léčba pozitivně i kvalitu života (QoL). Snížilo se riziko zhoršení QoL (8,5 měsíce kombinovaná léčba vs 4,7 měsíce FTD/TPI). Pro všechny podskupiny studie měla léčba FTD/TPI + bev vždy lepší výsledky než monoterapie FTD/TPI, bez ohledu na to, zda šlo o pacienty s mutací KRAS G12, nebo bez ní (Taberno et al.; ESMO 2023).
Na tyto výsledky reagovala příslušná odborná doporučení. V aktualizovaných guidelines ESMO je ve třetí linii léčby doporučena kombinovaná terapie FTD/TPI + bev u pacientů s mutací RAS, bez mutace RAS‚ bez mutace RAS s levostranným nádorem i vzácnými molekulárními subtypy (doporučení 1A).
„U pacientů s refrakterním mCRC tak máme novou léčebnou možnost. Terapie FTD/TPI + bev přispívá k delšímu celkovému přežití v porovnání s monoterapií FTD/TPI. Díky zavedení nových terapeutických možností v pozdějších liniích se zlepšila prognóza pacientů s mCRC. Kromě prodloužení celkového přežití je v tomto případě klíčová kvalita života. Pro většinu pacientů představuje bev s FTD/TPI nový standard třetí léčebné linie. Výkonnostní stav a kvalita života pacienta jsou zachovány, což dává více pacientům možnost léčby ve čtvrté linii léčby,“ shrnul prof. Prager.
Léčba karcinomu pankreatu v klinické praxi
Druhá část sympozia se týkala nemocných s metastatickým karcinomem pankreatu (mPDAC). Nemocných s tímto agresivním nádorem přibývá a diagnostika onemocnění se posouvá do nižší věkové skupiny.
Prognóza takto nemocných je stále špatná. Určitý posun ale nastává i zde. Spočívá například v nástupu pegylovaného lipozomálního irinotekanu (nal‑IRI – Onivyde). Ten se stal po publikaci výsledků studie NAPOLI‑1 v kombinaci s 5‑fluorouracilem (5‑FU) a leukovorinem (LV) standardem léčby u pacientů s mPDAC, u nichž došlo k progresi po chemoterapii založené na gemcitabinu. S jakými výsledky je tento režim používán v reálné klinické praxe v ČR, přiblížila prof. MUDr. Beatrice Mohelniková Duchoňová, Ph.D., z Onkologické kliniky FN Olomouc. Ta představila analýzu dat z registru VILP, který byl realizován v letech 2021–2023 a zahrnoval 142 pacientů s mPDAC léčených nal‑IRI + 5‑FU/LV, z nichž 129 bylo hodnotitelných.
Cílem analýzy bylo zhodnotit snášenlivost a účinnost léčby nal‑IRI + 5‑FU/LV u pacientů se stavem výkonnosti 0–1, kteří progredovali na léčbě založené na gemcitabinu podané v (neo)adjuvanci či v 1. linii léčby. Terapie probíhala do progrese nebo nezvládnutelné toxicity. Radioterapii v předchozí léčbě podstoupilo téměř 20 procent pacientů a 26 procent bylo léčeno chemoterapií (irinotekan 26 %, leukovorin 33,9 %, platina 31,5 %). Téměř tři čtvrtiny pacientů (73,6 %) dostaly lipozomální irinotekan ve 2. linii léčby. Více než 80 procent pacientů dostalo plnou dávku naI‑IRI (70 mg/m2), ostatní měli dávku redukovanou (≤ 50 mg/m2). Ke změně dávky (nejčastěji snížení z důvodu NÚ) došlo u 11 pacientů. Medián délky léčby byl 2,3 měsíce, rozptyl délky léčby byl ale velmi variabilní (0–18,8 měsíce).
Primárním sledovaným parametrem bylo OS, definované jako čas od zahájení léčby do progrese onemocnění nebo úmrtí. Medián OS v ČR ve sledovaném období činil 10,1 měsíce s tím, že šestiměsíční pravděpodobnost přežití byla 57,1 procenta, což jsou lepší data, než ukazuje registrační studie NAPOLI‑1 (viz graf).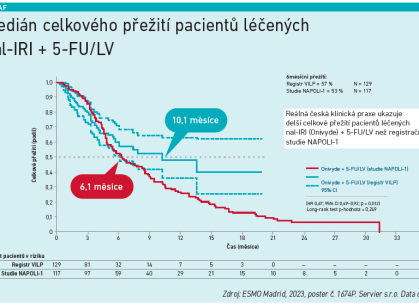
Sekundárními parametry bylo PFS, doba do selhání léčby (TTF), míra objektivní odpovědi na léčbu (ORR) a bezpečnost terapie. Medián PFS činil 3,5 měsíce, tedy srovnatelný s výsledky registrační studie. ORR dosáhla 10,1 procenta a medián doby do dosažení léčebné odpovědi 3,1 měsíce. U jednoho pacienta došlo ke kompletní remisi nemoci. Léčba nal‑IRI + 5‑FU/LV se ukázala být u pacientů s mPDAC dobře tolerovanou. Celkem bylo zaznamenáno 19 NÚ u 13,2 procenta pacientů, nejčastěji se jednalo o průjem nebo hematologickou toxicitu.
„Registr VILP potvrdil výsledky klinické studie NAPOLI‑1 v reálné praxi v rámci ČR, jak pokud jde o účinnost, tak i dobrou toleranci režimu nal‑IRI + 5‑FU/LV. Analýza dat doložila shodu šestiměsíční pravděpodobnosti přežití při této léčbě u pacientů z registru VILP a registrační studie (57 % vs. 53 %). Reálná česká klinická praxe potvrdila účinnost tohoto režimu po selhání nebo intoleranci chemoterapie na bázi gemcitabinu. Toho času vypočtené delší celkové přežití pacientů léčených nal‑IRI + 5‑FU/LV než v registrační studii NAPOLI‑1 (10,1 vs. 6,2 měsíce) poukazuje na velmi racionální indikaci českých onkologů v běžné klinické praxi,“ shrnula prof. Mohelniková Duchoňová.
Pegylovaný lipozomální irinotekan jako standard léčby ve 2. linii mPDAC
Kazuistiku odrážející zkušenosti z klinické praxe s nal‑IRI jako standardem léčby ve 2. linii mPDAC prezentovala MUDr. Věra Benešová z Onkologického oddělení Nemocnice Jihlava.
Pacientka 68 let, dosud bez interních komorbidit, bez pravidelné medikace, byla akutně přijata na Interní oddělení Nemocnice Jihlava v srpnu 2022 pro náhle vzniklý obstrukční ikterus. Pacientka (chronická kuřačka, astenička – 178 cm, 56 kg) před vznikem ikteru pozorovala jen lehké nechutenství. Vstupní sonografie břicha ukázala multilokulární cysticko‑solidní ložisko ve středním epigastriu nejasné biologické povahy působící dilataci intra‑ i extrahepatálních žlučových cest. Následné CT vyšetření 9. 8. potvrdilo maligně imponující solidně‑cystický tumor těla a kaudy pankreatu, výraznou dilataci žlučových cest, ascites v malé pánvi a divertikulózu sigmatu. Vstupní laboratorní vyšetření zaznamenalo výrazně zvýšené hodnoty nádorového markeru Ca19‑9: 8 388 kU/l značící diseminované onemocnění s očekávatelným horším průběhem a rychlou progresí. Dále BIL: 263, ALT: 5,25, GGT: 22.
První ERCP 10. 8., které mělo zprůchodnit žlučové cesty, bylo neúspěšné, proto byla zavedena zevní drenáž žlučových cest. 12. 8. po regresi edému doporučen pokus o další ERCP a 26. 8. se podařilo zavést metalický stent. Mezitím bylo 15. 8. provedeno endosonografické vyšetření slinivky břišní s biopsií. Histologie ukázala nález ojedinělých buněk adenokarcinomu.
Po úspěšné drenáži žlučových cest došlo k úpravě laboratorních hodnot a odeznění ikteru a pacientka byla indikována k vyšetření multidisciplinárním týmem s nálezem: lokálně pokročilý karcinom slinivky břišní, s postižením pobřišnice, vstupně ascites, vT4 cNO M1, st. IV, ECOG 1. Multidisciplinární tým doporučil aplikaci systémové paliativní chemoterapie.
„Výběr chemoterapie pohledem onkologa vychází z doporučení ČOS (Modrá kniha), která jsou každý rok aktualizována. Víme, že dnes má pacient s metastatickým onemocněním pankreatu průměrnou dobu přežití 11 měsíců. Cílem onkologické léčby těchto nemocných je stabilizace nebo regrese onemocnění s prodloužením délky života při zachování nebo zlepšení jeho kvality. Při volbě chemoterapeutického režimu bychom neměli zohledňovat jen jeho účinnost a efektivitu, ale i jeho toxicitu, přání a sociální situaci nemocného a možnosti dopravní dostupnosti,“ uvedla MUDr. Benešová.
V 1. linii léčby byla po posouzení celkové kondice pacientky zvolena chemoterapie monoterapií gemcitabinem inj. Léčba byla zahájena v září 2022 a byla velmi dobře tolerována, bez NÚ. Klinický stav pacientky se stabilizoval, nehubla, zvládala svůj život v domácím prostředí, proto po měsíci léčby v říjnu 2022 pokračováno v aplikaci kombinační chemoterapie gemcitabin + nab‑paklitaxel inj. Kombinační léčba probíhala také s dobrou tolerancí (aplikace po 14 dnech ambulantně), z NÚ byla pozorována jen sekundární alopecie, pacientka nehubla, byla bez bolestí, jaterní testy stabilizované.
Kontrolní vyšetření v únoru 2023 po třech měsících kombinační terapie popisuje parciální regresi onemocnění. Maligně imponující solidně‑cystický tumor těla a kaudy pankreatu ukazuje ve srovnání s předchozím vyšetřením CT parciální regresi cystoidů a nehomogenních hmot, hodnoty Ca 19‑9 poklesly na 356 kU/l. Po osmi měsících léčby v 1. linii dochází v květnu 2023 podle CT k progresi onemocnění. Byl zaveden venózní port, klinický stav pacientky zůstává nadále dobrý (ECOG 1).
„Ve 2. linii léčby jsme na základě předchozích velmi dobrých zkušeností a dle doporučení ČOS zvolili aplikaci lipozomálního irinotekanu s 5‑FU/LV. U pacientky nebyl nalezen polymorfismus v genu DPYD související se sníženou funkcí enzymu dihydropyrimidin dehydrogenázy. Léčba byla zahájena ambulantně koncem května 2023. Dle doporučení byla k prevenci nauzey aplikována setronová antiemetika, pacientka pokračovala v nutriční podpoře, byla s léčbou spokojena, začaly jí růst vlasy. Již po třech cyklech chemoterapie došlo k výraznému poklesu hodnot nádorového markeru Ca 19‑9 na 165 kU/l. Po šesti týdnech léčby však nastalo zhoršení stavu, pacientka byla přijata na onkologické oddělení pro týden trvající průjmy a dehydrataci, vyšetření vyloučila náhlou příhodu břišní. Pacientka netolerovala perorální příjem potravy, proto byla zavedena parenterální výživa. Průjmy ale přetrvávaly, proto bylo indikováno kolonoskopické vyšetření (bez patologického nálezu). Během čtyřtýdenní hospitalizace došlo pomalu k úpravě počtu i konzistence stolic a k úpravě celkového klinického stavu, pacientka byla postupně převáděna na perorální stravu. Aplikace systémové chemoterapie se přerušila na sedm týdnů. Po třech týdnech od propuštění byl konzultován postup další léčby – subjektivně se cítila dobře, přibrala na váze, frekvence stolic se nezvyšuje a sama měla aktivní zájem v léčbě pokračovat. Klinicky je již patrný výskyt ascitu, který není tenzní, elevace Ca 19‑9 na 871 kU/l. Vzhledem k dobré kondici pacientky bylo rozhodnuto v kombinační léčbě nal‑IRI + 5‑FU/LV pokračovat. I přes dlouhé přerušení léčby ukázalo kontrolní CT vyšetření epigastria v listopadu 2023 stabilizaci tumoru, pokles Ca 19‑9 na 333 kU/l. V současné době pacientka pokračuje v ambulantní aplikaci kombinační terapie se zachovanou kvalitou života. „V 1. linii byla léčena osm měsíců, což bylo nadstandardní, nyní již pokračuje dalších osm měsíců v léčbě 2. linie a toho času žije 17 měsíců od zjištění diagnózy, přestože její vstupní parametry byly velmi negativní a bylo i otázkou, zda nějakou léčbu bude možno vůbec nasadit. Při pohledu na časovou osu vidíme, že management pacienta s metastatickým onemocněním je z pohledu onkologa velmi náročný, pacienta musíme hodnotit komplexně a přihlížet k jeho různým problémům,“ zdůraznila MUDr. Benešová.
Pacientů s metastatickým karcinomem pankreatu přibývá. „Zatímco dříve jsme viděli dva za rok, dnes se každý měsíc jedná o několik pacientů. O tyto nemocné je potřeba pečovat komplexně a měli bychom respektovat i jejich přání. Významným faktorem je zde velmi omezená doba života, i když ta se v posledních letech prodloužila ze šesti na jedenáct měsíců a u individuálních respondérů lze dosáhnout i podstatně delší doby. Zásadním faktorem zde proto zůstává zachování dobré kvality života,“ uzavřela MUDr. Benešová. Jak se odborníci shodují, v klinické praxi mohou nejen dobu přežití, ale i kvalitu života pozitivně ovlivnit právě správně zvolené kombinační možnosti systémové terapie. Jeví se jako výhodné nasadit v 1. linii chemoterapii gemcitabin + nab‑paklitaxel, aby se mohlo ve 2. linii pokračovat kombinační léčbou s lipozomálním irinotekanem.