Konopí v léčbě bolesti
SOUHRN
Chronická neztišitelná bolest je nejčastější indikací použití konopí pro léčebné účely. Využíváme ho zejména v léčbě bolesti neuropatické a u onkologických pacientů. Kromě toho zmírňuje projevy spasticity a má výborný antiemetický efekt, možnosti jeho léčebného využití jsou ale mnohem širší. Konopí mohou v současnosti předepisovat pouze lékaři některých specializací, příslušné indikace stanovuje vyhláška. Článek seznamuje s mechanismy působení kanabinoidů na organismus prostřednictvím endokanabinoidního systému, uvádí hlavní indikace a kontraindikace léčby konopím a zmiňuje i praktické aspekty preskripce.
Klíčová slova: konopí pro léčebné účely • tetrahydrokanabinol • kanabidiol • endokanabinoidní systém • neuropatická bolest • nádorová bolest
Summary
Chronic intractable pain is the most common indication of medical cannabis. We use it mainly in the treatment of neuropathic pain and for cancer patients. In addition, it alleviates the symptoms of spasticity and has an excellent antiemetic effect, but the possibilities of its therapeutic use are much wider. Currently, cannabis can only be prescribed by doctors with certain specializations, the approved indications are specified by a law. The article describes the mechanisms of action of cannabinoids on the body, the function of the endocannabinoid system, presents the main indications and contraindications of cannabis treatment and mentions the practical aspects of its prescription.
Key words: medical cannabis • tetrahydrocannabinol • cannabidiol • endocannabinoid system • neuropathic pain • cancer pain
Úvod
Ačkoli konopí provází lidstvo od nepaměti, ať už jako součást lidového léčitelství, euforizující látka, nebo technická plodina, teprve systematické vědecké zkoumání mechanismu jeho účinku spolu s objevem endokanabinoidního systému nám umožňuje postupně objevovat komplexní účinek této rostliny na organismus a její terapeutický potenciál.
Konopí pro léčebné účely, jak zní oficiální název při jeho použití v medicíně, představují sušené samičí květy rostliny Cannabis sativa L. nebo Cannabis indica L. s přesně definovaným rozmezím obsahu tetrahydrokanabinolu a kanabidiolu. V České republice bylo konopí pro léčebné účely legalizováno v roce 2013, nicméně na český trh vstoupilo až v roce 2015 a finančně dostupné pro pacienty je pak od ledna 2020 po zavedení 90% úhrady ze zdravotního pojištění při preskripci do 30 g/měsíc. Tím se výrazně zvýšil zájem o tuto léčbu jak ze strany pacientů, tak i předepisujících lékařů.
Chronická neztišitelná bolest je vůbec nejčastější indikací použití léčebného konopí. Přestože v řadě preklinických i klinických studií prokázalo terapeutický efekt, závěry metaanalýz a systemických review jsou zatím opatrné,1 stejně tak jako doporučení odborných lékařských společností.
Stanovisko Evropské federace bolesti (European Pain Federation, EFIC) z roku 2018 je takové, že konopí má být předepisováno zkušeným lékařem jako součást multidisciplinárního přístupu a preferenčně coby adjuvantní léčba tam, kde léky první nebo druhé linie nepřinesly dostatečný efekt nebo nebyly tolerovány. Množství a kvalita důkazů podporují indikaci pro neuropatickou bolest, u ostatních typů bolesti je pak terapie konopím možná jako individuální terapeutický pokus. Během léčby musí být pacient monitorován.2
Účinné látky v konopí
Rostlina konopí obsahuje více než sto různých kanabinoidů, z nichž nejznámějšími a nejvíce prozkoumanými jsou tetrahydrokanabinol (delta‑9‑tetrahydrokanabinol, THC) a kanabidiol (CBD).
THC zodpovídá za psychotropní efekt a tím i za většinu nežádoucích účinků. Psychotropní efekt se může projevovat euforií, úzkostí, poruchou paměti, změnou vnímání času, halucinacemi nebo poruchou motoriky a koordinace. Intenzita tohoto účinku je závislá na dávce. Kromě toho má ale i účinek analgetický, antispastický, antiemetický a stimuluje chuť k jídlu.3 Po požití přechodně zvyšuje srdeční frekvenci a tlak, způsobuje sucho v ústech a zarudnutí spojivek.
CBD nemá psychotropní efekt, naopak tlumí některé nežádoucí účinky THC. Jeho efekt je antipsychotický, anxiolytický, antikonvulzivní a protizánětlivý.3
Účinky a využití dalších kanabinoidů jsou předmětem intenzivního zkoumání, pozornost je věnována např. protizánětlivým účinkům nepsychotropního kanabigerolu (CBG).3
V konopí je zastoupena řada dalších látek, zejména terpenů a flavonoidů, které interagují s kanabinoidy a podílejí se tak na výsledném synergickém působení rostliny, tzv. entourage efektu.4,5
Endokanabinoidní systém
Existence endokanabinoidního systému byla objevena na počátku 90. let 20. století. Reguluje celou řadu fyziologických procesů organismu, jeho funkce je komplexní a stále není zcela prozkoumána. Sestává z receptorů, ligandů – endokanabinoidů – a enzymů pro jejich syntézu a degradaci. Podílí se zejména na regulaci bolesti, a to jak na supraspinální, tak i na spinální a periferní úrovni, a je dokonce částečně funkčně propojen s opioidním systémem. Je zapojen i do modulace paměti, nálady, koordinace pohybů, tělesné teploty, příjmu potravy, systému odměny i neuroprotekce. Dále ovlivňuje imunitní funkce, kardiovaskulární systém i reprodukci.6 Hlavními kanabionoidními receptory jsou CB1 a CB2, nicméně kanabinoidy modulují i další receptory, např. ze skupiny kanálů TRP (transient receptor potential).
Receptory CB1 se nacházejí převážně v CNS, a to zejména v oblasti kortexu, hipokampu, striata, mozečku a olfaktoriálního bulbu.7 Téměř však chybějí v oblasti dechového centra v prodloužené míše, což vysvětluje, že ani po požití vysokých dávek konopí nedojde k útlumu dechového centra, na rozdíl od působení např. opioidů nebo benzodiazepinů. Receptory CB1 najdeme i v periferním nervovém systému, zejména na sympatických nervových zakončeních, ale také v játrech, svalech, kostech, kůži a reprodukčním systému; nacházejí se především na presynaptických nervových zakončeních a modulují, resp. většinou inhibují uvolňování různých neurotransmiterů.7
Receptory CB2 najdeme převážně na buňkách imunitního systému. V CNS jsou zastoupeny méně než receptory CB1, nacházejí se na mikrogliích (imunitní buňky CNS odvozené od makrofágů) a jsou výrazně inducibilní. Role těchto receptorů spočívá v modulaci chronické bolesti a potlačování chronického zánětu.8
THC působí jako parciální agonista receptorů CB1 a CB2. CBD je naopak nekompetitivním negativním alosterickým modulátorem receptorů CB 1 a CB2, čímž snižuje jejich schopnost vázat THC a zmírňuje tak jeho nežádoucí účinky.9
Mezi hlavní endokanabinoidy patří anandamid (arachidonoyletanolamid, AEA) a 2AG (2‑arachidonoylglycerol), jejichž spoluobjevitelem je český vědec Lumír Hanuš. Roli hrají především v endogenní modulaci bolesti.
Indikace konopí v léčbě bolesti
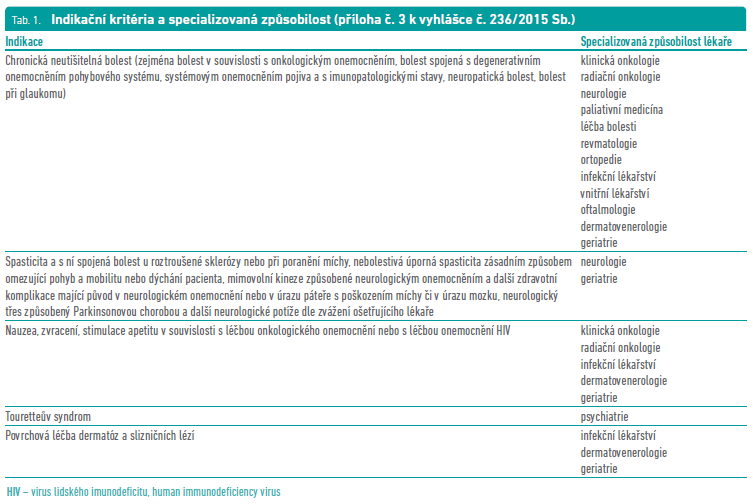
Všechny schválené indikace konopí pro léčebné účely jsou součástí vyhlášky 236/2015 Sb. (tab. 1). Vyplývá z ní, že ho lze využít v léčbě bolesti prakticky jakékoli etiologie.
Neuropatická bolest je jednou z hlavních indikací k léčbě konopím, kde byl prokázán dobrý klinický efekt. Jedná se o bolest v důsledku léze somatosenzorického nervového systému. Škála léků, které ji dokážou ovlivnit, je omezená a jejich efekt mnohdy nedostatečný, případně zatížený nežádoucími účinky. V léčbě nejčastěji používáme antiepileptika gabapentin a pregabalin, tricyklická antidepresiva (amitriptylin, nortriptylin), inhibitory zpětného vychytávání serotoninu a noradrenalinu (SNRI) venlafaxin a duloxetin. Z opioidů je indikován především tramadol, tapentadol a oxykodon. Z lokálních terapeutik pak lidokain a kapsaicin.
Konopí může přinést efekt v případech selhání této terapie. Mezi jeho indikace tak patří bolestivá polyneuropatie různé etiologie, nejčastěji diabetická10, prokázán byl efekt i při HIV neuropatii11. Využít ho můžeme i u postherpetické neuralgie, bolesti po poranění periferních nervů nebo v případě failed back surgery syndrome (FBSS).
Bolest při poškození míchy patří k dalším indikacím podpořeným studiemi.12 Setkáváme se s ní zejména u roztroušené sklerózy, po míšních traumatech, tumorech nebo při syringomyelii. U těchto stavů se současně uplatňuje antispastický efekt konopí.
Bolest a spasticita u roztroušené sklerózy (RS) jsou také častou indikací s prokázaným efektem. Čistě k léčbě spasticity u RS je registrován i nabiximols (Sativex) – konopný extrakt s THC a CBD ve formě oromukózního spreje, který ale již dlouhodobě není dostupný na českém trhu.
Fibromyalgie představuje obtížně léčitelný syndrom s dosud nejasnou etiologií charakterizovaný plošnou muskuloskeletální bolestí s palpační citlivostí v typických bodech, i zde léčba konopím může přinést významné zmírnění symptomů.13
Zdá se, že konopí lze využít i u bolesti při revmatoidní artritidě, kde se uplatňuje rovněž jeho protizánětlivý efekt.14
Ve studiích konopí prokázalo překvapivě dobré výsledky na redukci záchvatů migrény,15,16 ačkoli se běžně pro tuto diagnózu nepoužívá.
Kromě analgetického efektu konopí si pacienti často pochvalují zlepšení kvality spánku, někdy i zmírnění úzkosti a deprese.
U onkologických pacientů podáváme konopí s cílem zmírnit nejen vlastní nádorovou bolest, ale často i bolest vzniknuvší v důsledku operačního zákroku, radioterapie a chemoterapie. Konopí je také jedním z nejúčinnějších antiemetik,17 a lze ho tak použít ke zmírnění nauzey a zvracení při chemoterapii. Dalším jeho vítaným efektem u těchto pacientů je stimulace chuti k jídlu. Při poruše polykání nebo funkce zažívacího traktu je výhodná vaporizační forma podání. Konopí tak může významně přispět ke kvalitě života pacientů v paliativní péči.
Dronabinol a nabilon jsou syntetické kanabinoidy podobné THC, které mají v některých zemích schválenou indikaci právě pro nauzeu a vomitus po chemoterapii a u kachexie při AIDS, v ČR dostupné nejsou.
Konopí a opioidy
Konopí lze v léčbě kombinovat s opioidy, předpokládá se dokonce synergické působení. Nicméně je potřeba opatrnosti vzhledem k možné potenciaci sedativního efektu a ovlivnění kognitivních funkcí, zejména u starších pacientů. Přidání konopí do medikace nám někdy dokonce dovolí opioidní léčbu redukovat. V řadě případů může být konopí bezpečnější alternativou k opioidům, neboť nevyvolává útlum dechového centra a má mnohem nižší návykový potenciál i výskyt abstinenčních příznaků.
Rizika a kontraindikace
Oproti jiným látkám řazeným mezi návykové i ve srovnání s některými běžně používanými léčivy má konopí mnohem menší toxicitu i návykový potenciál. Přesto není zcela neškodné. Za většinu nežádoucích účinků je zodpovědný THC.
Kardiovaskulární rizika: THC ovlivňuje kardiovaskulární aparát, přechodně zvyšuje srdeční frekvenci a krevní tlak, ale také může způsobit ortostatickou hypotenzi v důsledku vazodilatace. Efekt je závislý na dávce. Je třeba opatrnosti v případě jakýchkoli kardiovaskulárních rizikových faktorů v anamnéze a je kontraindikován při závažném kardiovaskulárním onemocnění.
CNS rizika: Uživatelé konopí mají vyšší riziko psychózy i rozvoje schizofrenie, zejména v případě genetické predispozice. V případě denního užívání konopí s velmi vysokým obsahem THC bylo zjištěno až pětinásobně vyšší riziko psychózy.18 U pacientů se závažným psychiatrickým onemocněním (bipolární porucha, schizofrenie) v osobní nebo rodinné anamnéze je konopí kontraindikováno.
Osoby mladší 25 let: Konopí se nedoporučuje pro nepříznivé ovlivnění vývoje mozku a rovněž kvůli vyššímu riziku rozvoje psychiatrického onemocnění.
Těhotenství a kojení: Konopí je kontraindikováno vzhledem k přestupu přes placentu a do mateřského mléka a prokázanému negativnímu vlivu na vyvíjející se mozek plodu.
Riziko závislosti: V porovnání s jinými návykovými látkami je mnohem menší, nicméně existuje, i když se týká hlavně rekreačních uživatelů. Opatrnosti je potřeba u osob s anamnézou abúzu jakýchkoli návykových látek.
Abstinenční příznaky: Po vysazení léčby se abstinenční příznaky udávají pouze u určité části pacientů, zejména při dlouhodobém užívání vysokých dávek THC. Příznaky zahrnují neklid, podrážděnost, úzkost, depresi, poruchu spánku a ztrátu chuti k jídlu. Při dávkách a obsahu THC běžně používaných pro léčebné účely většinou není problém konopí vysadit najednou bez jakýchkoli příznaků z odnětí.
Lékové interakce: Kanabinoidy jsou metabolizovány cestou jaterního cytochromu P450. Zejména CBD zde působí jako významný enzymatický inhibitor a tak může zvyšovat koncentraci, resp. toxicitu jiných léčiv. Stejné riziko platí i pro volně prodejné přípravky s CBD. Opatrnosti při indikaci konopí je potřeba i při současném užívání léků se sedativním účinkem a obecně při polypragmazii. Vzhledem k uvedenému způsobu metabolizace je namístě obezřetnost i u pacientů s poruchou jaterní funkce.
Pravidla preskripce a praktický postup
Lékař předepisující léčebné konopí musí mít jednu ze specializací daných vyhláškou (tab. 1). Neatestovaný lékař tedy recept na konopí vystavit nemůže. Žádost o umožnění preskripce se podává prostřednictvím webového formuláře na stránkách https://pristupy.sukl.cz.
Konopí pro léčebné účely se předepisuje jako individuálně připravovaný léčivý přípravek (IPLP) formou elektronického receptu v celkovém množství pouze na jeden měsíc. Na předpis je potřeba napsat číselnou diagnózu, v indikaci pro bolest je to vždy R521 – Chronická neztišitelná bolest. Dále se uvádí druh konopí (C. sativa nebo C. indica), procentuální obsah THC a CBD a také specifický číselný kód, který tento obsah reprezentuje (seznam všech číselných kódů je rovněž součástí vyhlášky). Konopí pro léčebné účely má stanovený přípustný obsah THC 0,3–21 % a CBD 0,1–19 %. V případě předpisu kapslí se udává množství konopí v jedné kapsli, počet kapslí, celkové množství konopí na jeden měsíc v gramech a nakonec způsob a frekvence podání. Pacientovi lze předepsat maximálně 180 g konopí na měsíc, s 90% úhradou pojišťovny do 30 g na měsíc.
Způsob podání a dávkování
Konopí předepisujeme buď ve formě magistraliter kapslí nebo jako rostlinný materiál k vaporizaci. Cestu podání volíme individuálně, každá z nich má své výhody i nevýhody. Pokud pacient nemá předchozí zkušenost s konopím, je obvykle jednodušší začít léčbu perorálními kapslemi. Vaporizace totiž vyžaduje jak investici do vaporizéru (v řádu několika tisíc), tak i zvládnutí jeho obsluhy. Efekt kapslí nastupuje pomaleji (1–3 hod.), ale trvá delší dobu (6–8 hod.), v případě vaporizace se dostavuje rychleji (5–10 min.), ale trvání je kratší (2–4 hod.).19 Titrace účinné dávky je také podstatně rychlejší u inhalačního podání. Dle charakteru obtíží je možné kapsle a vaporizaci kombinovat. Také lze v individuálních případech kombinovat konopí s různým poměrem THC a CBD (např. na noc konopí s vyšším obsahem THC a přes den s nízkým THC a vyšším CBD). V případě výroby kapslí musí konopí nejprve projít procesem dekarboxylace, při kterém dochází k přeměně kanabinoidních kyselin na účinné kanabinoidy, čímž se zvyšuje jeho efektivita.
Vaporizace je v podstatě inhalace par, tj. nedochází při ní ke spalování a tvorbě toxických látek jako při kouření cigarety, extrakce účinných látek je také efektivnější. Vaporizér navíc umožňuje nastavit teplotu (obvykle 160–200 °C), čímž lze dále optimalizovat léčebný efekt, neboť každá z účinných látek má jinou teplotu odpařování.
Ať už zvolíme kteroukoli cestu podání, začínáme vždy od nízkých dávek (strategie „start low, go slow“). V případě perorálního podání se doporučuje začít užitím jedné kapsle s obsahem 0,0625 g konopí, a to na noc pro možný sedativní efekt.20 Je také možné řídit se množstvím THC s doporučenou úvodní dávkou 2,5 mg THC.19
Zejména na počátku léčby, kdy se hledá optimální dávka a poměr THC/CBD, je potřeba značné trpělivosti jak ze strany lékaře, tak pacienta. K minimalizaci nežádoucích účinků můžeme zvolit konopí buď s vyváženým poměrem THC/CBD, nebo s nízkým obsahem THC a vyšším CBD. Nutno zdůraznit, že analgetický efekt mají obě látky. V případě nedostatečného efektu nebo špatné tolerance je vhodnější vyzkoušet konopí s jiným poměrem účinných látek namísto toho, abychom lék zcela vysadili.
Řízení motorových vozidel
Konopí je podle zákona (č. 463/2013 Sb.) zařazeno na seznam návykových látek. Je nutné pacienty poučit, že THC ovlivňuje schopnost řídit motorová vozidla. Míra reálného ovlivnění je závislá na dávce a časovém odstupu od požití, je individuální, někteří chroničtí uživatelé mohou mít vyvinutu určitou toleranci. Nicméně zákonem stanovená hranice koncentrace THC v krvi pro řidiče je 2 ng/ml, nad tuto hodnotu se jedná o přestupek, nad 10 ng/ml pak o trestný čin. Jako bezpečný odstup pro řízení motorových vozidel se pacientům doporučuje 12 hodin od poslední dávky.20 V případě pozitivního testu ze slin by měl pacient trvat na krevní zkoušce, která jediná má právní validitu.
Zdroje informací
Na stránkách SAKL.CZ, zřízených Státní agenturou pro konopí pro léčebné účely (SAKL), lze najít základní informace pro lékaře i pacienty, včetně přehledné mapy předepisujících lékařů a seznamu lékáren. Podrobnějším zdrojem odborných informací pro lékaře je kniha Léčebné konopí v současné medicínské praxi (Leoš Landa a kolektiv, Grada 2020). Pacientům se zájmem o léčbu konopím je pak možné doporučit stránky pacientského spolku KOPAC.CZ.
Závěr
Při respektování správné indikace, dávkování a kontraindikací představuje konopí účinný a relativně bezpečný prostředek v léčbě chronické bolesti. Jeho preskripce ovšem patří do rukou zkušeného specialisty a musí být součástí komplexní péče. Nezbytným předpokladem úspěšné léčby konopím je i důkladná edukace pacienta.
Literatura
- Mücke M, Phillips T, Radbruch L, et al. Cannabis-based medicines for chronic neuropathic pain in adults. Cochrane Database Syst Rev 2018;3:CD012182.
- Häuser W, Petzke F, Fitzcharles MA. Efficacy, tolerability and safety of cannabis‑based medicines for chronic pain management – An overview of systematic reviews. Eur J Pain 2018;22:455–470.
- Hanuš LO, Šulcová A, Landa L. Kanabinoidní látky a léčivá síla přírody. In: Landa L (ed.). Léčebné konopí v současné medicínské praxi. Praha: Grada Publishing, 2020; 38–57.
- Ben‑Shabat S, Fride E, Sheskin T, et al. An entourage effect: inactive endogenous fatty acid glycerol esters enhance 2‑arachidonoyl‑glycerol cannabinoid activity. Eur J Pharmacol 1998;353:23–31.
- Russo EB. Taming THC: potential cannabis synergy and phytocannabinoid‑terpenoid entourage effects. Br J Pharmacol 2011;163:1344–1364.
- Reich GE, Narouze SN. The Endocannabinoid System In: Narouze SN (ed.). Cannabinoids and Pain. Cham: Springer Intermational Publishing, 2021; 39–45.
- Reich GE, Narouze SN. Cannabinoid Receptor 1 (CB1) In: Narouze SN (ed.). Cannabinoids and Pain. Cham: Springer Intermational Publishing 2021; 47–54.
- Vučković S, Srebro D, Vujović KS, et al. Cannabinoids and Pain: New Insights From Old Molecules. Front Pharmacol 2018;9:1259.
- Laprairie RB, Bagher AM, Kelly MEM, Denovan‑Wright EM. Cannabidiol is a negative allosteric modulator of the cannabinoid CB1 receptor. Br J Pharmacol 2015;172:4790–4805.
- Wallace MS, Marcotte TD, Umlauf A, et al. Efficacy of Inhaled Cannabis on Painful Diabetic Neuropathy. J Pain 2015;16:616–627.
- Aly E, Masocha W. Targeting the endocannabinoid system for management of HIV‑associated neuropathic pain: A systematic review. IBRO Neurosci Rep 2021;10:109–118.
- Wilsey B, Marcotte TD, Deutsch R, et al. An Exploratory Human Laboratory Experiment Evaluating Vaporized Cannabis in the Treatment of Neuropathic Pain From Spinal Cord Injury and Disease. J Pain 2016;17:982–1000.
- Sagy I, Bar‑Lev Schleider L, Abu‑Shakra M, Novack V. Safety and Efficacy of Medical Cannabis in Fibromyalgia. J Clin Med 2019;8:807.
- Blake DR, Robson P, Ho M, et al. Preliminary assessment of the efficacy, tolerability and safety of a cannabis‑based medicine (Sativex) in the treatment of pain caused by rheumatoid arthritis. Rheumatology 2006;45:50–52.
- Aviram J, Vysotski Y, Berman P, et al. Migraine Frequency Decrease Following Prolonged Medical Cannabis Treatment: A Cross‑Sectional Study. Brain Sci 2020;10:360.
- Cuttler C, Spradlin A, Cleveland MJ, Craft RM. Short‑ and Long‑Term Effects of Cannabis on Headache and Migraine. J Pain 2020;21:722–730.
- Zikos TA, Nguyen L, Kamal A, et al. Marijuana, Ondansetron, and Promethazine Are Perceived as Most Effective Treatments for Gastrointestinal Nausea. Dig Dis Sci 2020;65:3280–3286.
- Forti MD, Quattrone D, Freeman TP, et al, and the EU‑GEI WP2 Group. The contribution of cannabis use to variation in the incidence of psychotic disorder across Europe (EU‑GEI): a multicentre case‑control study. Lancet Psychiatry 2019;6:427–436.
- MacCallum C, Russo E. Practical considerations in medical cannabis administration and dosing. Eur J Intern Med 2018;49:12–19.
- Hřib R, Pecháčková M, Šaloun J. Kanabinoidy v léčbě chronické neonkologické bolesti In: Landa L (ed.). Léčebné konopí v současné medicínské praxi. Praha: Grada Publishing, 2020; 83–96.