Sedm roků, které změnily život pacientům s ATTR-CM
Na programu XXXIII. výročního sjezdu České kardiologické společnosti v Brně nechybělo ani odborné sympozium společnosti Pfizer věnované transthyretinové amyloidóze a s ní spojené kardiomyopatii. Nové přístupy k její diagnostice a léčbě byly předmětem diskuse odborníků ze čtyř specializovaných pracovišť. Závěr byl jednoznačný: díky dostupnosti specifické léčby v uplynulých sedmi letech se prognóza pacientů výrazně zlepšila. Klíčové zůstává včasné odhalení nemoci a zahájení její terapie v méně pokročilém stadiu.
Možnosti diagnostiky a specifické léčby ATTR‑CM v podmínkách českého zdravotnictví
Základní poznatky o jedné z forem systémové amyloidózy, transthyretinové kardiomyopatii (ATTR‑CM), shrnul ve svém úvodním sdělení prof. MUDr. Tomáš Paleček, Ph.D., z II. interní kliniky kardiologie a angiologie 1. LF UK a VFN v Praze. Transthyretin (TTR) je transportní protein produkovaný téměř výhradně játry. V organismu plní důležité fyziologické funkce – podílí se na transportu thyroxinu a retinol‑vázajícího proteinu. Destabilizace tetramerní struktury TTR, její disociace na monomery, následná agregace do amyloidních fibril odolných vůči proteolýze a jejich ukládání v extracelulárním prostoru myokardu ve formě amyloidových depozit představují hlavní patofyziologické mechanismy vzniku ATTR‑CM. „Transthyretinovou amyloidózu dělíme na dvě hlavní formy: získanou, tzv. wild‑type ATTR, která se objevuje převážně u starších osob a dříve byla označována jako senilní systémová amyloidóza, a dále na dědičnou, tzv. variantní formu ATTR, vznikající na podkladě mutací v genu pro TTR na 18. chromozomu,“ upozornil prof. Paleček s tím, že hereditární forma ATTR‑CM je poměrně vzácná. Ještě v roce 2012 byla ATTR‑CM považována za málo časté a relativně dobře snášené onemocnění, ale od roku 2006 její výskyt, především wild‑type formy, setrvale roste, pravděpodobně i díky přesnější diagnostice, neinvazivní kostní scintigrafii.
Signály, které nelze ignorovat
ATTR‑CM může stát v pozadí řady stavů napříč specializacemi. Nejčastěji souvisí se srdečním selháním, především se zachovanou ejekční frakcí, ale lékaři by na ni měli myslet i u pacientů s hypertrofickou kardiomyopatií bez jasné příčiny, s aortální stenózou nebo poruchami převodního systému – AV blokádami vyššího stupně. Upozornit na amyloidózu může i nepřiměřeně vysoká koncentrace NT‑proBNP neodpovídající klinickému stavu. U nemocných v NYHA I–II nejsou výjimkou hodnoty tohoto biomarkeru v tisících. Varovné je také kolísání krevního tlaku nebo přechod z léčené arteriální hypertenze do symptomatické hypotenze. Na EKG bývá nápadná nízká voltáž QRS komplexu při současném zvýšení hmotnosti levé komory. Přínosná je i magnetická rezonance, typické nálezy jsou difuzní subendokardiální ztluštění a pozdní sycení gadoliniem. Přehlédnout bychom neměli ani extrakardiální vodítka, která často předcházejí srdečním příznakům. Patří k nim oboustranný a opakovaný syndrom karpálního tunelu, stenóza páteřního kanálu, ruptura šlachy bicepsu nebo známky idiopatické polyneuropatie. Tyto nálezy by měly vést k podezření na ATTR‑CM a k dalším vyšetřením.
Srdeční selhání je převládající klinickou manifestací
Přehledová studie, která v uplynulém roce proběhla ve čtyřech českých centrech specializovaných na srdeční amyloidózu, potvrdila, že nejčastějším symptomem vedoucím k diagnostice wild‑type formy ATTR‑CM bylo srdeční selhání (62 %). Důležitým vodítkem může být syndrom karpálního tunelu, a to i jednostranný. Podle literatury se vyskytuje v anamnéze u více než 50 procent pacientů s wild‑type formou ATTR‑CM. „V naší studii dosahovala četnost syndromu karpálního tunelu u nemocných s ATTR‑CM 54 procent,“ uvedl přednášející a připomněl, že znalost typických klinických projevů ATTR‑CM vede k zachycení pacientů v méně pokročilých fázích onemocnění.
Jak rozpoznat ATTR‑CM včas?
Diagnostika ATTR‑CM může být složitá, protože typické klinické ani echokardiografické známky nemusejí být vždy přítomny. Proto se postupuje podle diagnostického algoritmu, jehož hlavním cílem je odlišit ATTR‑CM od AL amyloidózy. Prvním krokem je laboratorní vyšetření: stanovení poměru volných lehkých řetězců kappa/lambda v séru i moči a imunofixace séra a moči. Pokud jsou tyto výsledky normální, pokračuje se kostní scintigrafií s použitím radiofarmaka 99mTc‑DPD. Pozitivita ve stupni 2–3 podle Peruginiho kritérií potvrzuje přítomnost ATTR‑CM. V případě abnormálních laboratorních nálezů nebo scintigrafie pouze na stupni 1 je nezbytné provést endomyokardiální biopsii. Ta slouží k rozlišení mezi ATTR‑CM a AL amyloidózou. Další podpůrná vyšetření, jako jsou EKG, echokardiografie, srdeční magnetická rezonance (MR) nebo genetika, jsou užitečná zejména při podezření na hereditární formu nemoci. „Pozitivita DPD skenu bez ohledu na stupeň 2 až 3 v kombinaci s absencí abnormálních poměrů volných lehkých řetězců kappa/lambda má stoprocentní specificitu a pozitivní prediktivní hodnotu pro diagnostiku ATTR‑CM a tato kombinace je v současnosti pro diagnózu dostačující bez nutnosti bioptického průkazu, samozřejmě doplněná o všeobecné vyšetření,“ upřesnil prof. Paleček. Data z českých center ukazují, že u 63 procent pacientů lze ATTR‑CM diagnostikovat neinvazivně, zatímco u zbývajících 37 procent je nutná biopsie.
Podpůrná terapie i cílená léčba
Léčba ATTR‑CM má složku podpůrnou, zmírňující příznaky srdečního selhání, a specifickou, jež ovlivňuje průběh nemoci. Ta se zaměřuje na potlačení tvorby TTR v játrech, odstranění amyloidových usazenin v srdci a stabilizaci TTR. Název sympozia se odkazuje k roku 2018, kdy byla na kongresu Evropské kardiologické společnosti (ESC) představena III. fáze randomizované multicentrické studie ATTR‑ACT, která potvrdila účinnost přípravku tafamidis u obou forem nemoci ve srovnání s placebem. Během 30 měsíců užívání přípravku došlo k významnému snížení kombinovaného end‑pointu – celkové mortality a hospitalizací pro kardiovaskulární příčiny – o 29 procent u wild‑type formy a o 31 procent u formy hereditární. Tafamidis současně zpomalil zhoršování fyzické kondice a kvality života. „Pozitivní efekt se projevil až po 18 měsících, proto je důležité zahájit léčbu co nejdříve,“ zdůraznil prof. Paleček. Díky lepší diagnostice ve specializovaných centrech i dostupnosti léčby je dnes prognóza českých pacientů s ATTR‑CM výrazně příznivější.
Současnost diagnostiky ATTR‑CM a význam screeningu rizikových populací
Doc. MUDr. Miloš Kubánek, Ph.D., z Kliniky kardiologie IKEM podtrhl význam včasné diagnostiky nemoci: „ATTR‑CM můžeme pomocí farmakoterapie stabilizovat, můžeme předejít závažným kardiovaskulárním příhodám a snížit mortalitu nemocných. Nejsilnější data máme ve třídě jedna a dva.“ Z diagnostických metod vyzdvihl význam EKG, kde může být nápadný rozpor mezi nízkou voltáží QRS komplexů a hypertrofií levé komory. Umělá inteligence ve studii rozpoznala ATTR‑CM z EKG s vysokou přesností (AUC 0,85–0,91). Přesnost echokardiografického hodnocení byla ještě vyšší a kombinace obou metod dále zvyšovala úspěšnost diagnostiky. Cílem diagnostického úsilí by tedy mělo být dosažení podobné, případně vyšší přesnosti. Jak diagnostickou výtěžnost v praxi zlepšit?
Význam EKG vyšetření u amyloidóz
Nízká voltáž v končetinových svodech EKG se objevuje častěji u AL amyloidózy (cca 55 %) než u ATTR‑CM (35 %). U pacientů s ATTR‑CM bývá tento nález spojen s vyšším rizikem fibrilace síní, častějším perikardiálním výpotkem, menším objemem levé komory a zhoršenou funkcí pravé komory srdeční. U obou forem amyloidózy signalizuje nízká voltáž QRS komplexu horší prognózu.
Kombinace EKG a echokardiografie
Italská studie ACTIVE provedená u více než 5 300 osob nad 55 let odhalila echokardiograficky suspektní nález ATTR‑CM u sedmi procent z nich. Typické znaky zahrnovaly ztluštění stěn levé komory, ztuhnutí septa a chlopní, perikardiální výpotek, granulární strukturu myokardu nebo apikální „sparing“. ATTR‑CM byla potvrzena u čtvrtiny těchto pacientů. Užitečným markerem se ukázal poměr sumy voltáží QRS komplexů ve 12svodovém EKG k tloušťce stěny levé komory (negativní prediktivní hodnota 96 %, pozitivní 64 %). „Je tedy důležité u těchto pacientů kombinovat hodnocení EKG, echokardiografie a ukazují se i nové markery, které by mohly posloužit při diagnostice ATTR‑CM,“ dodal doc. Kubánek a zmínil, že probíhají studie zaměřené na prevalenci tohoto onemocnění v různých rizikových skupinách.
Rizikové populace
U pacientů nad 60 let se srdečním selháním se zachovanou ejekční frakcí a se septem ≥ 12 mm byla ATTR‑CM potvrzena ve 13 procentech případů. Po chirurgické výměně aortální chlopně byla u pacientů starších 65 let prevalence šest procent, po katetrové náhradě (TAVI) až 16 procent. Mezi rizikové skupiny patří i nemocní s fibrilací síní a pacienti s implantovaným kardiostimulátorem. V česko‑německé studii byla ATTR‑CM diagnostikována u osmi procent nemocných nad 65 let s nově zjištěnou fibrilací síní a alespoň jedním rizikovým faktorem – zvýšeným BNP, hypertrofií levé komory nebo recidivou fibrilace. U pacientů s trvalým kardiostimulátorem a tloušťkou septa > 12 mm byla pomocí scintigrafie a testů na monoklonální gamapatii zjištěna ATTR‑CM v devíti procentech případů. Hypertrofie levé komory byla přítomna téměř u poloviny z nich. Podobnou prevalenci (cca 15 %) uvádí i ostravská studie.
Doc. Kubánek zakončil svůj příspěvek slovy: „Je důležité korelovat nález na EKG a echokardiografii. Nízká voltáž QRS komplexu je přítomna jen u třetiny pacientů s ATTR‑CM, užitečnějším ukazatelem je proto suma voltáží QRS komplexu na 12svodovém EKG, kterou porovnáváme s maximálním ztluštěním stěny levé komory srdeční. Na ATTR‑CM je třeba myslet i u tradičních skupin, jako je srdeční selhání se zachovanou ejekční frakcí nebo aortální stenóza, ale také u pacientů s fibrilací síní či trvalou kardiostimulací pro atrioventrikulární blokádu.“
Arytmie a náhlá smrt u ATTR‑CM
MUDr. Hana Poloczková, Ph.D., z I. interní kardioangiologické kliniky LF MU a FN u sv. Anny v Brně se zaměřila na srdeční arytmie u pacientů s ATTR‑CM. Tyto arytmie jsou časté a multifaktoriální, mohou být latentní i manifestní, závislé na typu amyloidózy a stadiu onemocnění. U pacientů s ATTR‑CM jsou hůře snášeny, protože zhoršují hemodynamiku, projevy srdečního selhání, zvyšují počet hospitalizací a celkově negativně ovlivňují kvalitu života. „Mezi mechanismy a faktory, které se podílejí na vzniku arytmií, patří toxicita amyloidních fibril, ztluštění myokardu s rozvojem fibrózy, cytotoxický efekt amyloidních prekursorů, infiltrace převodního systému amyloidem, specifické nálezy, které se nacházejí v oblasti levé síně, kde také častěji dochází k infiltraci amyloidem, a celkový inflamatorní stav organismu,“ vyjmenovala MUDr. Poloczková. Konstatovala, že chybějí aktuální doporučené postupy pro péči o pacienty s arytmií a ATTR‑CM kvůli omezeným klinickým datům, převaze retrospektivních studií a malým kohortám často křehkých nemocných s řadou komorbidit, které jsou vyřazovány z větších analýz. A s jakými převodními poruchami se u nemocných s ATTR‑CM můžeme setkat?
AV blokáda
Retrospektivní studie Donnellana a kol. sledovala 369 pacientů s wild‑type i hereditární formou ATTR‑CM. Nejčastější abnormalitou při této diagnóze byl široký QRS komplex (51 %, resp. 48 % pacientů) a AV blok 1. stupně (49 %, resp. 43 %). Pokročilou AV blokádu vyžadující kardiostimulaci mělo 9,5 procenta nemocných. Během 28 měsíců sledování se u dalších 10–12 procent rozvinula pokročilá AV blokáda, což potvrzuje progresivní postižení převodního systému. Studie autorů Porcari a kol. identifikovala prediktory implantace kardiostimulátoru: prodloužený PR interval, šířku QRS komplexu ≥ 120 ms, tloušťku mezikomorového septa a anamnézu fibrilace síní. Woltze a kol. zjistili, že výskyt tří rizikových faktorů u pacienta s ATTR‑CM výrazně zvyšuje riziko potřeby trvalé kardiostimulace. Do jednoho roku od implantace byl srdeční rytmus u nemocných stimulován přibližně z 50–60 procent, po pěti letech téměř u všech stoprocentně. Pravokomorová stimulace měla negativní dopad na levou komoru – snižovala ejekční frakci, zhoršovala srdeční selhání, mitrální regurgitaci a zvyšovala počet hospitalizací. Proto se preferuje resynchronizační terapie a stimulace levého Tawarova raménka, ovšem soubory nemocných zařazených do studií jsou zatím malé.
Fibrilace síní
Další častou arytmií u pacientů s ATTR‑CM je fibrilace síní (FS), která se vyskytuje přibližně u 40 procent nemocných. K jejímu vzniku přispívá amyloidová infiltrace levé síně, porucha cévní funkce, systémový zánět a změny v systému srážení krve. Vzhledem k vysokému riziku arteriální trombózy a embolizace je u těchto pacientů vždy indikována trvalá antikoagulační léčba, a to i při zachovaném sinusovém rytmu. Co se týká antikoagulační terapie, mezi warfarinem a přímými perorálními antikoagulancii (DOAC) nebyl prokázán rozdíl v účinnosti. Léčba FS může směřovat buď ke kontrole rytmu (preferovaná strategie), nebo ke kontrole srdeční frekvence. Management léčby ale komplikuje častá intolerance některých přípravků. S opatrností může být zváženo podání dofetilidu, jehož použití se v minulosti nedoporučovalo, ale dnes je znovu zvažováno. Standardem zůstávají betablokátory a antikoagulancia. Udržení sinusového rytmu je u pacientů s amyloidózou obecně méně úspěšné než v běžné populaci. Pokud je však FS zachycena v časném stadiu, může být obnova a stabilizace rytmu možná. V takových případech lze zvažovat elektrickou kardioverzi. Ta ale nese vyšší riziko recidivy arytmie a komplikací. Riziko přítomnosti trombu přetrvává i při správně vedené antikoagulaci – až u 30 procent nemocných lze při transezofageální echokardiografii odhalit trombus v oušku levé síně. Proto je vždy nutné před plánovanou kardioverzí toto vyšetření provést. U pacientů v časnějších stadiích onemocnění se jako účinná a bezpečná jeví katetrizační ablace. U vysoce rizikových pacientů, u nichž není možná trvalá antikoagulace, lze jako prevenci tromboembolických komplikací zvážit i uzávěr ouška levé síně.
Komorové arytmie
Na rozdíl od pacientů s AL amyloidózou se komorové arytmie u osob s ATTR‑CM vyskytují méně často. Data o jejich výskytu a prognostickém významu jsou však zatím omezená, většinou pocházejí z retrospektivních nebo observačních studií. V jedné z novějších prospektivních studií, která sledovala 72 pacientů, byl zaznamenán výskyt nestabilních komorových tachykardií u 44 procent z nich. Přesto se v tomto souboru nevyskytla žádná závažná arytmie vedoucí k náhlé srdeční smrti. Prognostický význam komorových arytmií u ATTR‑CM zatím není jednoznačně stanoven. Rizikové kalkulačky pro náhlou srdeční smrt, běžně používané například u hypertrofické kardiomyopatie, nelze u této diagnózy spolehlivě použít. U pacientů s ATTR‑CM totiž bývá náhlá smrt způsobena jinými mechanismy – například bradykardií, elektromechanickou disociací nebo důsledkem pokročilého srdečního selhání. Je ale důležité poznamenat, že tato zjištění vycházejí převážně ze starších studií, které sledovaly pacienty s výrazně pokročilým onemocněním. Nemusejí tedy přesně odrážet aktuální situaci u nemocných diagnostikovaných a léčených v časnějších fázích. Implantace kardioverter‑defibrilátoru (ICD) je v tomto kontextu jednoznačně doporučena pouze v rámci sekundární prevence, tedy po prodělané srdeční zástavě, za předpokladu, že očekávané přežití přesahuje 12 měsíců. V oblasti primární prevence je situace méně jednoznačná a zůstává předmětem odborných diskusí. Evropská doporučení připouštějí zvážení implantace ICD u pacientů s amyloidózou (AL amyloidóza a ATTR‑CM), pokud prodělali hemodynamicky netolerovanou komorovou tachykardii. I v takových případech je ale zásadní komplexní zhodnocení celkového stavu a prognózy pacienta.
MUDr. Poloczková v závěru shrnula, že arytmie, zejména fibrilace síní, jsou u pacientů s ATTR‑CM časté, je nutné myslet na kontrolu rytmu, prevenci kardioembolizace, stimulaci srdečního rytmu a implantaci kardiostimulátoru, a to zejména u nemocných v časných stadiích s dobrým funkčním stavem a prognózou. Prevence náhlé srdeční smrti však stále zůstává nejasná.
Riziková stratifikace a prognóza nemocných s ATTR‑CM
Poslední vstup celého sympozia připravila MUDr. Renáta Aiglová, Ph.D., z II. interní kliniky – kardiologické LF UP a FN Olomouc. Upozornila, že prognóza hlavních typů amyloidóz způsobujících postižení srdce (AL amyloidóza a ATTR‑CM) je velmi nepříznivá, zejména pokud se průběh onemocnění nepodaří ovlivnit léčbou. Medián přežití pacientů s ATTR‑CM činí v 1. stadiu méně než šest let, ve 2. stadiu méně než čtyři roky a ve 3. stadiu pouze dva roky od stanovení diagnózy.
Progrese onemocnění se sleduje pomocí klinických a funkčních markerů (hospitalizace, zhoršení srdečního selhání, zhoršení kvality života, zhoršení tolerance zátěže), biomarkerů (NT‑proBNP, srdeční troponiny) a zobrazovacích metod (progrese hypertrofie stěny levé komory, systolická a diastolická dysfunkce, převodní poruchy). Pro odhad prognózy a stratifikaci rizika u ATTR‑CM je vhodné využít některý ze stagingových systémů.
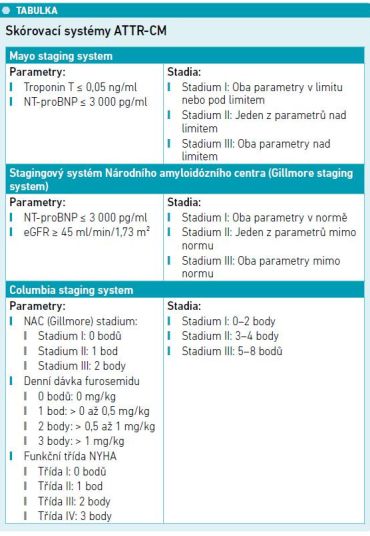 Mayo staging systém pracuje s hodnotami NT‑proBNP a troponinu T. Systém National Amyloidosis Centre (NAC), vyvinutý Gillmorem a kol., zahrnuje NT‑proBNP a odhadovanou glomerulární filtraci (eGFR). Columbia staging system kombinuje laboratorní parametry s klinickými údaji – konkrétně denní dávkou furosemidu a funkčním stavem podle klasifikace NYHA. S pomocí skórovacích systémů lze rovněž hodnotit efektivitu terapie (viz tabulku).
Mayo staging systém pracuje s hodnotami NT‑proBNP a troponinu T. Systém National Amyloidosis Centre (NAC), vyvinutý Gillmorem a kol., zahrnuje NT‑proBNP a odhadovanou glomerulární filtraci (eGFR). Columbia staging system kombinuje laboratorní parametry s klinickými údaji – konkrétně denní dávkou furosemidu a funkčním stavem podle klasifikace NYHA. S pomocí skórovacích systémů lze rovněž hodnotit efektivitu terapie (viz tabulku).
Vliv časné selektivní terapie na průběh ATTR‑CM
Tafamidis (Vyndaqel) působí jako selektivní stabilizátor TTR – váže se s vysokou afinitou na místa pro thyroxin a stabilizuje tetramer, čímž zpomaluje jeho disociaci na monomery a následnou tvorbu amyloidových depozit. Účinnost léčby je výrazně ovlivněna načasováním zahájení terapie.
Data z klinických studií ukazují, že pacienti s ATTR‑CM léčení již od 1. stadia nemoci měli ve srovnání s těmi, kteří zahájili léčbu později, nižší mortalitu, menší pokles kvality života, fyzické zdatnosti i renálních funkcí. Význam časné terapie potvrdila i studie porovnávající skupinu léčenou přípravkem tafamidis ihned po stanovení diagnózy s pacienty, u nichž byla medikace zahájena až po 30 měsících podávání placeba. Pacienti ve funkční třídě NYHA I–II a ve stadiu 1 podle jednotlivých stagingových systémů (Mayo, NAC, Columbia) dosahovali jednoznačně lepších výsledků. Dlouhodobá data shromáždil i mezinárodní registr THAOS, který potvrdil nejen příznivý efekt specifické léčby na průběh onemocnění, ale i demografický profil nemocných: ATTR‑CM postihuje převážně muže nad 70 let, u většiny se jedná o wild‑type formu, převažuje funkční třída NYHA I–II a zvýšené koncentrace NT‑proBNP. MUDr. Aiglová upozornila i na výsledky studie, která k hodnocení myokardiálního postižení využívala magnetickou rezonanci. Ve srovnání s referenční skupinou vykazovali léčení pacienti stabilní hodnoty enddiastolického tlaku a objemu. Nedocházelo k dalšímu nárůstu hypertrofie levé komory, byla zachována její systolická funkce a strainová analýza naznačila příznivý vývoj i v oblasti pravé komory, včetně zlepšení parametrů její deformace.
Publiku MUDr. Aiglová na závěr vzkázala: „Ve všech sděleních bylo ukázáno, že ATTR‑CM se stále pojí s nepříznivou prognózou. Snažili jsme se vás přesvědčit o tom, že včasná diagnostika a včasné zahájení léčby je stěžejní pro ovlivnění prognózy našich pacientů. Máme pro sledování pacientů a progrese onemocnění k dispozici různé systémy, různou metodiku, ale obecně můžeme říct, že ve všech stagingových systémech jsou běžně dostupné laboratorní, zobrazovací, EKG a klinické parametry. Dostupnou léčbou prokázanou klinickými studiemi i daty z reálné klinické praxe můžeme dosáhnout stabilizace onemocnění. Uvidíme, co nás čeká do budoucna.“