ROZHOVOR: U trombózy (zvláště atypické) mysleme na PNH
Paroxysmální noční hemoglobinurie (PNH) představuje vzácné onemocnění, jehož podkladem je získaná klonální porucha kmenové krvetvorné buňky. V jejím…
Iptakopan se dle ATC klasifikace řadí mezi Imunosupresiva, Inhibitory komplementu (L04AJ08).
Komplementový systém zahrnuje více než 40 solubilních i membránově vázaných proteinů, které kooperují mezi sebou i s dalšími komponentami imunitního systému. Hlavní funkcí komplementu, nespecifické součásti imunitního systému, je zprostředkování opsonizace a stimulace chemotaxe fagocytujících buněk. Nadměrná a nedostatečně regulovaná aktivace komplementu však může vést k řadě patologických stavů a ke tkáňovému poškození [1]. Mezi onemocnění asociovaná s vrozenými poruchami regulačních složek komplementu, v jejichž terapii je možné využít právě iptakopan, řadíme paroxysmální noční hemoglobinurii (PNH) a glomerulopatii C3 složky komplementu (C3G).
PNH je vzácné hematologické onemocnění. Rozvíjí se v důsledku získané mutace genu PIG‑A kmenové krvetvorné buňky, který kóduje tzv. GIP (glykosylfosfatidylinositolovou) kotvu. Ta váže v membráně krevních buněk řadu molekul. Některé z nich jsou inhibitory tzv. MAC (membrane attack complex), tlumí působení komplementu a chrání tak buňky před hemolýzou. Membrány krevních buněk vznikajících z narušených kmenových buněk proto nemají dostatečnou odolnost vůči komplementu. PNH je onemocnění charakterizované zejména intravaskulární hemolýzou. Příčinou hemolýzy je nadměrná citlivost erytrocytů ke komplementu (viz výše), obzvláště při mírném okyselení organismu (k němu dochází zejména během spánku při zvýšené retenci oxidu uhličitého; v noci tedy dochází k atakám hemolýzy, které se ráno projeví hemoglobinurií – odtud název). Uvolněný hemoglobin i poškození buněk zprostředkované komplementem vedou k aktivaci koagulačního systému a uvolňování prozánětlivých faktorů. Právě trombotické komplikace představují častou příčinu úmrtí nemocných s PNH. Mohou být i prvním projevem onemocnění [2].
C3 glomerulopatie představuje vzácné heterogenní onemocnění, pro které je typické progredující renální postižení. Roli hrají vlivy genetické a autoimunitní. V patogenezi se uplatňuje nadměrná aktivace alternativní složky komplementu. Mezi klinické projevy patří hematurie, proteinurie, nefrotický syndrom a často též těžká arteriální hypertenze [3].
Iptakopan je nízkomolekulární vysoce účinný inhibitor proximálního komplementu, první ve své třídě. Cílí na faktor B a tím selektivně inhibuje alternativní dráhu komplementové kaskády 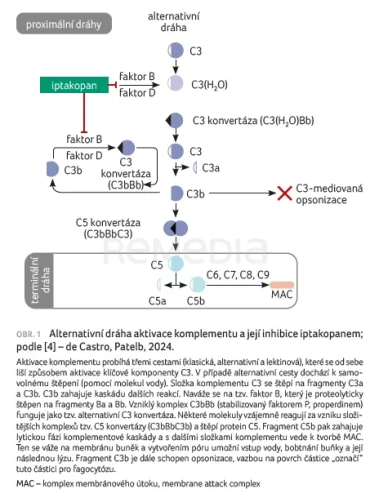 (obr. 1) [4]. U PNH zabraňuje tato inhibice aktivaci C3 konvertázy a následné tvorbě C5 konvertázy pro kontrolu extravaskulární hemolýzy zprostředkované C3 i terminální intravaskulární hemolýzy zprostředkované komplementem.
(obr. 1) [4]. U PNH zabraňuje tato inhibice aktivaci C3 konvertázy a následné tvorbě C5 konvertázy pro kontrolu extravaskulární hemolýzy zprostředkované C3 i terminální intravaskulární hemolýzy zprostředkované komplementem.
U C3G vede nadměrná aktivace alternativní dráhy komplementu k ukládání C3 v glomerulech, což vyvolává zánět, poškození glomerulů a fibrózu ledvin. Iptakopan selektivně blokuje nadměrnou aktivaci alternativní dráhy inhibicí aktivity C3 konvertázy související s alternativní dráhou, což vede ke snížení štěpení C3 a k omezení jeho ukládání v ledvinách.
Iptakopan je rychle absorbován. Maximální plazmatické koncentrace je dosaženo asi za dvě hodiny po podání [5]. Při doporučeném dávkovacím režimu 200 mg dvakrát denně je v průběhu celého dávkovacího intervalu dosahováno průměrné koncentrace ≥ 1 000 ng/ml, což se jeví jako optimální pro účinnou inhibici alternativní dráhy komplementu [5]. Rovnovážného stavu je dosaženo přibližně za pět dní (s malou akumulací, asi 1,4násobně). Maximální plazmatická koncentrace v ustáleném stavu je 4 020 ng/ml a plocha pod křivkou plazmatické koncentrace (AUCtau,ss) 25 400 ng*h/ml. Jejich výše není ovlivněna tučným jídlem ani potravou obecně. Proto je možné iptakopan podávat bez ohledu na jídlo [6]. Iptakopan má rovněž nízkou interindividuální variabilitu [5,6].
Vazba iptakopanu na plazmatické proteiny je závislá na koncentraci (75–93 %). Geometrický průměr zdánlivého distribučního objemu v rovnovážném stavu je přibližně 265 litrů.
Převládající cestou eliminace iptakopanu z organismu je metabolizace, přibližně z 50 % oxidací (zejména CYP2C8, méně CYP2D6). Vedlejší cestou eliminace je přímá glukuronidace (uridindifosfát glukuronosyltransferázy UGT1A1, UGT1A3 a UGT1A8). Metabolity iptakopanu nejsou považovány za farmakologicky aktivní. Na základě studie se zdravými dobrovolníky se ukazuje, že iptakopan se z více než 70 % vylučuje stolicí a téměř z 25 % močí. Biologický poločas iptakopanu v rovnovážném stavu je přibližně 25 hodin [6].
Přípravek je indikován v monoterapii k léčbě paroxysmální noční hemoglobinurie (PNH) u dospělých pacientů, kteří mají hemolytickou anémii. Druhou indikací je léčba glomerulopatie C3 složky komplementu (C3G) u dospělých pacientů. Přípravek se podává v kombinaci s inhibitorem renin‑angiotenzinového systému (RAS). Při jeho nesnášenlivosti nebo kontraindikaci je indikován iptakopan v monoterapii [6].
Kontraindikací léčby iptakopanem je hypersenzitivita na léčivou látku nebo na kteroukoliv pomocnou látku přípravku. Použití inhibitorů komplementu, jako je iptakopan, může predisponovat k závažným život ohrožujícím nebo fatálním infekcím způsobeným opouzdřenými bakteriemi. Z tohoto důvodu je léčba kontraindikovaná též u pacientů, kteří nejsou očkováni proti bakteriím Neisseria meningitidis a Streptococcus pneumoniae (pokud riziko odkladu léčby nepřeváží riziko vzniku infekce). Zároveň se doporučuje očkovat pacienty proti Haemophilus influenzae typu B (nejméně dva týdny před zahájením léčby).
Léčba iptakopanem je kontraindikovaná rovněž u pacientů s nevyřešenou infekcí způsobenou opouzdřenými bakteriemi, včetně bakterií N. meningitidis, Str. pneumoniae nebo H. influenzae typu B, při zahájení léčby [6].
Je třeba upozornit, že očkování (viz výše) snižuje, ale nevylučuje riziko závažné infekce. Pacienty je proto třeba na riziko upozornit a sledovat případné známky infekce. Při podezření na infekci by měla být okamžitě zahájena protiinfekční léčba. Přerušení léčby iptakopanem během závažné infekce je třeba zvážit na základě posouzení přínosů a rizik.
Pacienti s PNH užívající iptakopan mají být též pravidelně monitorováni s ohledem na riziko hemolýzy. Mezi její známky patří zvýšení hodnot laktátdehydrogenázy (LDH) spolu s náhlým poklesem koncentrace hemoglobinu nebo zmenšením velikosti PNH klonu, únava, hemoglobinurie, bolest břicha, dyspnoe, dysfagie, erektilní dysfunkce nebo závažné nežádoucí cévní příhody (včetně žilní nebo arteriální trombózy). V případě, že musí být léčba ukončena, je třeba sledovat pacienty ještě po dobu dvou týdnů po poslední dávce [6].
Iptakopan se podává v dávce 200 mg užívané perorálně dvakrát denně bez ohledu na jídlo. Dodržování dávkovacího schématu je obzvlášť důležité u pacientů s PNH kvůli minimalizaci rizika hemolýzy. Jedná se o dlouhodobou léčbu. Při vynechání dávky je třeba užít jednu dávku co nejdříve (i krátce před následující plánovanou dávkou) a pokračovat v pravidelném dávkovacím schématu. V případě vynechání více dávek je žádoucí kvůli riziku hemolýzy pacienta monitorovat [6].
U seniorů (≥ 65 let), pacientů s lehkou a středně těžkou poruchou funkce ledvin (eGFR ≥ 30 ml/min) ani s lehkou nebo středně těžkou poruchou funkce jater (Childovo–Pughovo skóre třídy A, B) není potřeba žádná úprava dávky. U nemocných s těžkou poruchou funkce ledvin nebo závislých na dialýze nejsou dostupná data, proto nelze podávat žádná doporučení ohledně dávkování. U pacientů s těžkou poruchou funkce jater (Childovo–Pughovo skóre třídy C) se podávání iptakopanu nedoporučuje. U pacientů mladších 18 let nejsou dostupné údaje o účinnosti a bezpečnosti, proto nelze podávání doporučit.
U pacientů přecházejících z terapie ekulizumabem má být léčba zahájena nejpozději jeden týden po poslední dávce ekulizumabu, u ravulizumabu nejpozději šest týdnů po poslední dávce ravulizumabu [6].
Účinnost a bezpečnost iptakopanu u dospělých pacientů s PNH byly hodnoceny ve dvou multicentrických otevřených 24týdenních studiích fáze III: studie APPLY‑PNH kontrolovaná aktivním komparátorem (NCT04558918) a jednoramenná studie APPOINT‑PNH (NCT04820530).
Do klinického hodnocení byli zařazeni pacienti s hodnotou hemoglobinu nižší než 10 g/dl. Ve studii APPLY‑PNH se jednalo o pacienty dosud léčené anti‑C5 terapií, kteří buď pokračovali dál v této terapii (n = 35; ekulizumab n = 23, ravulizumab n = 12), nebo byli randomizováni do skupiny léčené iptakopanem (n = 62). Jednoramenná studie APPOINT‑PNH sledovala monoterapii iptakopanem u 40 pacientů, kteří dosud nebyli léčeni inhibitory komplementu a jejichž aktivita LDH byla vyšší než 1,5násobek horní hranice normálního rozmezí.
V obou studiích léčba iptakopanem zlepšila u pacientů s perzistující anémií hematologické a klinické výsledky. Efekt terapie iptakopanem byl pozorován již sedmý den léčby a v dalším období přetrvával 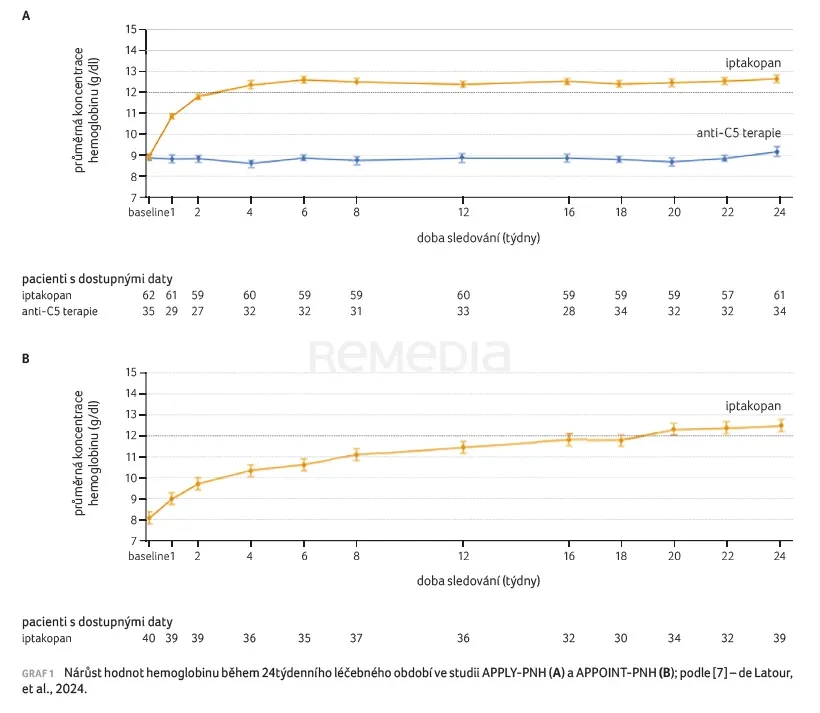 (graf 1) [7]. Efekt 24 týdenní terapie ve studii APPLY‑PNH byl hodnocen na základě dvou primárních cílových ukazatelů: podíl pacientů s trvalým zvýšením hodnot hemoglobinu o ≥ 2 g/dl oproti výchozí hodnotě a/nebo vzestup koncentrace hemoglobinu na ≥ 12 g/dl (v obou případech bez transfuze erytrocytů). Iptakopan prokázal superioritu oproti anti‑C5 terapii při dosažení hematologické odpovědi bez nutnosti transfuze
(graf 1) [7]. Efekt 24 týdenní terapie ve studii APPLY‑PNH byl hodnocen na základě dvou primárních cílových ukazatelů: podíl pacientů s trvalým zvýšením hodnot hemoglobinu o ≥ 2 g/dl oproti výchozí hodnotě a/nebo vzestup koncentrace hemoglobinu na ≥ 12 g/dl (v obou případech bez transfuze erytrocytů). Iptakopan prokázal superioritu oproti anti‑C5 terapii při dosažení hematologické odpovědi bez nutnosti transfuze 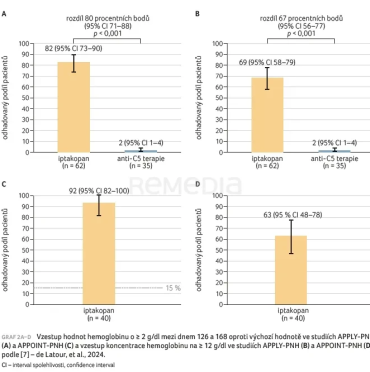 (graf 2A, B) [7].
(graf 2A, B) [7].
Primárním cílovým ukazatelem ve studii APPOINT‑PNH byl podíl pacientů s trvalým zvýšením hodnot hemoglobinu o ≥ 2 g/dl oproti výchozí hodnotě po 24 týdnech léčby, podíl pacientů s nárůstem hodnot hemoglobinu na ≥ 12 g/dl představoval sekundární cílový ukazatel. Tyto výsledky demonstruje graf 2C, D.
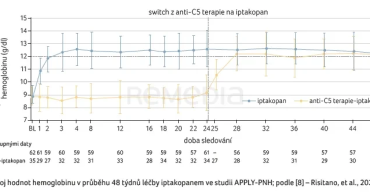
Po 24 týdnech léčby mohli pacienti ve studii APPLY‑PNH pokračovat do 24týdenní extenze hodnocení (pacienti léčení anti‑C5 terapií byli převedeni na iptakopan). Data po 48 týdnech léčby dokládají, že účinnost iptakopanu zůstává i v dlouhodobém časovém horizontu setrvalá [8]. Efekt léčby iptakopanem se rychle projevil i ve skupině pacientů převedených v týdnu 24 z anti‑C5 terapie jak ve vývoji hodnot hemoglobinu (graf 3), tak v dalších sledovaných parametrech (snížení absolutního počtu retikulocytů, zlepšení skóre funkčního hodnocení léčby – únavy dle FACIT‑F, vyhnutí se transfuzi aj.).
 Bezpečnostní profil léčby byl ve 48. týdnu podobný jako ve 24. týdnu [8]. Po 48 týdnech léčby iptakopanem bylo pozorováno zlepšení skóre symptomů, celkového zdravotního stavu i funkčních domén EORTC QLQ‑C30 (European Organization for the Research and Treatment of Cancer Quality of Life Questionnaire). Zlepšení u pacientů, kteří přešli z anti‑C5 terapie na léčbu iptakopanem, bylo srovnatelné se zlepšením dosaženým u pacientů původně randomizovaných k užívání iptakopanu. Tyto výsledky jsou dokladem o dlouhodobém pozitivním vlivu iptakopanu na kvalitu života související se zdravím i na běžné příznaky PNH [8].
Bezpečnostní profil léčby byl ve 48. týdnu podobný jako ve 24. týdnu [8]. Po 48 týdnech léčby iptakopanem bylo pozorováno zlepšení skóre symptomů, celkového zdravotního stavu i funkčních domén EORTC QLQ‑C30 (European Organization for the Research and Treatment of Cancer Quality of Life Questionnaire). Zlepšení u pacientů, kteří přešli z anti‑C5 terapie na léčbu iptakopanem, bylo srovnatelné se zlepšením dosaženým u pacientů původně randomizovaných k užívání iptakopanu. Tyto výsledky jsou dokladem o dlouhodobém pozitivním vlivu iptakopanu na kvalitu života související se zdravím i na běžné příznaky PNH [8].
 C3 glomerulopatie
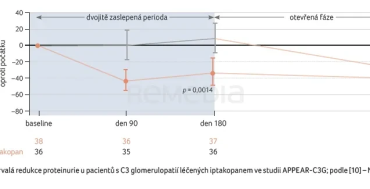
C3 glomerulopatieZásadním klinickým hodnocením pro indikaci iptakopanu v léčbě C3G je studie APPEAR‑C3G (NCT04817618) [9]. Do této multicentrické randomizované, dvojitě zaslepené studie kontrolované placebem byli zařazeni dospělí pacienti s C3G potvrzenou biopsií (n = 74). Iptakopan v dávce 200 mg dvakrát denně byl podáván šest měsíců v randomizovaném, dvojitě zaslepeném uspořádání s následnou šestiměsíční otevřenou fází léčby.
Sledovaným ukazatelem účinnosti bylo procentuální snížení 24hodinového UPCR (urine protein creatinine ratio) ve srovnání s výchozí hodnotou. Jak demonstruje graf 4, léčba iptakopanem vedla k dosažení výrazného a klinicky významného snížení proteinurie a toto snížení přetrvávalo po dobu 12 měsíců sledování [10]. Bezpečnostní profil léčby byl příznivý bez identifikace nových bezpečnostních signálů.
 Nežádoucí účinky
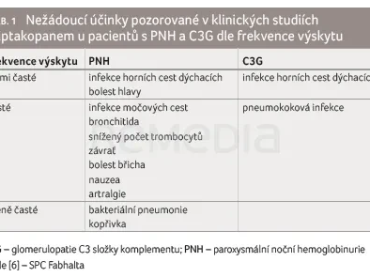
Nežádoucí účinkyNejčastěji hlášenými nežádoucími účinky u dospělých pacientů s PNH byly infekce horních cest dýchacích (18,9 %), bolest hlavy (18,3 %) a průjem (11,0 %). Nejčastěji hlášeným závažným nežádoucím účinkem byla infekce močových cest (1,2 %). Nejčastěji hlášeným nežádoucím účinkem u dospělých pacientů s C3G byla infekce horních cest dýchacích (12,9 %). Nejčastěji hlášeným závažným nežádoucím účinkem byla pneumokoková infekce (1 %). Nežádoucí účinky zaznamenané v klinických studiích s iptakopanem u pacientů s PNH a C3G dle frekvence výskytu prezentuje tabulka 1 [6].
Klinické hodnocení sledující možné interakce iptakopanu při současném podávání s jinými léčivými přípravky u zdravých dobrovolníků neprokázala žádné klinicky významné interakce [11].
In vitro data ukázala, že iptakopan má potenciál indukce CYP3A4 a mohl by snížit expozici senzitivním substrátům CYP3A4 (např. karbamazepin, cyklosporin, ergotamin, fentanyl, pimozid, chinidin, sirolimus, takrolimus). Současné podávání ale nebylo klinicky studováno, proto se doporučuje zvýšená opatrnost v případě, že je vyžadováno současné podávání.
Iptakopan má dále potenciál pro časově závislou inhibici CYP2C8, a může tak zvýšit expozici senzitivním substrátům CYP2C8 (např. repaglinid, dasabuvir, paklitaxel). Jejich současné podávání ale nebylo klinicky studováno, a proto je i v tomto případě nabádáno ke zvýšené opatrnosti. Současné podávání iptakopanu se silnými induktory CYP2C8, UGT1A1, P‑glykoproteinu, BCRP (breast cancer resistance protein) a OATP1B1/3 (organic anion transporting polypeptide B1/3) nebylo klinicky studováno, ale vzhledem k možnému snížení účinnosti iptakopanu se současné podávání nedoporučuje [6].
Onemocnění PNH je v těhotenství spojeno s nepříznivými riziky pro matku (zhoršující se cytopenie, trombotické příhody, infekce, krvácení, potrat i zvýšená mateřská mortalita) i pro plod (úmrtí plodu, předčasný porod). Rovněž C3G v těhotenství může být spojeno s nepříznivými následky pro matku (zejména preeklampsie a potrat) a pro plod (předčasný porod, nízká porodní hmotnost).
Údaje o podávání iptakopanu těhotným ženám jsou omezené, stejně tak nejsou k dispozici údaje o účinku iptakopanu na lidskou fertilitu. Studie reprodukční toxicity na zvířatech nenaznačují škodlivé účinky při maximální doporučené dávce pro člověka. Použití iptakopanu u těhotných žen nebo žen, které plánují otěhotnět, je možné zvážit pouze v nezbytném případě, na základě pečlivého posouzení přínosů a rizik.
Nejsou k dispozici údaje o tom, zda se iptakopan vylučuje do lidského mateřského mléka, jaké jsou jeho účinky na kojence nebo na tvorbu mléka. Riziko pro kojené novorozence/děti nelze vyloučit. Z tohoto důvodu se doporučuje po posouzení prospěšnosti kojení pro dítě/léčby pro matku ukončit kojení nebo léčbu iptakopanem [6].
Tisková publikace: Remedia ročník 35 číslo 3/2025 str. 208
Paroxysmální noční hemoglobinurie (PNH) představuje vzácné onemocnění, jehož podkladem je získaná klonální porucha kmenové krvetvorné buňky. V jejím…
Podle MUDr. Jaromíra Gumulce z FN Ostrava může paroxysmální noční hemoglobinurie dlouho probíhat bez příznaků a projevit se až atypickou či život…
Včasná diagnostika PNH a rychlé předání do centra rozhodují o osudu pacienta
PNH vyžaduje víc než antikoagulaci – cílená léčba komplementu snižuje riziko trombóz