Sedmileté výsledky otevřené prodloužené studie Glatiramer Acetate Low-frequency Administration (GALA)

Dlouhodobá účinnost a bezpečnost režimu dávkování glatiramer acetátu třikrát týdně u pacientů s relaps remitentní roztroušenou sklerózou
Cílem autorů práce, která byla uveřejněna v prosinci 2021 v časopise Multiple Sclerosis Journal – Experimental, Translational and Clinical, bylo ověřit dlouhodobé výsledky léčby s časným zahájením (early-start, ES) a odloženým začátkem (delayed-start, DS) glatiramer acetátem 40 mg/ml třikrát týdně (GA40) po dobu až sedmi let v rámci extenze studie GALA (Glatiramer Acetate Low-frequency Administration) (GALA) u pacientů s relaps remitentní roztroušenou sklerózou (RR-RS).
Studie GALA byla navržena pro ověření účinnosti a bezpečnosti GA40 jako dvanáctiměsíční, multicentrická, dvojitě zaslepená, placebem kontrolovaná klinická studie fáze III. Ukázalo se, že méně častý režim dávkování GA40 má profil účinnosti a bezpečnosti podobný jako u zavedeného režimu denního dávkování 20 mg/ml (GA20).
Po ukončení zaslepené fáze přešli pacienti do otevřené studie (open-label extention, OLE), v níž byli všichni léčeni GA40. Pacienti byli hodnoceni každé tři až šest měsíců.
Primárním cílovým parametrem účinnosti byl ARR (roční míra relapsů)
Pro účinnost byly pro kohorty ES a DS použity údaje z celého období expozice. Pro sledování bezpečnosti byla zvažována pouze expozice GA40.
Z pacientů, kteří pokračovali do OLE 580/834 (70 %) ve skupině ES a 261/419 (62 %) ve skupině DS sledování dokončilo. Po celé období placebem kontrolované a OLE studie bylo ARR 0,26 u pacientů skupiny ES a 0,31 u skupiny DS (HR = 0,83; 95% CI: 0,70–0,99). ES prodloužil střední dobu do prvního relapsu oproti DS (4,9 vs. 4,3 roku; HR = 0,82; 95% CI: 0,6–0,96).
Doba do šestiměsíčního potvrzení zhoršení disability (6mCDW) a procento pacientů bez progrese disability (6mCDW free)
Během celého období studie placebem kontrolované a otevřené fáze (placebo controlled and open and open-label extention, PC and OLE) měli pacienti v kohortě ES zhruba stejně dlouhou dobu do 6mCDW ve srovnání s kohortou DS (HR = 0,89; 95% CI: 0,69–1,16; p = 0,39) (viz graf a). Doba do 6mCDW pouze během období OLE se nelišila podle léčebné skupiny (HR = 1,11; 95% CI: 0,82–1,50; p = 0,49).
Procento pacientů, kteří zůstali bez progrese (6mCDW free), bylo v průběhu celého období studie PC a OLE podobné výchozímu stavu (88 % ve skupině ES a 87 % v kohortě DS; OR = 1,09; 95% CI: 0,81–1,47; p = 0,58) (viz graf b). Procento pacientů, kteří vykázali 6mCDW pouze během období OLE, se nelišilo podle léčebné skupiny (17 % u ES vs. 15 % u DS; OR = 1,22; 95% CI: 0,88–1,70; p = 0,22).
Změna EDSS od výchozí hodnoty během celého období studie PC a OLE
Průměrné hodnoty EDSS na začátku byly 2,81 pro ES a 2,75 pro DS. Během celého období studie PC a OLE byla průměrná změna od výchozí hodnoty podobná u ES i DS. Na konci prvního roku byla průměrná změna ve skupině ES −0,09 (± 0,03) a skupině DS −0,06 (± 0,04) s průměrným rozdílem −0,03 (95% CI: − 0,12–0,06; p = 0,52). Na konci sedmého roku byla průměrná změna také podobná jak ve skupině ES 0,25 (± 0,05), tak ve skupině DS 0,24 (± 0,07) s rozdílem 0,01 (95% CI: −0,14–0,17; p = 0,85).
Procento pacientů se stabilním nebo zlepšeným skóre EDSS bylo mezi kohortami podobné během celého období studie, stejně jako procento pacientů, kteří dosáhli EDSS 4 a EDSS 6. Podobně se doba k dosažení skóre EDSS 4 nebo 6 mezi skupinami významně nelišila.
Nežádoucí účinky byly v souladu se známým, dobrým a trvalým bezpečnostním profilem GA.
Závěr: Léčba GA40 měla klinický přínos po dobu sedmi let, což potvrzuje trvalou účinnost GA40. Terapie byla u pacientů s RR-RS obecně dobře tolerována.
Graf. Doba do šestiměsíčního potvrzení zhoršení disability (6mCDW) a procento pacientů bez progrese disability (6mCDW free)
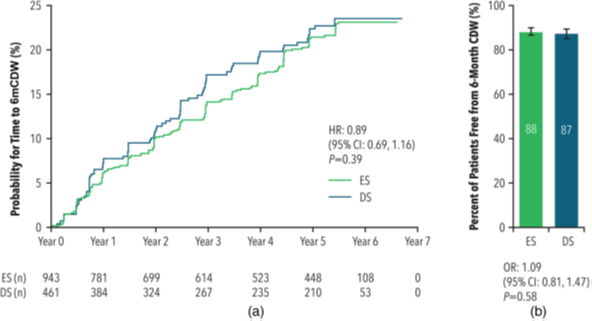
Vysvětlivky v textu
Zdroj:
Rieckmann P, et al. Multiple Sclerosis Journal – Experimental, Translational and Clinical. October–December 2021, 1–9, DOI: 10.1177/20552173211061550